
| A. | 标准状况下,11.2 L CCl4所含的分子数为0.5 NA | |
| B. | 常温常压下,4.2 g C2H4和C8H16的混合物中含有的碳原子数为0.3 NA | |
| C. | 7.8 g苯分子中碳碳双键的数目为0.3 NA | |
| D. | 6.4 g Cu与20 mL 10 mol•L-1浓硫酸反应,转移的电子数为0.2 NA |
分析 A、标况下四氯化碳为液体;
B、C2H4和C8H16的最简式均为CH2;
C、苯不是单双键交替的结构;
D、铜与稀硫酸不发生反应,所以反应生成的二氧化硫的物质的量减少,转移的电子数减少.
解答 解:A.标况下四氯化碳不是气体,不能使用标况下的气体摩尔体积计算11.2L四氯化碳的物质的量,故A错误;
B.4.2g C2H4和C8H16的混合物中含有0.3mol最简式CH2,含有0.3mol碳原子,含有的碳原子数为0.3NA,故B正确;
C.7.8g苯的物质的量为0.1mol,苯分子中的碳碳键为一种独特键,其分子中不存在碳碳双键,故C错误;
D.6.4g铜的物质的量为:$\frac{6.4g}{64g/mol}$=0.1mol,20mL 10mol•L-1浓硫酸中含有硫酸0.2mol,0.1mol铜完全反应需要消耗0.2mol,生成0.1mol二氧化硫,转移了0.2mol电子;由于随着反应的进行,浓硫酸变成稀硫酸,稀硫酸与铜不发生反应,所以反应生成的二氧化硫小于0.1mol,转移的电子小于0.2mol,转移的电子数小于0.2NA,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 吸热反应是由于反应物的总能量比生成物的总能量低 | |
| B. | 放热反应的△H>0 | |
| C. | 需要加热才能发生反应不一定是吸热反应 | |
| D. | 酸碱中和反应都是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①③④⑤ | C. | ①③⑤ | D. | ①③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸、纯碱、石灰石 | B. | 硝酸、烧碱、胆矾 | ||
| C. | 醋酸、碱式碳酸铜、醋酸钠 | D. | 盐酸、熟石灰、苛性钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
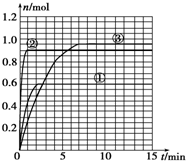 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z和W,它们的物质的量随时间的变化如下表所示.
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z和W,它们的物质的量随时间的变化如下表所示.| t/min | X/mol | Y/mol | Z/mol | W/mol |
| 0 | 2.00 | 1.00 | 0.00 | 0.00 |
| 1 | 1.80 | 0.80 | 0.20 | 0.10 |
| 3 | 1.50 | 0.50 | 0.50 | 0.25 |
| 5 | 1.30 | 0.30 | 0.70 | 0.35 |
| 9 | 1.10 | 0.10 | 0.90 | 0.45 |
| 10 | 1.10 | 0.10 | 0.90 | 0.45 |
| 14 | 1.10 | 0.10 | 0.90 | 0.45 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
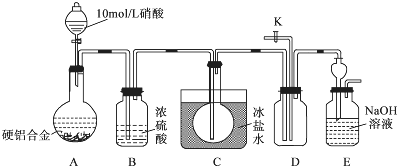
| 金属离子 | 开始沉淀时的pH | 沉淀完全的pH |
| Al3+ | 3.4 | 4.7 |
| Cu2+ | 4.1 | 6.9 |
| Mg2+ | 9.4 | 12.4 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
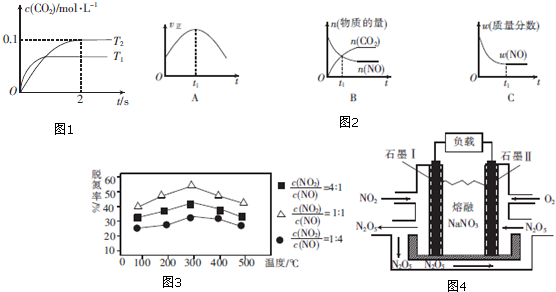
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
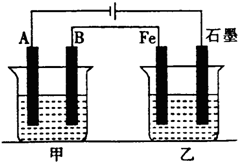 如图所示,甲、乙为相互串联的两电解池,甲池利用电解原理在铁上镀银,一段时间后,甲池阴极增重43.2g,乙中盛放足量的CuSO4溶液,请回答:
如图所示,甲、乙为相互串联的两电解池,甲池利用电解原理在铁上镀银,一段时间后,甲池阴极增重43.2g,乙中盛放足量的CuSO4溶液,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com