
【题目】按要求回答下列问题。
(1)写出下列有机物的结构简式:
①2,2,3,3-四甲基戊烷_________;
②2,5-二甲基庚烷____________;
③2,3-二甲基-6-乙基辛烷__________。
(2)写出下列物质的分子式:
①![]() ___________;
___________;
②![]() ___________;
___________;
(3)写出下列物质的键线式:
①![]() ___________;
___________;
②CH3CH=CHCH3___________;
(4)按系统命名法命名有机物CH3CH(C2H5)CH(CH3)2的名称是___________;
(5)![]() 所含官能团的名称是___________;该有机物发生加聚反应后,所得产物的结构简式为__________________。
所含官能团的名称是___________;该有机物发生加聚反应后,所得产物的结构简式为__________________。
【答案】CH3CH2C(CH3)2C(CH3)3 CH3CH(CH3)CH2CH2CH(CH3)CH2CH3 CH3CH(CH3)CH(CH3)CH2CH2CH(CH2CH3)2 C6H14 C7H12 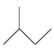
![]() 2,3-二甲基戊烷 碳碳双键、醛基
2,3-二甲基戊烷 碳碳双键、醛基 ![]()
【解析】
(1)烷烃分子中C原子之间以单键结合,剩余价电子全部与H原子结合,根据C原子价电子是4,结合烷烃系统命名方法书写物质结构简式;
(2)根据C原子价电子是4,每个拐点和顶点都是1个C原子,书写物质分子式;
(3)在键线式表示时,拐点和顶点表示1个C原子,单线表示碳碳单键,双线表示碳碳双键,据此书写物质的键线式表示;
(4)根据烷烃的系统命名方法对化合物命名;
(5)根据官能团的结构确定其名称,碳碳双键发生加成反应,双键变单键,然后彼此结合形成高分子化合物。
(1)①2,2,3,3-四甲基戊烷结构简式是:CH3CH2C(CH3)2C(CH3)3;
②2,5-二甲基庚烷的结构简式是:CH3CH(CH3)CH2CH2CH(CH3)CH2CH3;
③2,3-二甲基-6-乙基辛烷结构简式是:CH3CH(CH3)CH(CH3)CH2CH2CH(CH2CH3)2;
(2)①![]() 分子中含有6个C原子,由于分子中C原子间全部以单键结合,属于烷烃,分子式是C6H14;
分子中含有6个C原子,由于分子中C原子间全部以单键结合,属于烷烃,分子式是C6H14;
②![]() 分子中含有7个C原子,含有1个环和1个碳碳双键,因此该不饱和烃比烷烃少结合4个H原子,故其分子式是C7H12;
分子中含有7个C原子,含有1个环和1个碳碳双键,因此该不饱和烃比烷烃少结合4个H原子,故其分子式是C7H12;
(3)①![]() 的键线式表示为:
的键线式表示为: ;
;
②CH3CH=CHCH3的键线式表示为:![]() ;
;
(4)有机物CH3CH(C2H5)CH(CH3)2分子中最长碳链上含有5个C原子,从右端开始给主链上C原子编号,以确定支链的位置,该物质的名称是2,3-二甲基戊烷;
(5)![]() 所含官能团的名称是碳碳双键、醛基;该有机物分子中含有碳碳双键,在发生加聚反应时,不饱和碳碳双键中较活泼的键断开,然后这些不饱和C原子彼此结合,形成很长碳链,C原子变为饱和C原子,就得到相应的高聚物,故所得产物的结构简式为
所含官能团的名称是碳碳双键、醛基;该有机物分子中含有碳碳双键,在发生加聚反应时,不饱和碳碳双键中较活泼的键断开,然后这些不饱和C原子彼此结合,形成很长碳链,C原子变为饱和C原子,就得到相应的高聚物,故所得产物的结构简式为![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 1.00mol NaCl中含有6.02×1023个NaCl分子
B. 1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023
C. 欲配置1.00L ,1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中
D. 电解58.5g熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为九种主族元素在周期表中的位置:
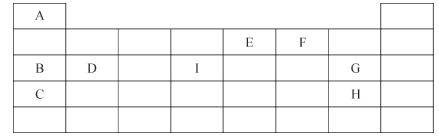
请回答下列问题:
(1)I元素的位置是第 ________周期,第______族。
(2)C、B、D 三种元素的金属性由强到弱的顺序为___________________(填元素符号)。
(3)E、F两种元素对应的最简单氢化物的稳定性:________________ (填化学式)。
(4)C的单质与稀盐酸反应的离子方程式为_________________________ 。
(5)G 的单质气体通入H、C形成化合物的水溶液中,写出该反应的化学方程式:______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeOCr2O3,还含有硅、铝等杂质。制备流程如图所示:
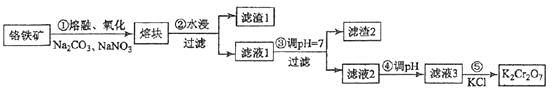
回答下列问题:
⑴步骤①的主要反应为:FeOCr2O3+Na2CO3+NaNO3![]() Na2CrO4 + Fe2O3 + CO2+ NaNO2
Na2CrO4 + Fe2O3 + CO2+ NaNO2
上述反应配平后FeOCr2O3与NaNO3的系数比为__________。该步骤不能使用陶瓷容器,原因是________________(可用化学方程式表示)。
⑵步骤④调滤液2的pH使之变_________(填“大”或“小”),原因是_________(用离子方程式表示)。
⑶有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体。冷却到10℃得到的K2Cr2O7固体产品最多,步骤⑤的反应类型是___________________。
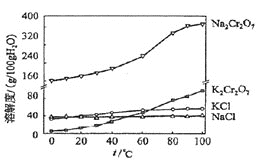
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验原理及操作中,正确的是
A.用酒精做萃取剂萃取碘水中的碘单质
B.配制![]() 溶液时,将称好的
溶液时,将称好的![]() 固体直接放入容量瓶中溶解
固体直接放入容量瓶中溶解
C.向某溶液中滴加![]() 溶液,有白色沉淀,再滴加足量稀HCl,若沉淀不溶解,则说明原溶液中一定含
溶液,有白色沉淀,再滴加足量稀HCl,若沉淀不溶解,则说明原溶液中一定含![]()
D.在某试样中加入NaOH溶液,加热,产生能使湿润的红色石蕊试液变蓝的气体即证明试样中含有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锑酸钠(NaSbO3)具有广泛的应用,可用作显像管、光学玻璃和各种高级玻璃的澄清剂,纺织品、塑料制品的阻燃剂,搪瓷乳白剂,制造铸件用漆的不透明填料及铁皮、钢板抗酸漆的成分。工业上用双氧水氧化法制备NaSbO33H2O的工艺流程如下:
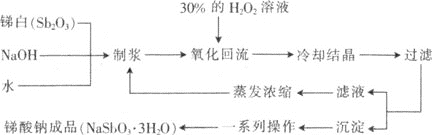
回答下列问题:
⑴NaSbO33H2O中Sb的化合价为________。
⑵先将锑白、氢氧化钠和水按一定的比例制浆,制浆过程中,搅拌、加热的目的是________。
⑶将制得的浆液加热至适当温度后,慢慢滴入30%的H2O2溶液进行氧化回流,温度不宜过高的原因是________。此过程中涉及反应如下,配平此化学方程式:
____Sb2O3 + ____H2O2 + ____NaOH + ____H2O = ____NaSbO33H2O。
⑷此流程中,可以循环利用的主要物质有________。
⑸“沉淀”主要成分为锑酸钠,流程中“一系列操作”主要包括________,产品在90~100℃下烘干,温度不宜太高的原因是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,科学家合成一系列具有独特化学特性的氢铝化合物(AlH3)n。已知,最简单的氢铝化合物Al2H6的球棍模型如下图所示,它的熔点为150 ℃,燃烧热极高。下列说法肯定错误的是( )

A. Al2H6在固态时所形成的晶体是分子晶体
B. Al2H6在空气中完全燃烧,产物为氧化铝和水
C. 氢铝化合物可能成为未来的储氢材料和火箭燃料
D. 氢铝化合物中可能存在组成为AlnH2n+2的一系列物质(n为正整数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列两个热化学方程式,回答下列问题:
2H2(g)+O2(g)![]() 2H2O(1) ΔH=571.6 kJ · mol1
2H2O(1) ΔH=571.6 kJ · mol1
C3H8(g)+5O2(g)![]() 3CO2(g)+4H2O(l) ΔH=2 220 kJ · mol1
3CO2(g)+4H2O(l) ΔH=2 220 kJ · mol1
(1)H2的燃烧热为_______,C3H8的燃烧热为_______。
(2)1 mol H2和2 mol C3H8组成的混合气体完全燃烧释放的热量为______________。
(3)现有H2和C3H8的混合气体共5 mol,完全燃烧时放热3 847 kJ,则在混合气体中H2和C3H8的体积比是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇的结构简式为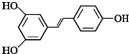 。根据要求回答下列问题:
。根据要求回答下列问题:
(1)白藜芦醇的分子式为 _______________
(2)所含官能团的名称为____________
(3)下列关于白藜芦醇的分类判断正确的是_________
A.它属于链状烯烃 B.它属于脂环化合物
C.它属于芳香化合物 D.它属于烃的衍生物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com