
COCl2(g)CO(g)+Cl2(g) ΔH>0。当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A.①②④ B.①④⑥
C.②③⑥ D.③⑤⑥
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
太阳能的开发和利用已成为最引人注目的研究课题之一,下面是科学家研究的一种利用太阳能制取H2的方法。
(1)首先利用太阳能加热氧化锌和木炭的混合物,当温度达到1 200 ℃时,可得到高纯度的锌粉,然后将得到的高纯度锌与400 ℃以上的水蒸气反应,得到H2、ZnO(循环使用),请写出反应的化学方程式:_____________________,____________________________。
(2)若投入40.5 kg氧化锌,则理论上制得的H2的体积是多少升?(标准状况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质全部是弱电解质的是( )
A.H2O、NH3·H2O、H3PO4、HF
B.Cu(OH)2、CH3COOH、C2H5OH、CH3COONa
C.H2SO3、Ba(OH)2、BaSO4
D.H2SiO3、H2S、CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
对于常温下的0.1 mol·L-1的NH4Cl溶液,请填空:
(1)溶液的pH________7(填“>”、“<”或“=”)。
(2)各类离子,其浓度由大到小的排列顺序是______________。
(3)存在的电荷守恒关系为____________________________。
(4)c(NH )+c(NH3·H2O)=________(填数字或离子浓度均可)。
)+c(NH3·H2O)=________(填数字或离子浓度均可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在密闭容器中能表示反应X(g)+2Y(g)2Z(g)一定达到平衡状态的是( )
①X、Y、Z的物质的量之比为1:2:2 ②X、Y、Z的浓度不再发生变化 ③容器中的压强不再发生变化 ④单位时间内生成n mol Z,同时生成2n mol Y
A.①② B.①④
C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
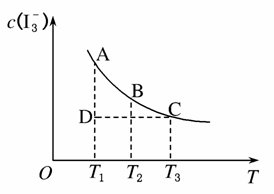
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)I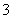 (aq),某I2、KI混合溶液中I
(aq),某I2、KI混合溶液中I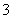 的物质的量浓度c(I
的物质的量浓度c(I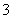 )与温度T的关系如图所示,(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
)与温度T的关系如图所示,(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
A.反应:I2(aq)+I-(aq)I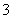 (aq)的ΔH>0
(aq)的ΔH>0
B.若温度为T1、T2,反应平衡常数分别为K1、K2,则K1<K2
C.若反应进行到状态D时,一定有ν正>ν逆
D.状态A与状态B比较,状态A的c(I2)大
查看答案和解析>>
科目:高中化学 来源: 题型:
在450 ℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:

2SO2(g)+O2(g)2SO3(g) ΔH=-190 kJ·mol-1
(1)该反应500 ℃时的平衡常数________450 ℃时的平衡常数(填“>”、“<”或“=”)。
(2)450 ℃时,在一2 L密闭容器中,将二氧化硫和氧化混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是________________。
(3)据图判断,反应进行至20 min时,曲线发生变化的原因是__________________(用文字表达),10 min到15 min的曲线变化的原因可能是________(填字母)。
A.加了催化剂
B.缩小容器体积
C.降低温度
D.增加SO3物质的量
(4)欲提高SO2的转化率,下列措施可行的是________。(填字母)
a.向装置中再充入N2
b.向装置中再充入O2
c.改变反应的催化剂
d.升高温度
(5)利用图中数据计算450 ℃时反应进行至15 min时,SO2的平衡转化率为:________。
(6)450 ℃时,另一2 L容积不变的密闭容器中,测得某时刻各物质的量如下:
n(SO2)=0.4 mol,n(O2)=0.2 mol,n(SO3)=0.8 mol,则此时该反应向________进行(填“正反应方向”“逆反应方向”或“处于平衡状态”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于如图所示装置的说法,正确的是( )
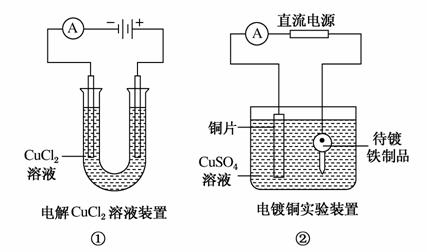

A.①装置中阴极处产生的气体能够使湿润KI淀粉试纸变蓝
B.②装置中待镀铁制品应与电源正极相连
C.③装置中电子由b极流向a极
D.④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对各组物质性质的比较中,正确的是 ( )。
A.熔点:Li<Na<K
B.导电性:Ag>Cu>Al>Fe
C.密度:Na>Mg>Al
D.空间利用率:体心立方堆积<六方最密堆积<面心立方最密堆积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com