
【题目】金属及其化合物在科学研究和工业生产中具有重要的用途。
(1)三氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:
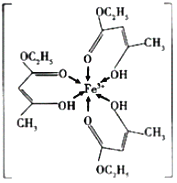
①此配合物中,铁离子价电子排布图为_______________;
②此配离子中碳原子的杂化轨道类型为_________________;
③此配离子中含有的化学键为_______________。
A 离子键 B 金属键 C 极性键 D 非极性键 E 配位键 F 氢键 G σ键 H π键
(2)NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。NO2-离子的VSEPR模型名称为_____,K3[Co(NO2)6]是黄色沉淀,该物质中四种元素的电负性由大到小的顺序是_________。
(3)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2,其中适合作录音带磁粉原料的是_____。
(4)锰的一种配合物的化学式为Mn(BH4)2(THF)3,写出两种与BH4-互为等电子体的微粒____(请写一个分子和一个离子)。
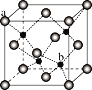
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶体的结构如图所示,a的配位数为_____,已知晶胞密度为ρ g/cm3,则晶包的棱长为_____nm(NA表示阿伏伽德罗常数)。
【答案】![]() sp2、sp3 C D E G H 平面三角形 O>N>Co>K CrO2 CH4(SiH4)、NH4+ 4 (388/ρNA)1/3 ×107nm
sp2、sp3 C D E G H 平面三角形 O>N>Co>K CrO2 CH4(SiH4)、NH4+ 4 (388/ρNA)1/3 ×107nm
【解析】
(1)①铁的原子序数为26,基态铁原子核外电子数为26,基态铁原子的核外电子排布式为[Ar]3d54s2,则Fe3+的核外电子排布式为[Ar]3d5,Fe3+的价电子排布图为![]() ,故答案为:
,故答案为:![]() 。
。
②此配离子中-C2H5和-CH3中碳原子为sp3杂化,“C=O”和“C=C”中碳原子为sp2杂化,此配离子中碳原子的杂化轨道类型为sp2、sp3,故答案为:sp2、sp3。
③根据配离子的结构可知,乙酰乙酸乙酯中碳碳之间存在非极性键,碳氢、碳氧、氧氢之间存在极性键,单键中只有σ键,碳碳双键和碳氧双键存在σ键和π键,Fe3+与乙酰乙酸乙酯之间存在配位键,此配离子中含有的化学键为极性键、非极性键、配位键、σ键、π键,故答案为:C D E G H。
(2)NO2-中中心原子N的孤电子对数为![]() ×(5+1-2×2)=1,成键电子对数为2,价层电子对数为1+2=3,NO2-的VSEPR模型为平面三角形,元素的非金属性越强,电负性越大,元素的金属性越强电负性越小,则四种元素的电负性由大到小的顺序为O>N>Co>K,故答案为:平面三角形,O>N>Co>K。
×(5+1-2×2)=1,成键电子对数为2,价层电子对数为1+2=3,NO2-的VSEPR模型为平面三角形,元素的非金属性越强,电负性越大,元素的金属性越强电负性越小,则四种元素的电负性由大到小的顺序为O>N>Co>K,故答案为:平面三角形,O>N>Co>K。
(3)V2O5中阳离子为V5+,V5+的核外电子排布式为1s22s22p63s23p6,没有未成对电子;CrO2中阳离子为Cr4+,Cr4+的核外电子排布式为:1s22s22p63s23p63d2,3d上有2个未成对电子,根据“金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好”,磁性最大的是CrO2,所以适合作录音带磁粉原料的是CrO2,故答案为:CrO2。
(4)用替换法,与BH4-互为等电子体的的分子是CH4、SiH4,离子为NH4+等,故答案为:CH4(SiH4)、NH4+。
(5)由晶胞可知b的配位数为4,该晶体的化学式为ZnS,则a的配位数也为4,用“均摊法”,晶胞中含a:8×![]() +6×
+6×![]() =4,含b:4,设晶胞的边长为x,则晶胞的体积为x3,1mol晶体的体积为
=4,含b:4,设晶胞的边长为x,则晶胞的体积为x3,1mol晶体的体积为![]() ,1mol晶体的质量为(32+65)g=97g,则1mol晶体的体积为
,1mol晶体的质量为(32+65)g=97g,则1mol晶体的体积为![]() ,
,
![]() =
=![]() ,解得x=
,解得x=![]() cm=
cm=![]() nm,故答案为:4,
nm,故答案为:4,![]() 。
。


科目:高中化学 来源: 题型:
【题目】已知:CH3—CH=CH2+HBr→CH3—CHBr—CH3(注意溴原子的连接位置,下同),1 mol某芳香烃A充分燃烧后可以得到9 mol CO2和5 mol H2O,该烃苯环上的一氯代物有2种。该烃A在不同条件下能发生如下所示的一系列变化。

请回答下列问题
(1)写出A的结构简式:__________,A中官能团的名称是________。
(2)上述反应中,②是________反应,⑦是________反应。(填反应类型)
(3)写出D、E物质的结构简式:D_______,E_______。
(4)写出A→C反应的化学方程式:____________________。
(5)写出F→H反应的化学方程式:________________。
(6)写出F催化氧化反应的化学方程式:___________。
(7)下列关于F的说法不正确的是______(填序号)。
a. 能发生消去反应 b. 能与金属钠反应
c. 1mol F最多能和4mol氢气反应 d. 分子式C9H11O
e. 能使酸性高锰酸钾褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠是一种食品添加剂,具有防腐和抗氧化作用。某同学对亚硝酸钠进行了相关探究。
(一)查阅资料
①亚硝酸钠(NaNO2)为无色、无味的晶体。
②HNO2是一种弱酸,酸性比醋酸略强,性质不稳定,易分解生成NO和NO2;能被常见强氧化剂氧化;但在酸性溶液中它也是一种氧化剂,如能把I-氧化成I2。
③AgNO2是一种微溶于水、易溶于酸的浅黄色固体。
(二)问题讨论
(1)人体正常的血红蛋白中应含Fe2+,误食亚硝酸盐(如NaNO2)会致使机体组织缺氧,出现青紫而中毒,原因是__________________________________________。
若发生中毒时,你认为下列物质有助于解毒的是______(填字母)。
a.鸡蛋清 b.胃舒平 [主要成分是Al(OH)3] c.小苏打 d.维生素C
(2)由于亚硝酸钠和食盐性状相似,曾多次发生过将NaNO2误当食盐食用的事件。要区别NaNO2和NaCl两种固体,你需用的试剂是_____________________________。
(三)实验测定
为了测定某样品中NaNO2的含量,某同学进行如下实验:①称取样品a g,加水溶解,配制成100 mL溶液。②取25.00 mL溶液于锥形瓶中,用0.0200mol·L-1 KMnO4标准溶液(酸性)进行滴定,滴定结束后消耗KMnO4溶液 V mL。
(3)上述实验①所需玻璃仪器除玻璃棒、胶头滴管之外还有________________。
(4)在进行滴定操作时,KMnO4溶液盛装在________(填“酸式”或“碱式”)滴定管中。当滴入最后一滴溶液,____________________________________________________时达到滴定终点。
(5)滴定过程中发生反应的离子方程式是_________________________________;测得该样品中NaNO2的质量分数为________。
(6)若滴定过程中刚出现颜色变化就停止滴定,则测定结果________。(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜―→铜绿―→……―→铜”的转化。
铜![]() 铜绿
铜绿![]() A
A![]() Cu(OH)2
Cu(OH)2![]() B
B![]() Cu
Cu
(1)从物质分类标准看,“铜绿”属于________(填字母)。
A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式:________________。
(3)请写出铜绿与盐酸反应的化学方程式:__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工厂排放的SO2烟气对环境造成污染,某企业用下图流程综合处理,下列有关说法正确的是

A. 二氧化硫吸收塔中发生的反应为SO2+SO32-+H2O=2HSO3-
B. 氨气吸收塔中发生的反应为HSO3-+OH-=H2O+SO32-
C. 上述流程利用的是氧化还原反应原理
D. 上述流程可循环利用的物质有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中Mg2+、NH4+、Al3+三种离子的物质的量之比为( )
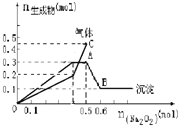
A. 1∶1∶2B. 2∶2∶1
C. 1∶2∶2D. 9∶2∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现将下列物质分别装入有水的锥形瓶里(见下图),立即塞紧带 U 形管的塞子, 发现 U 形管内滴有红墨水的水面如图所示状态,判断加入的物质不可能是( )
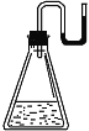
A.NaOH 固体B.浓硫酸C.![]() 晶体D.CaO固体
晶体D.CaO固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,22.4 L CCl4中含CCl4分子数为NA
B. 5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等
C. 0.1 mo1·L-1 MgCl2溶液中含Cl-数为0.2NA
D. 3.9 g Na2O2 晶体中含有的离子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的有机产物,肯定是一种的是( )
A. 异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B. 2—氯丁烷(![]() )与NaOH溶液共热发生反应
)与NaOH溶液共热发生反应
C. 甲苯在一定条件下发生硝化生成一硝基甲苯的反应
D. 等物质的量的甲烷和氯气的混和气体长时间光照后的产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com