
分析 X、Y、Z、Q、R、T分别代表原子序数依次增大的短周期元素.X、Y、Z同周期且相邻,都是蛋白质的组成元素,则X为C、Y为N、Z为O;X、T同族,则T为Si;Q与R原子的最外层电子数之和与T原子的最外层电子数相等,则Q、R原子最外层电子数之和为4,二者原子序数大于氧、小于Si,可推知Q为Na、R为Al;U是d区元素,U2+的核外最高能级有2对成对电子,原子外围电子排布为3d74s2,故U为Co,据此解答.
解答 解:X、Y、Z、Q、R、T分别代表原子序数依次增大的短周期元素.X、Y、Z同周期且相邻,都是蛋白质的组成元素,则X为C、Y为N、Z为O;X、T同族,则T为Si;Q与R原子的最外层电子数之和与T原子的最外层电子数相等,则Q、R原子最外层电子数之和为4,二者原子序数大于氧、小于Si,可推知Q为Na、R为Al;U是d区元素,U2+的核外最高能级有2对成对电子,原子外围电子排布为3d74s2,故U为Co.
(1)Q为Na,原子的核外电子排布式为1s22s22p63s1,故答案为:1s22s22p63s1;
(2)CO2分子结构式为O=C=O,双键中含有1个σ键、1个π键,故分子中σ键与π键数目之比为1:1,NO2-离子中N原子价层电子对数为2+$\frac{5+1-2×2}{2}$=3,VSEPR模型为平面三角形,
故大拿为:1:1;平面三角形;
(3)Si单质为原子晶体,Al、Na单质为金属晶体,Si单质熔点最高,由于铝离子半径小于钠离子半径,铝离子所带电荷更多,故金属铝中金属键更强,则Al的熔点高于钠的,故熔点由高到低的顺序是:Si>Al>Na,既能与强酸反应,又能与强碱反应的是Al,
故答案为:Si>Al>Na;Al;
(4)通常情况下,Co2+的溶液很稳定,它与NH3形成的配位数为6的配离子却不稳定,在空气中易被氧化为[Co(NH3)6]3+,该反应的离子方程式是:4[Co(NH3)6]2++O2+2H2O═4[Co(NH3)6]3++4OH-,
故答案为:4[Co(NH3)6]2++O2+2H2O═4[Co(NH3)6]3++4OH-.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、化学键、价层电子对互斥理论、晶体类型与性质、配合物等,推断元素是解题关键,注意对基础知识的理解掌握.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
| t/min | 0 | 20 | 40 | 60 | 80 |
| c(H2O2)/mol•L-1 | 1.0 | 0.60 | 0.40 | 0.20 | 0.10 |
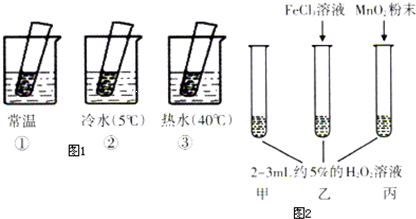
| 现象 | 结论 | |
| 热水中 | 溶液中有气泡产生,比常温快 | 升高温度,H2O2的分解速率加快 |
| 常温中 | 溶液中有气泡产生,且速度较快 | 无 |
| 冷水中 | 溶液中有气泡产生,比常温慢 | 降低温度,H2O2的分解速率减慢 |
| 现象 | 结论 | |
| 丙加入MnO2 | MnO2能加快化学反应速率 | |
| 乙加入FeCl3 | FeCl3能加快化学反应速率 | |
| 甲不加其他试剂 | 溶液中有少量气泡出现 | 不使用催化剂化学反应速率较小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,A在一定条件下能与水反应,可用于饮用水的消毒,试写出此反应的化学反应方程式NCl3+3H2O=NH3+3HClO.
,A在一定条件下能与水反应,可用于饮用水的消毒,试写出此反应的化学反应方程式NCl3+3H2O=NH3+3HClO.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LH2O含有的分子数为1 NA | |
| B. | 常温常压下,1molNa2CO3含有的Na+离子数为2 NA | |
| C. | 通常状况下,1 NA 个CO2分子占有的体积为22.4L | |
| D. | 1mol/L的MgCl2溶液中,含有Cl- 个数为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在饱和氯水中:Cl-、NO3-、Na+、SO32- | |
| B. | 0.1mol/L NaAlO2溶液中:K+、CO32-、SO42-、Cl- | |
| C. | 在强碱性溶液中:Na+、NH4+、SO32-、Cl- | |
| D. | 1.0mol•L-1的盐酸溶液中:K+、Fe2+、ClO-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶液的pH | 加入盐酸的总体积 |
| 12 | V(HCl)=0 |
| 8 | V(HCl)=20.00mL |
| 5 | V(HCl)=40.00mL |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NH4+,NO3-,CO32-,Na+ | B. | Na+,Ba2+,Mg2+,HCO3- | ||
| C. | NO3-,Ca2+,K+,H+ | D. | NO3-,K+,AlO2-,OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com