
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.硫酸中放出氢气量最多? |
| B.醋酸中放出氢气量最多? |
| C.盐酸中放出的氢气量最多? |
| D.硝酸中放出的氢气量最多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.②③ | C.③④ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.弱电解质的相对强弱可由相同温度下的电离常数值的大小来判断 |
| B.同一弱电解质,浓度越大,电离程度越大 |
| C.升高温度,弱电解质的电离程度减小 |
| D.通常,电解质越弱,则其溶液的导电能力就越差 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.柠檬酸分子 | B.柠檬酸根 | C.H+ | D.OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| c(OH-) |
| c(NH3?H2O) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.④③②① | B.①②③④ | C.③②④① | D.③④②① |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.有化学键断裂的过程一定发生化学变化 |
| B.氯化钠是一种电解质,电解饱和食盐水可制得金属钠 |
| C.将pH=a的醋酸稀释为pH=a + 1的过程中,c(CH3COOH) / c(H+)减小 |
| D.SiO2是酸性氧化物,能与强碱溶液反应,但不与任何酸反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.往乙酸中通入氨气 |
B.往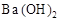 溶液中滴加硫酸 溶液中滴加硫酸 |
| C.往氢硫酸溶液中通入氯气 |
| D.往NaOH溶液中通入过量CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com