
已知NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.7.2 g CaO2晶体中阴离子和阳离子总数为0.3 NA
B.在标况下,22.4LHF和22.4LC2H4原子个数比为1:3
C.将1 mol NH4NO3溶于稀氨水中使溶液呈中性,溶液中NH4+数目为NA
D.0.1 mol H2O2分子中含极性共价键数目为0.3 NA
科目:高中化学 来源: 题型:解答题

| t/s | 0 | 10 | 20 | 30 | 40 |
| n(SO3)/mol | 0 | 0.6 | 1.0 | 1.2 | 1.2 |
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古高三上月考二化学试卷(解析版) 题型:选择题
根据有机化合物的命名原则,下列命名正确的是
A. 3﹣甲基﹣1,3﹣丁二烯
3﹣甲基﹣1,3﹣丁二烯
B. 2﹣羟基丁烷
2﹣羟基丁烷
C.CH3CH(C2H5)CH2CH2CH3 2﹣乙基戊烷
D.CH3CH(NH2)CH2COOH 3﹣氨基丁酸
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理:

下列说法正确的是( )
A.V=44.8
B.原样品中Fe元素的质量分数为38.89%
C.滤液A中的阳离子为Fe 2+、Fe3+、H+
2+、Fe3+、H+
D.样品中CuO的质量为4.0 g
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
O2F2可以发生反应:H2S+4O2F2→SF6+2HF+4O2,下列说法正确的是( )
A.还原剂与氧化剂的物质的量之比为1:4
B.氧气是氧化产物
C.若生成4.48 L HF,则转移0.8 mol电子
D.O2F2既是氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟二化学试卷(解析版) 题型:实验题
实验室用如图所示装置制备KClO溶液,再与KOH、Fe(NO3)3溶液反应制备高效净水剂K2FeO4.
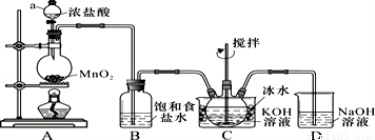
已知:K2FeO4易溶于水、微溶于浓KOH溶液,在0℃~5℃的强碱性溶液中较稳定.
【制备KClO及K2FeO4】
(1)装置C中三颈瓶置于冰水浴中的目的是 .
(2)C中得到足量KClO后将三颈瓶上的导管取下,依次加入KOH溶液、Fe(NO3)3溶液,水浴控制反应温度 为25℃,搅拌1.5 h,溶液变为紫红色(含K2FeO4),该反应的离子方程式为 .再加入饱和KOH溶液,析出紫黑色晶体,过滤,得到K2FeO4粗产品.
为25℃,搅拌1.5 h,溶液变为紫红色(含K2FeO4),该反应的离子方程式为 .再加入饱和KOH溶液,析出紫黑色晶体,过滤,得到K2FeO4粗产品.
(3)K2FeO4粗产品含有Fe(OH)3、KCl等杂质,其提纯步骤为:
①将一定量的K2FeO4粗产品溶于冷的3 mol/L KOH溶液中,
② ,
③ ,
④搅拌、静置、过滤,用乙醇洗涤2~3次,用乙醇洗涤的理由_____________ .
⑤在真空干燥箱中干燥.
【测定产品纯度】
(4)称取提纯后的K2FeO4样品0.2100 g于烧杯中,加入强碱性亚铬酸盐溶液,发生的反应为:Cr(OH)4﹣+FeO42﹣═Fe(OH)3↓+CrO42﹣+OH﹣;过滤后再加稀硫酸调节溶液呈强酸性,此时反应的离子方程式为: .
(5)将(4)反应后的溶液配成250 mL溶液,取出25.00 mL放入锥形瓶,用0.01000 mol/L的(NH4)2Fe(SO4)2溶液滴定至终点,重复操作2次,平均消耗(NH4)2Fe(SO4)2溶液30.00 mL.滴定时发生的离子反应为: .计算该K2FeO4样品的纯度为 .
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟二化学试卷(解析版) 题型:选择题
下表中物质甲物质一定条件下与乙组中的4种物质都能发生反应的是( )
选项 | 甲物质 | 乙组中的物质 |
A | SO2 | 淀粉碘化钾溶液、氨水、KMnO4溶液、碳酸钠溶液 |
B | Mg | Cl2、CO2、NH4Cl溶液、NaOH溶液 |
C | SiO2 | 碳、NaOH溶液、氢氟酸、Na2CO3 |
D | 稀硫酸 | Al(OH)3、碳、Cu2(OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应 | |
| B. | 乙烯、聚氯乙烯、苯乙烯分子结构中都含有不饱和键 | |
| C. | 乙醇既可以作燃料,也可以在日常生活中使用,如无水乙醇可用于杀菌、消毒 | |
| D. | 淀粉、油脂、蛋白质都属于纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高反应体系的温度 | B. | 增加锌粒的用量 | ||
| C. | 不用锌粒,改用锌粉 | D. | 滴入少量硫酸铜溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com