


科目:高中化学 来源:不详 题型:单选题
| A.推销商做实验时,用铁棒作阳极 |
| B.电解纯净水和自来水时的现象不同是因为纯净水和自来水所含电解质溶液浓度不同 |
| C.铝棒电极发生的电极反应为Al-3e-===Al3+ |
| D.电解自来水时出现“红褐色或灰绿色的絮状物”是因为产生了铁的氢氧化物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 甲 | 乙 | 丙 | 丁 |
| A | Pt | Pt | CuCl2 | HCl气体 |
| B | C | Cu | CuSO4 | CuO固体 |
| C | Pt | C | H2SO4 | H2SO4(纯) |
| D | Fe | Fe | NaCl | NaOH固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A. 6.72L | B. 8.96L | C.11.2L | D.5.6L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.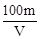 | B.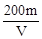 | C.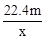 | D.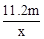 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
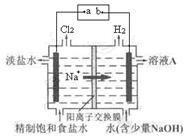
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


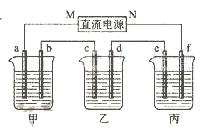
 (1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。
(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。 ①电源的N端为 极;
①电源的N端为 极; ②电极b上发生的电极反应为 ;
②电极b上发生的电极反应为 ; ③电极b上生成的气体在标准状况下的体积:
③电极b上生成的气体在标准状况下的体积:
 ④电极c的质量变化是 g;
④电极c的质量变化是 g; (2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?  。
。 ⑤电解前后各溶液的pH如何变化。(填增大,减小或不变)
⑤电解前后各溶液的pH如何变化。(填增大,减小或不变) 甲溶液 ;
甲溶液 ; 乙溶液_______;
乙溶液_______; 丙溶液_______;
丙溶液_______;查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaOH溶液 | B.CuSO4溶液 | C.Na2SO4溶液 | D.NaCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com