
常温下,向l00mL 0.01 mol?L-1 盐酸中逐滴加入0.02 mol?L-1 MOH溶液,如下图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是( )
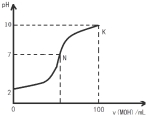
A.MOH是弱碱
B.N点c(Cl-) = c(M+)
C.随着MOH溶液的滴加,比值 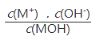 不变
不变
D.K点对应的溶液c(MOH)+c(OH-)-c(H+) = 0.005 mol?L-1
D
【解析】
试题分析:A. 若MOH为强碱,则在恰好完全中和前后溶液的pH应该有一个很大的突越。,但是该图的pH在恰好中和时变化不明显。因此MOH为弱碱。正确。B.根据电荷守恒可得c(Cl-)+c(OH-) = c(H+)+c(M+),而在N点的溶液中c(OH-) = c(H+),所以N点c(Cl-) = c(M+)。正确。C.随着MOH溶液的滴加,c(M+)、c(OH-)不断增大,在恰好完全中和前, c(MOH)逐渐减小,因此c(M+)·c(OH-)/ c(MOH)比值逐渐增大。错误。D.在K点根据电荷守恒可得c(H+)+c(M+)=c(OH-)+c(Cl-);根据物料守恒可得c(M+)+ c(MOH) =0.01 mol/L;c(Cl-)=0.005mol/L,所以c(M+)=c(OH-)+c(Cl-)- c(H+),c(M+)+ c(MOH)= c(OH-)+c(Cl-)- c(H+)+ c(MOH),c(MOH)+c(OH-)-c(H+) = 0.01mol/L-0.005mol/L=0.005mol/L。正确。
考点:考查酸碱中和反应中离子浓度的大小比较、物质的强弱的判断及离子浓度的关系的知识。


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源:2013-2014辽宁省大连市高三双基测试化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A. 硫酸铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓
B.向明矾溶液中滴加Ba(OH)2溶液至Al3+ 刚好沉淀完全:2Al3+ + 3SO42- + 3Ba2+ + 6OH- = 3BaSO4↓ + 2Al(OH)3↓
C.NH4HCO3溶于过量的NaOH溶液中:HCO3?+OH?=CO32?+H2O
D.稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑
查看答案和解析>>
科目:高中化学 来源:2013-2014辽宁省五校第二学期期末联考高一化学试卷(解析版) 题型:选择题
下列说法中正确的一组是
A.H2和D2互为同素异形体;
B. 和
和 互为同分异构体;
互为同分异构体;
C.正丁烷和异丁烷是同系物;
D. 和
和 是同一种物质
是同一种物质
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高三高考模拟理综化学试卷(解析版) 题型:简答题
雾霾天气严重影响人们的生活质量,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一。消除氮氧化物和硫氧化物有多种方法。
(1)氮、氧元素非金属性较强的是 。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:
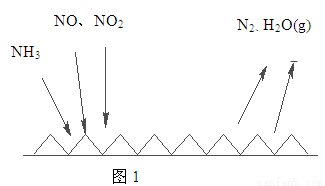
①由图1可知SCR技术中的氧化剂为 。
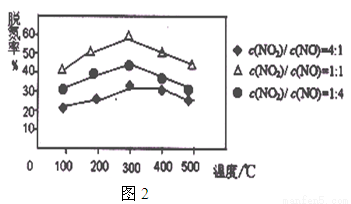
②用Fe做催化剂时,在氨气足量的情况下,不同c(NO2)/c(NO)对应的脱氮率如图2所示,脱氮效果最佳的c(NO2)/c(NO)= 。当NO2与NO的物质的量之比为1:1时,用氨脱氮,每生成1molN2放出的热量为QkJ,写出该反应的热化学方程式 。
(3)海水具有良好的吸收SO2的能力,其吸收过程如下:
①SO2溶于海水生成H2SO3,H2SO3最终会电离出SO32-,SO32-可以被海水中的溶解氧氧化为SO42-。海水的pH会 (填“升高” 、“不变”或“降低”)。
②SO2和O2在H2SO4溶液中可以构成原电池,其负极反应式是 。
(4)碲(Te)为ⅥA族元素,是当今高新技术新材料的主要成分之一。工业上可将SO2通入TeCl4的酸性溶液中进行“还原”得到碲,该反应的化学方程式是_________ 。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:推断题
(13分)(1).PET是应用广泛的五大工程塑料之一,PET结构片段:
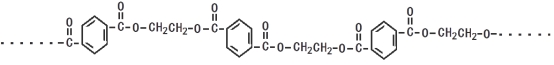
①PET由两种有机物通过缩聚反应生成,其中分子较大的单体分子结构简式为 ,分子较小的单体含氧官能团名称是 。
②PET塑料有多种降解途径,其中常用的甲醇法是在一定条件下将其与过量的甲醇作用,降解为两种小分子。该反应的化学方程式为: 。
(2).水杨酸(邻羟基苯甲酸)是合成阿司匹林(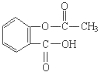 )的原料。
)的原料。
①水杨酸与乙酸酐(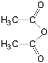 )反应生成阿司匹林的化学方程式: 。
)反应生成阿司匹林的化学方程式: 。
②写出一种阿司匹林同分异构体的结构式 ,该同分异构体符合以下条件:
a.芳香族化合物;
b.与氢氧化钠溶液共热,完全反应将消耗四倍物质的量的氢氧化钠;
c.苯环上氢原子被一个溴原子取代,可能的产物有两种。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:选择题
在25℃、1×105Pa时,等质量的H2、Cl2、CO2、C2H2四种气体中( )
A. H2分子数最大 B. C2H2原子数最大
C. CO2密度最大 D. Cl2分子间平均距离最大
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:选择题
短周期元素X、Y、W、Q在元素周期表中的相对位置如下图所示。Y是地壳中含量最多的元素。下列说法正确的是( )
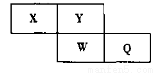
A.1mol Q单质与氢氧化钠溶液反应转移的电子数目为2 NA
B.X的气态氢化物能使湿润的蓝色石蕊试纸变红
C.氢化物的沸点:H2Y>HQ
D.最髙价氧化物的水化物的酸性:W > Q
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如下表:
元素代号 | X | Y | Z | W |
原子半径/pm | 160 | 143 | 70 | 66 |
主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
下列叙述正确的是( )
A.X、Y元素的金属性 X<Y
B.一定条件下,Z单质与W的常见单质化合生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高三5月校质检理综化学试卷(解析版) 题型:选择题
海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示。下列说法错误的是( )
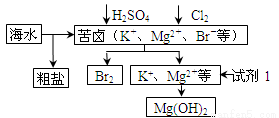
A.试剂1可以选用石灰乳
B.从苦卤中提取Br2的反应的离子方程式为:2Br - + Cl2=2Cl- + Br2
C.工业上,电解熔融MgO冶炼金属镁可减小能耗
D.可用BaCl2溶液除去粗盐中的SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com