
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则( )

A.M点所示溶液导电能力强于Q点
B.N点所示溶液中c(CH3COO-)>c(Na+)
C.M点和N点所示溶液中水的电离程度相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
科目:高中化学 来源: 题型:
 某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则( )
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则( )| A、M点所示溶液导电能力强于Q点 | B、N点所示溶液中c(CH3COO-)>c(Na+) | C、M点和N点所示溶液中水的电离程度相同 | D、Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
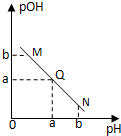 某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH( pOH=-lgc(OH-))与pH的变化关系如图所示,则( )
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH( pOH=-lgc(OH-))与pH的变化关系如图所示,则( )| A、N点所示溶液中c(H+)<c(OH-) | B、M点所示溶液导电能力强于Q点 | C、M点水的电离程度大于N点 | D、Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中
pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则
A.M点所示溶液导电能力强于Q点
B.N点所示溶液中c(CH3COO-)﹥c(Na+)
C.M点和N点所示溶液中水的电离程度相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积

查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省临沂市高三3月教学质量检测(一模)化学试卷(解析版) 题型:选择题
某温度下,向一定体积0.1 mol/L的氨水中逐滴滴加0.1mol/L的盐酸,溶液中pH与pOH[注:pOH=-lgc(OH-)]的变化关系如图所示,则下列说法中错误的是

A.M点所示溶液中c( NH4+)>c(Cl-)
B.Q点所示溶液的导电熊力强于M点
C.Q点消耗盐酸的体积等于氨水的体积
D.M点和N点所示溶液中水的电离程度相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com