
食盐(NaCl)是生活中常用的调味品,HCl是胃酸的主要成分,下列关于两种物质的说法正确的是
( )。
A.炒菜时放入食盐并不破坏NaCl中的化学键
B.HCl的电子式是H+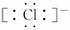
C.NaCl熔化时破坏共价键
D.HCl的结构式是H—Cl
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
常见元素A、B、M组成的四种物质发生反应:甲+乙 丙+丁,其中甲由A和M组成,乙由B和M组成,丙只含M。
(1)若甲为淡黄色固体,乙和丙均为常温下的无色无味气体。则甲的电子式为 ;生成标准状况下5.6L丙转移移电子数为 ;常温下丁溶液pH 7,用离子方程式解释 。
(2)若丁为能使品红褪色的无色气体,丙为常见紫红色金属,化合物甲、乙中原子个数比均为1:2(M均显+1价),原子序数B大于A。则:
①A在周期表中位置为
②将丁通至FeCl3溶液中的现象为
离子反应方程式为
③正确书写上述生成丙的化学方程式
④向MCl2的溶液中通入丁,可观察到白色的MC1沉淀,写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程如图(写出最佳答案)。
(1)沉淀的化学式:沉淀1____________________,沉淀2__________________,沉淀3________________;
(2)写出混合液+A的离子方程式:__________________________________________
________________________________________________________________________;
溶液1+B的离子方程式:_______________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是( )
A.氢氧化钠与盐酸;氢氧化钠与碳酸
B.BaCl2溶液与Na2SO4溶液;Ba(OH)2溶液与H2SO4溶液
C.Na2CO3溶液与硝酸溶液;NaHCO3溶液与硝酸溶液
D.石灰石与硝酸;石灰石与盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
现用98%的浓H2SO4(ρ=1.84 g·cm-3)配制浓度为0.5 mol·L-1的稀硫酸500 mL。
(1)选用的玻璃仪器除烧杯、玻璃棒外,还需__________________________。
(2)请将下列操作按正确的顺序把序号填写在横线上
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加水至刻度线
D.洗涤所用仪器
E.稀释浓H2SO4
F.将溶液转入容量瓶
其操作的正确顺序为_____________________________________________________。
(3)简要回答下列问题:
①所需浓H2SO4的体积为______ mL。
②如果实验室有15 mL、20 mL、25mL的量筒,选用______ mL的量筒最好。量取时发现量筒不干净,用水洗净后直接量取将使实验最终结果______(填“偏高”、“偏低”或“无影响”)。
③在转入容量瓶前烧杯中液体应________________,否则会使浓度________(填“偏高”、“偏低”或“无影响”)。
④定容时必须使溶液凹液面最低处与刻度线相切,若俯视会使结果________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是同周期的五种主族元素。A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A;C和D的最高价氧化物对应的水化物均呈酸性,且酸性C>D,E是这五种元素中原子半径最小的元素,它们的原子序数由小到大的顺序是
( )。
A.A<B<C<D<E B.C<D<A<B<E
C.B<A<D<C<E D.E<C<D<B<A
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家发现:具有2、8、20、28、50、82、114、126等数目的质子或中子的原子核具有特别的稳定性,并将这些偶数称为“幻数”,而具有双幻数的He、Ni、Sn、Pb等尤为稳定。根据此信息回答下列问题:
(1)写出前三种质子数为“幻数”的元素原子的结构示意图,并标明元素符号________________________________________________________________。
(2)已知氧有三种同位素O、O、O,根据上述“幻数”规律,氧的同位素中原子核最稳定的是________。
(3)根据现有元素周期律推算,R位于元素周期表的第________周期第________族,核稳定性R__________R(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关聚乙烯的说法正确的是
( )。
A.聚乙烯是通过加聚反应生成的
B.聚乙烯具有固定的元素组成,因而具有固定的熔、沸点
C.聚乙烯塑料袋因有毒,故不能装食品
D.聚乙烯因性质稳定,故不易造成污染
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,反应2SO2(g)+O2(g)  2SO3(g),达到平衡时,n(SO2)∶n(O2)∶n(SO3)=2∶3∶4。缩小体积,反应再次达到平衡时,n(O2)=0.8 mol,n(SO3)=1.4 mol,此时SO2的物质的量应是
2SO3(g),达到平衡时,n(SO2)∶n(O2)∶n(SO3)=2∶3∶4。缩小体积,反应再次达到平衡时,n(O2)=0.8 mol,n(SO3)=1.4 mol,此时SO2的物质的量应是
( )。
A.0.4 mol B.0.6 mol C.0.8 mol D.1.2 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com