
| A. | 此时溶液中NH3•H2O的物质的量浓度为$\frac{a-0.01}{2}$+10-10-10-4mol/L | |
| B. | 溶液中c(NH4+)=c(Cl-) | |
| C. | 此时水的电离程度最大 | |
| D. | 25℃时NH3•H2O的电离平衡常数Kb=$\frac{{{{10}^{-9}}}}{a-0.01}$(mol/L) |
分析 A.溶液中(Cl-)=0.005mol/L,c(H+)=10-10mol/L,c(OH-)=10-4mol/L,结合电荷守恒分析;
B.根据电荷守恒分析;
C.溶液中铵根离子浓度最大时,水的电离程度最大;
D.根据Kb=$\frac{c(N{{H}_{4}}^{+})×c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$计算.
解答 解:A.溶液中(Cl-)=0.005mol/L,c(H+)=10-10mol/L,c(OH-)=10-4mol/L,已知电荷守恒c(H+)+c(NH4+)=c(Cl-)+c(OH-),则c(NH4+)=c(Cl-)+c(OH-)-c(H+)=0.005mol/L+10-4mol/L-10-10mol/L,所以c(NH3•H2O)=$\frac{a}{2}$mol/L-c(NH4+)=$\frac{a-0.01}{2}$+10-10-10-4mol/L,故A正确;
B.已知电荷守恒c(H+)+c(NH4+)=c(Cl-)+c(OH-),溶液显碱性,则c(H+)<c(OH-),所以c(NH4+)>(Cl-),故B错误;
C.a mol/L的氨水与0.01mol/L的HCl溶液等物质的量恰好反应生成氯化铵时,溶液中铵根离子浓度最大,水的电离程度最大,等体积混合溶液的pH=10,显碱性,氨水电离的氢氧根离子抑制了水的电离,水的电离程度不是最大,故C错误;
D.溶液中c(NH4+)=c(Cl-)+c(OH-)-c(H+)=0.005mol/L+10-4mol/L-10-10mol/L,c(NH3•H2O)=$\frac{a}{2}$mol/L-c(NH4+)=$\frac{a-0.01}{2}$+10-10-10-4mol/L,c(OH-)=10-4mol/L,则Kb=$\frac{c(N{{H}_{4}}^{+})×c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{1.02×1{0}^{-6}}{a-9.8×1{0}^{-3}}$,故D错误.
故选A.
点评 本题考查了酸碱混合的定性判断和定量计算,题目难度稍大,明确溶液中的电荷守恒、电离常数的计算是解答本题关键,注意把握溶液酸碱性与溶液pH的关系.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
 下列所列各组物质中,物质之间通过一部步反应不能实现如图所示转化的是( )
下列所列各组物质中,物质之间通过一部步反应不能实现如图所示转化的是( ) | 选项 | a | b | c |
| A | Al2O3 | Na[Al(OH)4] | Al(OH)3 |
| B | HNO3 | NO | NO2 |
| C | Si | SiO2 | H2SiO3 |
| D | Fe | FeCl3 | FeCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | Al和Fe2O3的铝热反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 | ||
| C. | NaOH溶液与CH3COOH溶液反应 | D. | 甲烷在O2中的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA | |
| B. | 28克由C3H6和C4H8组成的混合气体中含共用电子对数目为6NA个 | |
| C. | 0.1mol氧气作为氧化剂得到电子的数目一定为0.4NA | |
| D. | 常温下,0.1mol•L-1的碳酸钠溶液中含有的阴离子数大于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子) 、
、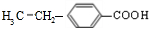 ;
;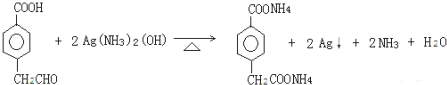 ;反应⑦的化学方程式为
;反应⑦的化学方程式为 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ,F1和F2互为同分异构体,G1和G2互为同分异构体. 请填空:
,F1和F2互为同分异构体,G1和G2互为同分异构体. 请填空:
 ,
,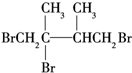 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com