
| A�� | ͨ���������CD3�����Ʊ�C���� | |
| B�� | A��B�����γ����壬�����һ��Ϊ��������ṹ | |
| C�� | C�����������������D������������ˮ���� | |
| D�� | A2B2O4��ˮ�пɵ���������Ӻ������ӣ�����A2B2O4�д������Ӽ� |
���� ������Ԫ��A��B��C��D��ԭ������֮��Ϊ37��A��������ۺ�����۴����͵���0���������Ӻ�Heԭ�Ӿ�����ͬ�ĵ����Ų�����AΪHԪ�أ�C�ǵؿ��к�����ߵĽ���Ԫ�أ���CΪAlԪ�أ�D����̬�⻯�������ۺ����ᶼ��ǿ�ᣬ��DΪClԪ�أ�B��ԭ������=37-1-13-17=6����BΪCԪ�أ��ݴ˽��Ԫ��������֪ʶ���
��� �⣺������Ԫ��A��B��C��D��ԭ������֮��Ϊ37��A��������ۺ�����۴����͵���0���������Ӻ�Heԭ�Ӿ�����ͬ�ĵ����Ų�����AΪHԪ�أ�C�ǵؿ��к�����ߵĽ���Ԫ�أ���CΪAlԪ�أ�D����̬�⻯�������ۺ����ᶼ��ǿ�ᣬ��DΪClԪ�أ�B��ԭ������=37-1-13-17=6����BΪCԪ�أ�
A��CD3ΪAlCl3���Ȼ���Ϊ���ۻ���������Ȼ��������磬������Ȼ������������A����
B��A��B�ֱ�ΪH��CԪ�أ������γɵĻ�����Ϊ��������������϶࣬��ṹ��һ��Ϊ��������ṹ������ȲΪֱ���ͽṹ����ϩΪƽ��ṹ����B����
C��C��������Ϊ��������D������������ˮ����Ϊ�����ᣬ�������ܹ����ڸ����ᣬ��C��ȷ��
D��A2B2O4ΪH2C2O4������Ϊ���ۻ���������в��������Ӽ�����D����
��ѡC��
���� ���⿼��ԭ�ӽṹ��Ԫ�������ɵĹ�ϵ����Ŀ�ѶȲ����ƶ�Ԫ��Ϊ���ؼ���ע������ԭ�ӽṹ��Ԫ�������ɡ�Ԫ�����ڱ��Ĺ�ϵ������������ѧ�������Ӧ��������


 һ����ʦȨ����ҵ��ϵ�д�
һ����ʦȨ����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
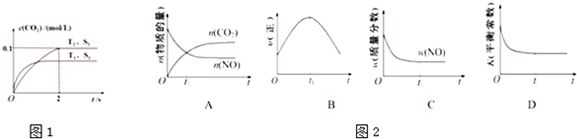
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ�� | ���� | ���� |
| A | �����ˮ������Һ�еμ�������Һ | δ���������� | ����û��ˮ�� |
| B | ��Ϸֱ�װ��Cl2��NH3�ļ���ƿ�е����� | ������������ | NH3�Ի�ԭ�Ժͼ��� |
| C | ��1.0mol•L-1��NaHA��Һ�еμ�2�μ��� | ��Һ�ʻ�ɫ | NaHA��Һ�Լ��� |
| D | ��ͬ��пƬ�ֱ���ͬ��ͬ�������c��H+��=1mol•L-1�����ᡢ���ᷴӦ | п�����ᷴӦ�������ݽϿ� | һ����Cl-�Ը÷�Ӧ�ٽ����� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
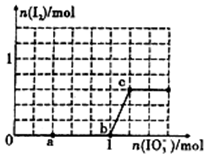 ��֪����ԭ��HSO3-��I-��������IO3-��I2���ں�3mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ������˵������ȷ���ǣ�������
��֪����ԭ��HSO3-��I-��������IO3-��I2���ں�3mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ������˵������ȷ���ǣ�������| A�� | 0-a�η�����Ӧ��3 HSO3-+IO3-�T3SO42-+I-+3H+ | |
| B�� | a��b�ι�����NaHSO3�����ʵ���Ϊ1.8mol | |
| C�� | b��c�η�Ӧ����������ΪI2 | |
| D�� | ����Һ��I-��I2�����ʵ���֮��Ϊ5��1ʱ�������KIO3Ϊ1��lmol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ѧ��Ӧ���ʺ���������������������أ�
��ѧ��Ӧ���ʺ���������������������أ�| ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
| ���������mL������״���� | 100 | 240 | 464 | 576 | 620 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
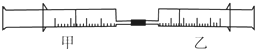 ��ͼ��ʾ�����ס�������װ�в�ͬ���ʵ���Ͳ�õ�������������������Ͳ�ڵ�������ѹ������Ͳ�ڣ����б������е�4����ͬʵ�飨���������ͬ��ͬѹ�²ⶨ��������˵����ȷ���ǣ�������
��ͼ��ʾ�����ס�������װ�в�ͬ���ʵ���Ͳ�õ�������������������Ͳ�ڵ�������ѹ������Ͳ�ڣ����б������е�4����ͬʵ�飨���������ͬ��ͬѹ�²ⶨ��������˵����ȷ���ǣ�������| ʵ����� | ����Ͳ������ | ����Ͳ������ |
| 1 | 10mL HCl | 10mL NH3 |
| 2 | 30mL NO2 | 10mL H2O��Һ�� |
| 3 | 20mL HBr | 10mL Cl2 |
| 4 | 10mL CCl4 | 10mL NH3 |
| A�� | ����4��ʵ���������������ԭ��Ӧ | |
| B�� | ʵ��2������Ͳ�����յ���ɫ������NO | |
| C�� | ʵ��3������Ͳ�ڳ�������ɫ���� | |
| D�� | ʵ��4������Ͳ�ڻ����������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com