
【题目】氯酸镁Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下:
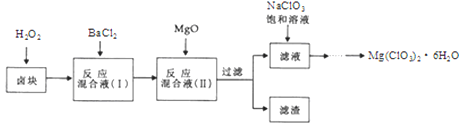
已知:
①.卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②.四种化合物的溶解度(S)随温度(T)变化曲线如图所示。回答下列问题:
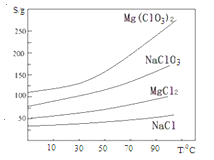
(1).过滤时主要的玻璃仪器有
(2).加入BaCl2的目的是除去杂质离子,检验已沉淀完全的方法是
(3).加入H2O2溶液的作用是: ;加入MgO的作用是
(4).滤渣的主要成分为 。
(5).向滤液中加入NaClO3饱和溶液后,发生反应的化学方程式为:MgCl2 + 2NaClO3 = Mg(ClO3)2↓ + 2NaCl,再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为① ;②趁热过滤;③ ;④过滤、洗涤、干燥。
(6).产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2: 取10.00 mL于锥形瓶中,加入10.00 mL稀硫酸和20.00mL 1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.l000 mol·L-1K2Cr2O7溶液滴定剩余的Fe2+至终点,此过程中反应的离子方程式为:Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ +6Fe3++7H2O。
步骤4:将步骤2、3重复两次,计算得平均消耗K2Cr2O7溶液15.00 mL。
①写出步骤2中发生反应的离子方程式(还原产物为Cl-)
②产品中Mg(ClO3)2·6H2O的质量分数为 【Mg(ClO3)2·6H2O的相对分子质量为299,列出表达式即可)】
【答案】(1)漏斗、烧杯、玻璃棒;
(2)静置,取上层清液适量于试管中,加入BaCl2溶液,若无白色沉淀生成,则SO42-沉淀完全;
(3)使Fe2+氧化,调节溶液的pH,使Fe3+沉淀完全;
(4)BaSO4和Fe(OH)3;(5)蒸发浓缩,冷却结晶;
(6)①ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O;②(11×299)/(12×3.50)% 即 78.3%。
【解析】
试题分析:(1)过滤时用到的主要玻璃仪器有烧杯、玻璃棒、漏斗,答案为:烧杯、玻璃棒、漏斗;(2)加入BaCl2主要是为了除去SO42-,要检验杂质是否除净的方法为:静置,取上层清液适量于试管中,加入BaCl2溶液,若无白色沉淀生成,则SO42-沉淀完全,答案为:静置,取上层清液适量于试管中,加入BaCl2溶液,若无白色沉淀生成,则SO42-沉淀完全;(3)加入过氧化氢的作用是为了将Fe2+氧化,在调节pH除去,所以为了不引入杂质,加入MgO调节pH,答案为:使Fe2+氧化,调节溶液的pH,使Fe3+沉淀完全;(4)滤渣的主要成分有BaSO4和Fe(OH)3,答案为:BaSO4和Fe(OH)3;(5)向滤液中加入NaClO3饱和溶液后,发生反应的化学方程式为:MgCl2+2NaClO3= Mg(ClO3)2↓+2NaCl,进一步制取Mg(ClO3)2·6H2O就需要除去NaCl,操作步骤为:蒸发浓缩、趁热过滤,再冷却结晶,答案为:蒸发浓缩,冷却结晶;(6)①测定Mg(ClO3)2·6H2O含量的原理是用亚铁离子将氯酸根离子还原为氯离子,再用重铬酸钾滴定剩余的亚铁离子,反应的离子方程式分别为:ClO3- + 6Fe2 + + 6H + = 6Fe3 + + Cl- + 3H2O、Cr2O72- + 6Fe2 + + 14H + = 2Cr3 + + 6Fe3 + + 7H2O,答案为:ClO3- + 6Fe2 + + 6H + = 6Fe3 + + Cl- + 3H2O;②10mL产品中ClO3-的物质的量为:1.000mol/L × 0.02L/6-0.1mol/L × 0.015L = 11/120mol, 产品中Mg(ClO3)2·6H2O得含量为:(11 × 299)/(12 × 3.50)% 即 78.3%,答案为:(11 × 299)/(12 × 3.50)% 即 78.3%


科目:高中化学 来源: 题型:
【题目】现有某混合物的无色透明溶液,可能含有以下离子中的若干种:
Na+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份各100mL溶液进行如下实验:
①第一份加入足量AgNO3溶液有沉淀产生,加足量稀硝酸后沉淀部分溶解;
②第二份加足量NaOH溶液充分加热后,收集到气体0.896L(标准状况);
③第三份加足量BaCl2溶液后,过滤后充分干燥得到沉淀6.27g,再经足量稀硝酸洗涤、干燥后,沉淀质量变为2.33g。根据上述实验现象和有关数据,回答下列问题:
(1)原溶液中一定存在的阴离子是 ,一定不存在的离子是 ,可能存在的离子是 。
(2)②中发生化学反应的离子方程式为 。
(3)③中生成可溶于稀硝酸的沉淀化学式为 ,物质的量为 mol,该沉淀溶于稀硝酸的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分离提纯方法选择不正确的是
A | 除去氯化钠溶液中的泥沙 | 过滤 |
B | 用四氯化碳提取溴水中的溴 | 萃取 |
C | 分离乙酸(沸点 118℃ )与乙酸乙酯(沸点 77℃ ) | 分液 |
D | 从含有少量氯化钠的硝酸钾溶液中提取硝酸钾 | 结晶 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过分析比较,认为无需检验就可判断其中必有的两种物质是 和 。(填化学式)
(2)为了确定X,现将(1)中的两种物质记为A和B,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生棕色沉淀,向该沉淀中滴入稀硝酸,沉淀部分溶解,最后留有白色沉淀不再溶解。则:
①X为 。
A.SO32-B.SO42- C.CH3COO-D.SiO32-
②A中的化学键类型为
③将0.02mol的A与0.01mol的C同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的质量为 (精确到0.1g)。
④利用上述已经确定的物质,可以检验出D、E中的阳离子。请简述实验操作步骤、现象及结论
(3)将Cu投入到装有D溶液的试管中,Cu不溶解;再滴加稀硫酸,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的 (填相应的离子符号)。有关反应的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物a的分子式和己烷相同,且主链上有4个碳原子,则下列关于a 的观点正确的是( )
A.a分子中可能有三个甲基
B.a的一氯代物可能有三种
C.a的分子式为C6H10
D.a能与溴的四氯化碳溶液发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(本题8分)
(1)化合物A的结构简式为: ,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_________;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为________。
,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_________;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为________。
(2)篮烷分子的键线式如图所示,试回答:

①写出篮烷分子的化学式____________
②篮烷分子的一氯取代物是种数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述中正确的是( )
4NO(g)+6H2O(g),下列叙述中正确的是( )
A.达到化学平衡时4v正(O2)=5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达平衡状态
C.达到化学平衡时,若升高温度,则正反应速率减小,逆反应速率增大
D.平衡混合物中各物质的量浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A是石油裂解气的主要产物之一,其产量常用于衡量一个石油化工发展水平的标志。下列是有机物A~G之间的转化关系:
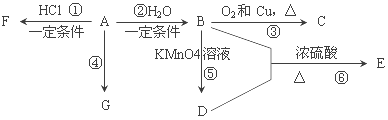
请回答下列问题:
(1)A的官能团的名称是______________________;C的结构简式是______________;
(2)E是一种具有香味的液体,由B+D→的反应方程式为___________,该反应类型是______________;
(4)G是一种高分子化合物,其结构简式是______________;
(4)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质F(沸点12.27°C)进行应急处理.写出由A制F的化学反应方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向10.0 mL 0.10 mol/L氨水中滴入0.10 mol/L的盐酸,溶液的pH与所加盐酸的体积关系如图所示(假设无气体逸出)。下列有关叙述正确的是( )
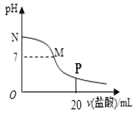
A. M~N间一定存在:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B. M点对应的盐酸体积为10.0mL
C. pH=7的溶液中:c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D. P点处的溶液中存在:2c(NH4+)+2c(NH3·H2O)=c(Cl-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com