
如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是( )
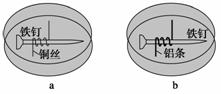
A.a中铁钉附近呈现红色 B.b中铁钉上发生还原反应
C.a中铜丝上发生氧化反应 D.b中铝条附近有气泡产生
科目:高中化学 来源: 题型:
随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
(1)f在元素周期表的位置是__________。
(2)比较d、e常见离子的半径的小(用化学式表示,下同)_______>__________;比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______>__________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式__________。
(4)已知1mole的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:___________________。
(5)上述元素可组成盐R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
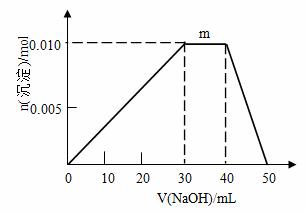
①R离子浓度由大到小的顺序是:__________。
②写出m点反应的离子方程式_________________。
③若R溶液改加20mL1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为__________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室中,下列除去杂质的方法正确的是( )
A.溴苯中混有溴,加入KI溶液,用汽油萃取
B.乙烷中混有乙烯,通氢气在一定条件下反应,使乙烯转化为乙烷
C.硝基苯中混有浓硝酸和浓硫酸,将其倒入浓烧碱溶液中,静置,然后分液
D.乙烷中混有乙炔,通入高锰酸钾酸性溶液洗气除去
查看答案和解析>>
科目:高中化学 来源: 题型:
某化合物有碳、氢、氧三种元素组成,其红外光谱图有C-H键、O-H键、C-O键的振动吸收,该有机物的相对分子质量是60,则该有机物的结构简式是( )
A.CH3CH2OCH3 B.CH3CH(OH)CH3 C.CH3CH2CH2OH D.CH3CH2CH2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,把1 mol N2O4气体通入体积为10 L的真空密闭容器中,立即出现红棕
色,反应进行4 s时,NO2的浓度为0.04 mol·L-1,再经过一定时间后,反应达到平衡,这时
容器内的压强为开始时的1.8倍。则下列说法正确的是( )
A.前4 s以N2O4的浓度变化表示的平均反应速率为0.01 mol·L-1·s-1
B.4 s时容器内的压强为开始时的1.2倍
C.平衡时容器内含0.4 mol N2O4
D.平衡时容器内含0.8 mol NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是)
A. 钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀
B. 原电池反应是导致金属腐蚀的主要原因,故不能用来减缓金属的腐蚀
C. 钢铁电化学腐蚀的两种类型主要区别在于水膜的pH不同,引起的正极反应不同
D. 无论哪种类型的金属腐蚀,其实质都是金属被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com