
【题目】下列反应中必须加入还原剂才能进行的是( )
A.H2→H2O B.Zn→ Zn2+
C.Cl2→Cl- D.CuO→CuCl2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】回答下列问题:

(1)当电极a为A1、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:_____________。
(2)当电极a为Fe、电极b为Cu、电解质溶液为浓硝酸时,该装置_______(填“能”或“不能”)形成原电池,若不能,请说明理由________________________;若能,请写出该电池负极的电极反应方程式____________________。
(3)设计一燃料电池,以电极a为正极,电极b为负极,CH4为燃料,采用酸性溶液为电解液;则CH4应通入_______极(填a或b,下同),电子从_______极流出。电池的负极反应方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物E是一种合成高血压药物的中间体,其合成路线流程图如下:

(1)  中所含官能团名称为_____和______。
中所含官能团名称为_____和______。
(2)苯环上的硝基对新引入基团的位置会产生一定的影响,如:
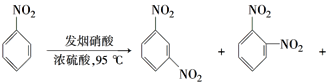 (产物中,间二硝基苯占93%)苯经两步反应制得A,第一步反应的条件为_________。
(产物中,间二硝基苯占93%)苯经两步反应制得A,第一步反应的条件为_________。
(3)写出同时满足下列条件的B的一种同分异构体X的结构简式: _________。
①含有两个苯环,分子中有6种不同化学环境的氢;
②既能与盐酸反应,又能与NaHCO3溶液反应。
(4)合成E时,还可能生成一种与E互为同分异构体的副产物Y,Y的结构简式为______。
(5)常温下,苯酚在Br2的CCl4溶液中发生取代反应,得到一溴代物。请写出以苯酚、CCl4为原料制备 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。______________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过下列反应从硫化物中提取单质锑。
①2Sb2S3+6Fe+3O2![]() Sb4O6+6FeS ②Sb4O6+6C
Sb4O6+6FeS ②Sb4O6+6C![]() 4Sb+6CO↑
4Sb+6CO↑
关于反应①、②的说法不正确的是( )
A. 反应①中被氧化的元素是Sb和Fe
B. 反应①中每生成2molFeS时共转移4mol电子
C. 反应②说明高温下C的还原性比Sb强
D. 每生成2molSb时,反应①与反应②中还原剂的物质的量之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用如图装置制取乙烯,反应原理为 CH3CH2OH![]() CH2═CH2↑+H2O,某化学学习小组通过该原理制取乙烯并对其性质进行验证。
CH2═CH2↑+H2O,某化学学习小组通过该原理制取乙烯并对其性质进行验证。

(1)在制取时,常常需要在烧瓶中加入碎瓷片,目的是____________。
(2)要检验生成的物质,应该首先检验________,常选用的药品为_______________。
(3)制取时,关键要控制好温度。
①温度过高而发生副反应,使部分乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑。为了除去除水蒸气外的杂质气体,常用装有下列试剂的洗气瓶进行洗气,则应选用的试剂是______。
A.酸性KMnO4溶液 B.浓硫酸 C.NaOH溶液 D.溴水
②制取时温度过低,在1400C时主要发生分子间取代反应生成乙醚(CH3CH2OCH2CH3),试写出其反应方程式___________。
(4)将净化后的气体先通入酸性高锰酸钾溶液,酸性高锰酸钾溶液褪色,并有新的无色无味气体产生,该气体可参与大气循环,发生反应的离子方程式为_____。然后将气体通入溴水,溴水褪色,并有油状物质生成。
(5)乙烯的某种同系物的相对分子质量为乙烯的3倍,其同分异构体总数为_____。将其与氢气加成,得到的烷烃再与氯气发生取代反应,其一氯取代产物为三种的烷烃的结构简式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2) 为一元中强酸,具有较强的还原性,可用电渗析法制备,“四室电渗析法”工作原理如下图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。下列叙述不正确的是( )

A. 阳极反应为2H2O-4e-=O2↑+4H+
B. 产品室中发生反应H++ H2PO2-=H3PO2, 该法还可得副产品NaOH
C. 原料室中H2PO2- 向左移动,Na+ 向右移动,该室pH 升高
D. 阳膜1的主要作用是防止H2PO2- 进入阳极室被氧化并允许H+通过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组对Mg和Al的性质进行了下列的实验及研究。

(1)以镁条、铝片为电极,稀NaOH溶液为电解质构成的原电池(如图1所示)时发现,刚开始时,电流表指针向右偏转,镁条做负极;但随后很快指针又向左偏转,镁条表面有极少量的气泡产生。
①开始阶段,负极发生的反应是________。
②随后阶段,铝片发生的电极反应式是_______;则镁电极发生的电极反应式是________。
(2)经研究测定,镁与不同浓度的硝酸反应,生成气体产物的含量随HNO3浓度变化曲线如图2所示,溶液中的产物有Mg(NO3)2、NH4NO3和H2O。96 mg Mg在1 L 4molL﹣1的HNO3中完全溶解,并可收集到22.4mL(标准状况下)气体(忽略反应过程中HNO3浓度的变化),该反应的化学方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol/L的Na2SO4溶液是 ( )
A. 溶液中含有1mol Na2SO4
B. 1升水中加入142g Na2SO4
C. 1mol Na2SO4溶于1mol水中
D. 将322g Na2SO4·10H2O溶于少量水后再稀释成1000mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com