
����Ŀ�����з�ӦaA(g)+bB(g) ![]() pC(g)����֪���ﵽƽ��������¶ȣ�B��ת���ʱ��Сѹǿ��C������������С��
pC(g)����֪���ﵽƽ��������¶ȣ�B��ת���ʱ��Сѹǿ��C������������С��
��1���÷�Ӧ���淴Ӧ��________��Ӧ����������������������������a+b______p������<������>������=������
��2���¶ȡ�����������䣬ƽ������B��A��ת����_________��B��ת����_________��������������������С��������������
��3���������¶ȣ��ٴ�ƽ��ʱ��B��C��Ũ��֮�Ƚ�_____________��������������������С��������������
��4��������������ٴ�ƽ��ʱ��������������ʵ���___________��������������������С��������������
��5����B����ɫ���壬A��C��ɫ��ƽ���ѹ���������Ϊԭ����һ�룬�ٴ�ƽ��ʱ��������������ɫ____����ά������������ѹǿ���䣬����Ne���ٴ�ƽ��ʱ��������������ɫ__________��������������������dz��������������
���𰸡����� > ���� ��С ��С ���� ���� 26.����@>@����@��С@��С@����@����@��dz
��������
���⿼����������ԭ������1�������¶ȣ�B��ת���ʱ��˵����Ӧ������Ӧ������У�������Ӧ����Ϊ���ȷ�Ӧ�����淴ӦΪ���ȷ�Ӧ����Сѹǿ��C������������С��˵����Ӧ���淴Ӧ������У���a��b>p����2��ƽ������B�����ӷ�Ӧ���Ũ�ȣ�ƽ��������Ӧ�����ƶ�����A��ת��������B���������ӣ���B�ĵ�ת���ʽ��ͣ���3������Ӧ�����ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ���B�����ʵ�����С��C�����ʵ�������B��C��Ũ��֮�ȼ�С����4��ʹ�ô������Ի�ѧƽ����Ӱ�죬����������������ʵ������䣻��5��ƽ���ѹ���������������ֵ�Ũ�ȶ�����������ɫ�����ѹʱ������Ƿ�Ӧ���壬���������������ֵ�Ũ�Ƚ��ͣ�������ɫ��dz��


 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I����ͼ��ȫ��Һ����ص�ʾ��ͼ
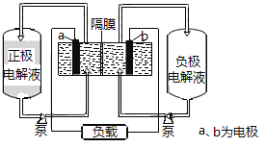
�õ�س�ŵ���ܷ�ӦʽΪ��![]()
��ش��������⣺
��1�����ʱ��������ӦʽΪ______________������������ɫ�仯��______��
��2���ŵ�����У�����������Һ��pH ________��ѡ��������������������������������
II���������÷Ϸ���������Ҫ�ɷ�ΪV2O5��VOSO4�Ͷ������裩�Ĺ�����������ͼ��ʾ��
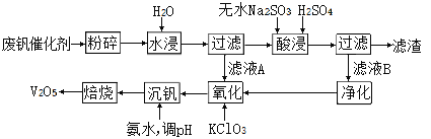
��3������������______________________����һ����;����
��4��25��ʱ��ȡ������ʵ��������õ��������ʺ���ҺpH֮��Ĺ�ϵ���±���ʾ��
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
�������ʣ����� | 88.1 | 91.8 | 96.5 | 98 | 99.8 | 97.8 | 96.4 | 93.0 | 89.3 |
�����ϱ������жϣ����백ˮ��������ԣ���Һ�����pHΪ____��
��5��Ϊ����߷��Ľ����ʣ������ʹ�Ϸ������е�V2O5ת��ɿ�����ˮ��VOSO4����������У���������ͻ�ԭ��������ʵ���֮��Ϊ________��
��6�����������У�VO2+��ΪVO2+����÷�Ӧ�����ӷ���ʽΪ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���һ�ݻ�������ܱ������з������淴ӦA(g)��3B(g)![]() 2C(g)����ﵽƽ��״̬�ı�־��( )
2C(g)����ﵽƽ��״̬�ı�־��( )
A. C���ɵ�������C�ֽ���������
B. ��λʱ������n mol A��ͬʱ����3n mol B
C. ��ϵ���ܶȲ��ٱ仯
D. A��B��C��Ũ��֮��Ϊ1��3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������ȷ���ǣ� ��
A.�����Ҵ���ӦB.���ܽ⼦����
C.ʳ���к�������D.Ϊһ����ɫ��ζ��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ���ѧϰ��ѧ����Ҫ����,������������Ϣ���ɡ��±����������ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼ�(��֪��Ԫ�ص�ԭ�Ӱ뾶Ϊ0.089 nm)��
Ԫ�ش��� | A | B | C | D | X | Y |
ԭ�Ӱ뾶/nm | 0.037 | 0.143 | 0.102 | 0.099 | 0.074 | 0.075 |
��Ҫ���ϼ� | +1 | +3 | +6,-2 | -1 | -2 | +5,-3 |
��1��CԪ�������ڱ��е�λ��Ϊ________�������ӽṹʾ��ͼΪ��_______��
��2��B������������Ӧ��ˮ������Y������������Ӧ��ˮ���ﷴӦ�����ӷ���ʽΪ___��
��3������C��D ����Ԫ��˵����ȷ����__________������ţ���
a.�����ӵİ뾶D>C b.��̬�⻯����ȶ���D��Cǿ c.����������Ӧ��ˮ���������C��Dǿ
��4����100mL18mol/L��C������������Ӧ��ˮ�����Ũ��Һ�м��������ͭƬ������ʹ���ַ�Ӧ��������������Ϊ6.72L(����£�����÷�Ӧ������ת�Ƶĵ�����Ϊ______��
��5��д����A��D��X����Ԫ����ɵ�ij�ֿ�������ɱ�����ʵĵ���ʽ_____________��
��6���Ƚ�YԪ������ͬ�������Ԫ�ص��⻯����۷е�ߵ�__ ��___ (���⻯�ﻯѧʽ��������___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������µ��ݻ������������,���������������ٱ仯ʱ,������ӦA(g)+2B(g)![]() 3C(g)+D(s)�Ѵﵽƽ�����(����)
3C(g)+D(s)�Ѵﵽƽ�����(����)
�� ��������ѹǿ���� ���������ܶȡ�
�� ������������������ ����������ʵ���
A. �� ��B. �� ��C. �� �� ��D. �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�����Ϊȼ�ϵ�ص�ԭ�ϡ�ͨ�����з�Ӧ�����Ʊ��״���CO ( g ) + 2H2 ( g ) ![]() CH3OH ( g ) ��H ����90.8 kJ��mol��1 ����һ�ݻ��ɱ���ܱ������г���10 mol CO ��20 mol H2��CO ��ƽ��ת�������¶���T����ѹǿ��P���ı仯��ͼ��ʾ�����ﵽƽ��״̬A ʱ�����������Ϊ20 L��
CH3OH ( g ) ��H ����90.8 kJ��mol��1 ����һ�ݻ��ɱ���ܱ������г���10 mol CO ��20 mol H2��CO ��ƽ��ת�������¶���T����ѹǿ��P���ı仯��ͼ��ʾ�����ﵽƽ��״̬A ʱ�����������Ϊ20 L��

��1��T1����Ӧ��ƽ�ⳣ��Ϊ_______________��
��2��ͼ��P1 _______ P2������>������<������=�������練Ӧ��ʼʱ�Գ���10 mol CO��20 mol H2������ƽ��״̬Bʱ���������V(B)=__________L��
��3�����ڷ�ӦCO(g)+2H2(g)![]() CH3OH(g)�ڻ�ѧƽ��״̬Bʱ��������ȷ����________
CH3OH(g)�ڻ�ѧƽ��״̬Bʱ��������ȷ����________
A��CO�ĺ������ֲ��� B��������CH3OHŨ����COŨ�����
C��2v��(CH3OH)= v��(H2) D�������л�������ƽ����Է����������ֲ���
��4����֪CO2(g)+H2(g) ![]() CO(g) + H2O(g) ��H = + 41.3 kJ��mol��1 ����д����CO2��H2��ȡ�״����Ȼ�ѧ����ʽ___________________________________��
CO(g) + H2O(g) ��H = + 41.3 kJ��mol��1 ����д����CO2��H2��ȡ�״����Ȼ�ѧ����ʽ___________________________________��
��5����CH3OH��O2��ϡH2SO4���ȼ�ϵ�أ�д���õ�������ĵ缫��Ӧʽ��_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������������ķ�����һ����ȵ���
A. ͬ�ܶ���ͬѹǿ�� N2 �� C2H4 B. ͬ�¶ȡ�ͬ����� O2 �� N2
C. ͬ�����ͬ�ܶȵ� C2H4 �� CO D. ͬѹǿ��ͬ����� O2 �� N2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡһС���Ʒ�����������ȣ�����ʵ��������ȷ����( )
���������ۻ� ���ڿ�����ȼ�գ�����ʻ�ɫ ��ȼ��ʱ��������
��ȼ�պ����ɵ���ɫ���� ��ȼ�պ����ɰ�ɫ����
A. �٢ڢ� B. �٢ڢ� C. �٢ڢ� D. �٢ۢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com