
| A. | 蛋白质和油脂都属于高分子化合物,一定条件下都能水解 | |
| B. | 甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 | |
| C. | 乙酸分子中含有羧基,可与NaHCO3溶液反应生成CO2 | |
| D. | 苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 |
分析 A.油脂的相对分子质量在10000以下;
B.甲烷中H被Cl取代,苯中的H被硝基取代;
C.乙酸中含-COOH,具有酸性;
D.碳碳双键能与溴发生加成反应.
解答 解:A.油脂的相对分子质量在10000以下,不是高分子,而蛋白质为高分子,二者均可发生水解反应,故A错误;
B.甲烷中H被Cl取代,苯中的H被硝基取代,均为取代反应,故B正确;
C.乙酸中含-COOH,具有酸性,则与NaHCO3溶液反应生成CO2,故C正确;
D.碳碳双键能与溴发生加成反应,则苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键,故D正确;
故选A.
点评 本题考查有机物的结构与性质,为高考常见题型和高频考点,侧重于学生的分析能力和应用能力的考查,注意有机物的官能团及反应类型,题目难度不大.


科目:高中化学 来源: 题型:解答题
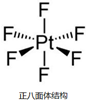 Ⅰ.一定条件下,O2可通过得失电子转化为O2-、O2+ 和O22-.
Ⅰ.一定条件下,O2可通过得失电子转化为O2-、O2+ 和O22-.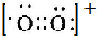 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
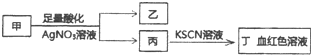
| A. | 若乙为白色沉淀,则甲可能含有SiO32- | |
| B. | 若乙为黄色沉淀,则甲可能为FeI3 | |
| C. | 若乙为浅黄色沉淀,则甲可能含有S2- | |
| D. | 若乙为浅黄色沉淀,则甲可能是FeBr2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

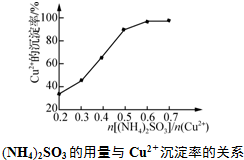 ,工业上$\frac{n[(N{H}_{4})_{2}S{O}_{3}]}{n(C{u}^{2+})}$采用0.6最为适宜,此时(NH4)2SO3略过量,其原因是保证生成的CuCl不被氧气氧化或(NH4)2SO3被空气中的氧气氧化.
,工业上$\frac{n[(N{H}_{4})_{2}S{O}_{3}]}{n(C{u}^{2+})}$采用0.6最为适宜,此时(NH4)2SO3略过量,其原因是保证生成的CuCl不被氧气氧化或(NH4)2SO3被空气中的氧气氧化.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23 g Na与足量H2O反应完全后可生成NA个H2分子 | |
| B. | 1 mol Cu和足量热浓硫酸反应可生成NA个SO3分子 | |
| C. | 标准状况下,22.4 L N2和H2混合气中含NA个原子 | |
| D. | 3 mol单质Fe完全转变为Fe3O4,失去8NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 A1/MnO4-电池是一种高能电池,以Ga2O3为缓蚀剂,其示意图如图所示.已知电池总反应为Al+MnO4-+2H2O═Al(OH)4-+MnO2.下列说法正确的是( )
A1/MnO4-电池是一种高能电池,以Ga2O3为缓蚀剂,其示意图如图所示.已知电池总反应为Al+MnO4-+2H2O═Al(OH)4-+MnO2.下列说法正确的是( )| A. | 电池工作时,K+向负极移动 | |
| B. | 电池工作时,Al电极周围溶液pH增大 | |
| C. | 正极反应为MnO4-+2H2O+3e-═MnO2+4OH- | |
| D. | 电池工作时,电子由Al经溶液流向Ni |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 雷雨天气时产生少量NO | |
| B. | 往农田中施放铵态氮肥 | |
| C. | 豆科植物等根部的根瘤菌吸收空气中的氮气转变为氨 | |
| D. | N2和H2在高温、高压和催化剂存在下合成氨 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com