
【题目】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体)向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果错误的是

A. 混合酸中NO3-物质的量为0.4mol
B. OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C. 第二份溶液中最终溶质为FeSO4
D. H2SO4浓度为5 mol·L-1
【答案】D
【解析】试题分析:A.OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,硝酸全部起氧化剂作用,所以n(NO3-)=2n(Fe)=2×(11.2g÷56g/mol)=0.4mol,正确;B.由图像可知,由于铁过量,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑,正确;C.硝酸全部被还原,没有显酸性的硝酸,因为溶液中有硫酸根,并且铁单质全部转化为亚铁离子,所以溶液中最终溶质为FeSO4,正确;D.反应消耗22.4g铁,也就是22.4g÷56g/mol=0.4mol,所有的铁都在硫酸亚铁中,根据硫酸根守恒,所以每份含硫酸0.4mol,所以硫酸的浓度是c=0.4mol÷0.1L=4mol/l,错误。


科目:高中化学 来源: 题型:
【题目】制备单质锰的实验装置如图所示,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,电解装置中大箭头表示溶液中阴离子移动的方向。下列说法不正确的是( )

A.M是电源的负极
B.左侧气孔逸出的气体可能为副产物H2
C.电解槽中发生的总反应为MnSO4+2H2O![]() MnO2+H2↑+H2SO4
MnO2+H2↑+H2SO4
D.若用阳离子交换膜代替阴离子交换膜,阳极可能得到MnO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方案能达到实验目的的是
A. 用浓硫酸干燥NH3 B. 用乙醇萃取溴水中的溴单质
C. 用品红溶液鉴别SO2和CO2 D. 用焰色反应鉴别KCl和KOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下图所示的四个原电池装置,其中结论正确的是

A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为6H2O+6e-===6OH-+3H2↑
C.③中Fe作正极,电极反应式为Fe-2e-===Fe2+
D.④中Cu作正极,电极反应式为2H++2e-===H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关能源的理解或说法错误的是
A. 煤、石油、太阳能、风能等均属于新能源
B. 乙醇是一种可再生能源,可代替汽油作为汽车燃料
C. 氢气是最轻的燃料,是具有广阔发展前景的能源
D. 研发开采可燃冰(水合甲烷)的技术,可大大缓解能源危机
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3溶液与KSCN溶液混合时存在平衡:Fe3+(aq)+SCN-(aq)Fe(SCN)2+(aq)。已知某一条件下,反应达到平衡时,Fe(SCN)2+的物质的量浓度与温度的关系如图所示,下列说法正确的是( )
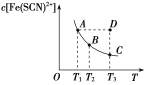
A.该反应为吸热反应
B.T1、T2时反应的平衡常数分别为K1、K2,则K1>K2
C.反应处于D时,一定有v正大于v逆
D.A点的c(Fe3+)比B点的c(Fe3+)大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列试剂贮存方法错误的是( )
A.浓硫酸密封保存
B.氢氟酸保存在玻璃瓶中
C.新制氯水保存在棕色试剂瓶中
D.烧碱溶液可用带橡皮塞的玻璃瓶暂时保存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B![]() 3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A. υ(A)= 0.5 mol/(L·s) B. υ(B)= 0.3 mol/(L·s)
C. υ(C)= 12 mol/(L·min) D. υ(D)= 6 mol/(L·min)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com