
【题目】下列离子方程式正确的是
A. 钠和水反应:Na+H2O==Na++OH-+H2↑
B. 盐酸与氢氧化钠溶液反应:H++OH-==H2O
C. 三氯化铁腐蚀印刷线路板:Fe3++Cu==Fe2++Cu2+
D. 醋酸与碳酸钠反应制备二氧化碳:CO32-+2H+==CO2↑+H2O
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A.图1表示1 L pH=2的CH3COOH溶液加水稀释至V L,pH随lg V的变化
B.图2表示不同温度下水溶液中H+和OH-浓度的变化的曲线,图中温度T2>T1
C.图3表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率小于b点
D.图4表示同一温度下,在不同容积的容器中进行反应2BaO2(s)![]() 2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系
2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏伽德罗常数,下列说法正确的是( )
A.16g氧气和臭氧的混合物中含有的氧原子数为NA
B.标准状况下,22.4 L水中含有的氧原子数为NA
C.NA个氯气分子的体积为22.4L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有的Cl﹣个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在l0℃时,10 mL 0.4 mol L-1H2O2溶液发生催化分解:2H2O2![]() 2H2O+O2↑,不同时刻测得生成O2的体积(已折算为标准状况)如下表:
2H2O+O2↑,不同时刻测得生成O2的体积(已折算为标准状况)如下表:
t/min | 0 | 2 | 4 | 6 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 |
下列叙述不正确的是(溶液体积变化忽略不计)
A. 0~2 min的平均反应速率比4~6 min快
B. 0~6 min 的平均反应速率v(H2O2)=3.3×10-2 moL-1 L-1 min-1
C. 反应至 6 min 时,c(H2O2)=0.3 mol·L-1
D. 反应至6 min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近两年流行喝苹果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品。苹果酸(α-羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构式如下,下列说法不正确的是

A.苹果酸在一定条件下能发生酯化反应
B.苹果酸在一定条件下能发生催化氧化反应
C.苹果酸在一定条件下能发生消去反应
D.1 mol苹果酸与Na2CO3溶液反应最多消耗3 mol Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镓(Ga)位于周期表的第四周期,与Al同主族,主要存在Ga3+、GaO2-两种离子形态,被广泛应用于电子工业。
(1)Ga的原子序数为______。
(2)半导体材料氮化稼是由Ga与NH3在一定条件下合成的,该过程中每生成3molH2时,就会放出30.8kJ的热量。
①反应的热化学方程式是________。
②反应的化学平衡翻常数表决达式是_________________。
③在恒温恒容的密闭体系内进行上述可逆反应,下列有关表达正确的是_____(填字母代号).

A.Ⅰ图象中如果纵坐标为正反应速率,则t时刻改变的条件可以为升温或加压
B.Ⅱ图象中纵坐标可以为稼的转化率
C.Ⅲ图象中纵坐标可以为化学反应速率
D.Ⅳ图象中纵坐标可以为体系内混合气体的平均相对分子质量
(3)工业上多用电解精炼法提纯稼。具体原理如下图所示:

已知:金属的活动性Zn>Ga>Fe>Cu
①X为电源的_____极,电解精炼稼时阳极泥的成分是__________;
②在电解过程中使某种离子迁移到达阴极并在阴极放电析出高纯稼, 请写出该电解过程中的电极反应方程式:阳极_________;阴极_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在等体积的NaCl、MgCl2、AlCl3三种溶液中,分别加入等量的AgNO3溶液,恰好都完全反应,则以上三种溶液的物质的量浓度之比为( )
A.1:2:3
B.3:2:1
C.1:1:1
D.6:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物X、Y和高聚物Z,可以用烃A为主要原料,采用以下路线合成。
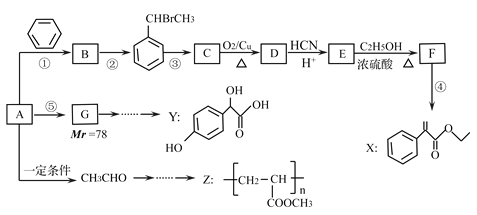
已知:Ⅰ.反应①、反应②的原子利用率均为100%.
Ⅱ. (R或R可以是烃基或氢原子)
(R或R可以是烃基或氢原子)
请回答下列问题:
(1)A的结构简式为____________。
(2)Z中的官能团名称为__________,反应③的条件为___________。
(3)关于药物Y(![]() )的说法正确的是______________。
)的说法正确的是______________。
A.1mol药物Y与足量的钠反应可以生成33.6L氢气。
B.药物Y的分子式为C8H8O4,能使酸性高锰酸钾溶液褪色
C.药物Y中⑥、⑦、⑧三个-OH的酸性由强到弱的顺序是⑧>⑥>⑦
D.1mol药物Y与H2、浓溴水中的Br2反应,最多消耗H2、Br2分别为4mol和2mol
(4)写出反应E→F的化学方程式_________________,F→X的化学方程式______________________。
(5)写出符合下列条件的E的一种同分异构体的结构简式____________。
①遇FeCl3溶液可以发生显色反应,且是苯的对位二元取代物;②能发生银镜反应和水解反应;③核磁共振氢谱有6个峰。
(6)参考上述流程以CH3CHO和CH3OH为起始原料,其它无机试剂任选,设计合成Z的线路。_________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com