
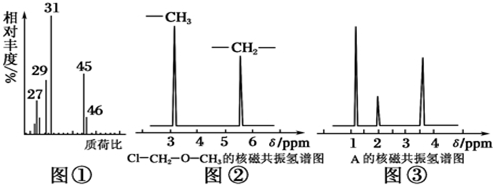
���� I����1��Ũ��������Ϊˮ����������ʯ������Ϊ������̼���������Դ˿�ȷ���л�����C��Hԭ�Ӹ�����ֵ��������������������ȷ���л����и�ԭ�Ӹ�����ֵ��
��2�������л���ԭ�Ӹ�����ֵ��ȷ�����ʽ�������Է���������ȷ���л������ʽ��
��3�������л������ʽ��ϼۼ����ۿ�ȷ���л���Ŀ��ܽṹ��
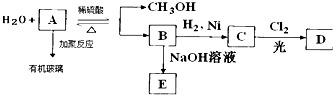
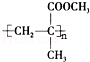
II����4���л���A�����������ֲ�ͬ��ѧ��������ԭ�ӣ�ӦΪ�Ҵ���
��� �⣺I����1���������֪n��H2O��=$\frac{5.4g}{18g/mol}$=0.3mol��n��CO2��=$\frac{8.8g}{44g/mol}$=0.2mol��n��O2��=$\frac{6.72L}{22.4L/mol}$=0.3mol��
������ԭ���غ��֪�л����к���n��O��=0.3mol+0.2mol��2-0.3mol��2=0.1mol��
���л�����N��C����N��H����N��O��=0.2mol��0.6mol��0.1mol=2��6��1��ʵ��ʽΪC2H6O��
�ʴ�Ϊ��C2H6O��
��2���������и�Ԫ�ص�ԭ�Ӹ�����ΪN��C����N��H����N��O��=2��6��1�������ʽΪC2H6O������Է�������Ϊ46�����л���ķ���ʽΪC2H6O��
�ʴ�Ϊ��C2H6O��
��3���л���ķ���ʽΪC2H6O�������п��ܴ���C-C��C-H��C-O��O-H�Ȼ�ѧ�������ܵĽṹ��ʽ��CH3CH2OH��CH3OCH3��
�ʴ�Ϊ��CH3CH2OH��CH3OCH3��
�� ��4���л���A�����������ֲ�ͬ��ѧ��������ԭ�ӣ�ӦΪ�Ҵ�����CH3CH2OH��������ֻ��һ�ֲ�ͬ��ѧ��������ԭ�ӣ�
�ʴ�Ϊ��CH3CH2OH��
���� ���⿼���л�����ƶϣ�������ѧ���ķ�����ʵ��ͼ��������Ŀ��飬Ϊ�߿��������ͣ���Ŀ�Ѷ��еȣ����غ�Ƕ��ж��л������ʽΪ������Ĺؼ���ע����������ͼ���˴Ź������ס�����������л���ṹȷ���е����ã�


 �Ƹ�С״Ԫͬ������������ϵ�д�
�Ƹ�С״Ԫͬ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� CH3OH+CH2=C��CH3��COOH��
CH3OH+CH2=C��CH3��COOH���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ŵ�ʱ��CH3OH���뷴Ӧ�ĵ缫Ϊ���� | |
| B�� | �ŵ�ʱ��ÿͨ������11.2L O2��ȫ��Ӧת�Ƶ�����Ϊ1mol | |
| C�� | �ŵ�ʱ���������Һ��pH������ | |
| D�� | �ŵ�ʱ��������ӦΪ��CH3OH-6e-+8OH-=CO32-+6H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
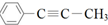 ��������ȷ���ǣ�������
��������ȷ���ǣ�������| A�� | ���л�����ֻ���зǼ��Լ� | |
| B�� | ���л�������ˮ�ļӳɲ���ֻ��1�� | |
| C�� | �÷����������10��ԭ�ӹ�ƽ�� | |
| D�� | �÷����������5��̼ԭ�ӹ�ֱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�ɢϵ�ķ�ɢ��ΪFe2O3 | |
| B�� | �ڵ糡�����£�����������ɢϵ��ɫ�����˵���÷�ɢϵ������� | |
| C�� | ����NaOHʱ�����ķ�Ӧ����Ϊ��Fe2++2Fe3++8OH-�TFe3O4+4H2O | |
| D�� | ���ù��˵ķ�������ɫ������������Na+���뿪 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
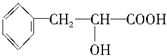
 ��ֻҪ��д��һ����ѧ����ʽ���л���д�ṹ��ʽ����
��ֻҪ��д��һ����ѧ����ʽ���л���д�ṹ��ʽ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������ɫ���ٱ仯 | |
| B�� | ��λʱ��������nmol������ͬʱ����nmol������ | |
| C�� | ���÷�Ӧ�ڸ����ܱ�����㶨�������н��з�Ӧ����ϵ���¶Ȳ��ٱ仯 | |
| D�� | 2v����H2��=v����HI�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
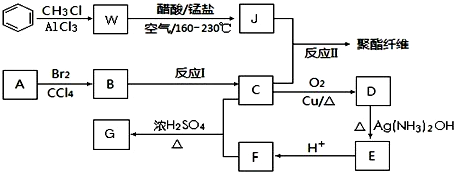
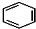 +RCl$\stackrel{AlCl_{3}}{��}$
+RCl$\stackrel{AlCl_{3}}{��}$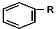 +HCl��-R������
+HCl��-R������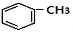 $��_{����/160-230��}^{����/����}$
$��_{����/160-230��}^{����/����}$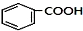
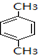 ��
��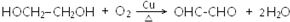 ��
��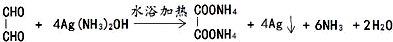 ��
��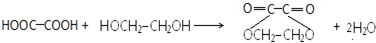 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com