
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列溶液中粒子的物质的量浓度关系正确的是
A.0.1mol·L1NaHC2O4溶液与0.1mol·L1KOH溶液等体积混合,所得溶液中:
c(Na)>c(K)>c(C2O42)>c(OH)>c(HC2O4)
B.20mL 0.1 mol·L1NH4Cl溶液与10mL 0.1mol·L1NaOH溶液混合后溶液呈碱性,所得溶液中:c(Cl)>c(NH4+)>c(Na)>c(OH)>c(H)
C.常温下,pH=2的HF溶液与pH=12的氢氧化钠溶液等体积混合,所得溶液中:
c(Na)+c(OH)>c(H)+c(F)
D.0.1mol·L1NH3·H2O溶液与0.1mol·L1HNO3等体积混合,所得溶液中:
c(H)>c(OH)+c(NH3·H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
用试纸检验气体性质是一种重要的实验方法。如图所示的实验中(可加热),下列试纸的选用、现象及对应结论都正确的一项是( )
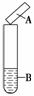
| 选项 | 试剂B | 湿润的试纸A | 现象 | 结论 |
| A | 碘水 | 淀粉试纸 | 变蓝 | 碘具有氧化性 |
| B | 浓氨水,生石灰 | 蓝色石蕊试纸 | 变红 | 氨气为碱性气体 |
| C | Na2SO3,硫酸 | 品红试纸 | 褪色 | SO2具有漂白性 |
| D | Cu,浓硝酸 | 淀粉KI试纸 | 变蓝 | NO2为酸性气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
10 ℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50 ℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
甲同学认为:该溶液pH升高的原因是HCO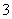 的水解程度增大,碱性增强。
的水解程度增大,碱性增强。
乙同学认为:该溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度________NaHCO3的水解程度(填“大于”或“小于”)。
丙同学认为甲、乙的判断都不充分。
丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则________(填“甲”或“乙”)的判断正确。试剂X是________。
A.Ba(OH)2溶液 B.BaCl2溶液
C.NaOH溶液 D.澄清石灰水
(2)将加热煮沸后的溶液冷却到10 ℃,若溶液的pH________8.3(填“高于”、“低于”或“等于”),则________(填“甲”或“乙”)判断正确。
(3)查阅资料,发现NaHCO3的分解温度为150 ℃,丙断言________(填“甲”或“乙”)判断是错误的,理由是__________________________________ _______________________________________________________________。
(4)关于NaHCO3饱和水溶液的表述正确的是_______________________。
a.c(Na+)=c(HCO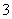 )+c(CO
)+c(CO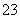 )+c(H2CO3)
)+c(H2CO3)
b.c(Na+)+c(H+)=c(HCO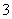 )+c(CO
)+c(CO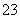 )+c(OH-)
)+c(OH-)
c.HCO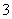 的电离程度大于HCO
的电离程度大于HCO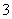 的水解程度
的水解程度
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不符合ⅦA族元素性质特征的是
A.易形成-1价离子 B.从上到下原子半径逐渐减小
C.从上到下非金属性逐渐减弱 D.从上到下氢化物的稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化合物,既能与强酸反应,又能与强碱溶液反应的是
①Al(OH)3 ②NaHCO3 ③(NH4)2S ④NaHSO4
A.只有① B.①和② C.①②③ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。E是地壳中含量最高的金属元素。
根据以上信息回答下列问题:
(1)D元素在周期表中的位置是 ,乙物质的化学式是 •
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写)
。
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是
查看答案和解析>>
科目:高中化学 来源: 题型:
现有四种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4 ②1s22s22p63s23p3 ③1s22s22p3 ④1s22s22p5
则下列有关比较中正确的是( )
A.第一电离能:④>③>②>①
B.原子半径:④>③>②>①
C.电负性:④>③>②>①
D.最高正化合价④>③=②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z是原子序数依次增大的4种短周期元素(稀有气体除外)。其中只有X为金属元素,焰色反应为黄色。W、Y的原子最外层电子数相等,且W的原子最外层电子数是其内层电子数的3倍。请回答:
(1)W在元素周期表中的位置 。
(2)X单质与水反应的离子方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com