
| A. | 把一段打磨过的镁带放入少量冷水中 | |
| B. | 把 Cl2通入FeCl2溶液中 | |
| C. | 把绿豆大的钾投入水中 | |
| D. | 氢氟酸滴到玻璃上 |
分析 A.镁和冷水不反应;
B.氯气和氯化亚铁反应生成氯化铁,亚铁离子在溶液中呈浅绿色、铁离子在溶液中呈黄色;
C.K和水剧烈反应生成KOH和氢气;
D.玻璃中含有二氧化硅,二氧化硅和HF反应生成四氟化硅和水.
解答 解:A.镁和沸水反应生成氢氧化镁和氢气,镁和冷水不反应,所以看不到明显现象,故A正确;
B.氯气具有强氧化性,氯气和氯化亚铁反应生成氯化铁,亚铁离子在溶液中呈浅绿色、铁离子在溶液中呈黄色,所以看到溶液由浅绿色变为黄色,有明显现象,故B错误;
C.K和水剧烈反应生成KOH和氢气,且K浮在水面上,四处游动,产生紫色火焰,所以有明显现象,故C错误;
D.玻璃中含有二氧化硅,二氧化硅和HF反应生成四氟化硅和水,玻璃被腐蚀,有明显现象,故D错误;
故选A.
点评 本题考查元素化合物性质,明确物质的性质及物质之间发生的反应是解本题关键,会运用化学语言描述现象,题目难度不大.


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | SiO2 H4SiO4 | B. | Cl2O HClO4 | C. | Mn2O7 HMnO4 | D. | N2O5 HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
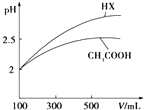 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6 mol | B. | 2.8 mol | C. | 3.2 mol | D. | 3.6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧碱溶液中通入过量二氧化硫 2OH-+SO2═SO32-+H2O | |
| B. | 在亚硫酸氢铵稀溶液中加入足量的氢氧化钠稀溶液 NH4++H++2OH-═NH3•H2O+H2O | |
| C. | 硫酸铁的酸性溶液中通入足量硫化氢 2Fe3++H2S═2Fe2++S↓+2H+ | |
| D. | 铜与浓硝酸:Cu+2H++2NO3-═Cu2++2NO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
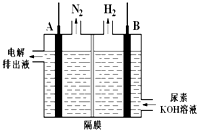
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 位于同一主族的元素的价电子数相同,则各元素的常见化合价也一定相同 | |
| B. | 碱金属族元素同卤族元素一样,其单质的熔沸点随元素原子序数的增大而逐渐升高 | |
| C. | 若x是ⅡB族中元素的原子序数,那么原子序数为x+1的元素是ⅢA族 | |
| D. | 在周期表中金属和非金属元素的分界线附近的元素是过渡元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com