
一定条件下,发生反应:①M(s)+N(g)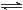 R(g) △H = -Q1 kJ·mol-1,②2R (g)+N(g)
R(g) △H = -Q1 kJ·mol-1,②2R (g)+N(g)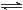 2T (g) △H = -Q2 kJ·mol-1。 Q1、Q2 、Q3均为正值。下列说法正确的是
2T (g) △H = -Q2 kJ·mol-1。 Q1、Q2 、Q3均为正值。下列说法正确的是
A.1 mol R(g)的能量总和大于1 mol M(s)与1 mol N(g) 的能量总和
B.将2 mol R (g)与1 mol N(g)在该条件下充分反应,放出热量Q2 kJ
C.当1 mol M(s)完全转化为T (g)时(假定无热量损失),放出热量Q1+ kJ
kJ
D.M(g)+N(g)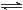 R(g) △H=-Q3 kJ·mol-1 , 则Q3 <Q1
R(g) △H=-Q3 kJ·mol-1 , 则Q3 <Q1
C
【解析】
试题分析:A、反应①为放热反应,1 mol R(g)的能量总和小于1 mol M(s)与1 mol N(g) 的能量总和,错误; B、反应②为可逆反应,可逆反应不能进行到底,将2 mol R (g)与1 mol N(g)在该条件下充分反应,放出热量小于Q2 kJ,错误;C、根据反应①、②,利用盖斯定律分析知,当1 mol M(s)完全转化为T (g)时(假定无热量损失),放出热量Q1+Q2/2kJ,正确;D、1 molM(g)具有的能量大于1 molM(s),结合反应①知,M(g)+N(g)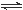 R(g) △H=-Q3 kJ·mol-1 , 则Q3 >Q1,错误。
R(g) △H=-Q3 kJ·mol-1 , 则Q3 >Q1,错误。
考点:考查化学反应与能量变化。


科目:高中化学 来源:2013-2014重庆市下学期期中考试高二化学试卷(解析版) 题型:填空题
(10分)下图是研究铜与浓硫酸的反应装置:
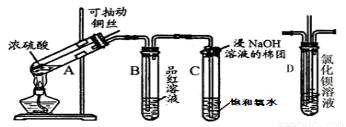
(1)A试管中发生反应的化学方程式为 。
(2)反应一段时间后,可观察到B试管中的现象为 。
(3)C试管口浸有NaOH溶液的棉团作用是 。
(4)实验结束后,证明A试管中反应所得产物是否含有铜离子的操作方法是 。
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,经查阅文献获得下列资料。
资料1 |
附表铜与浓硫酸反应产生黑色物质的相关性质 |
资料2 | X射线晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种。 |
仅由上述资料可得出的正确结论是 。
A.铜与浓硫酸反应时所涉及的反应可能不止一个 B.硫酸浓度选择适当,可避免最后产物中出现黑色物质;C.该反应发生的条件之一是硫酸浓度≥15 mol·L D.硫酸浓度越大,黑色物质越快出现、越难消失
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市下学期期中考试高一化学试卷(解析版) 题型:选择题
下列有关说法正确的是( )
A.大多数金属在自然界以游离态形式存在
B.工业上,一般用热还原法获得Hg和Ag
C.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
D.人们常用钢作建造材料而不用纯铁主要原因是钢的机械性能更好
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市5月高三月考理综化学试卷(解析版) 题型:选择题
甲、乙、丙、丁为中学常见物质,其中甲、乙为单质,丙为氧化物,它们之间存在如图所示的转化关系。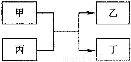 下列说法正确的是
下列说法正确的是
A.若甲、乙均为金属单质,则丁所属的物质类别一定是碱性氧化物
B. 若甲为金属单质,乙为非金属单质,则甲只能是Mg
C.若甲、乙元素是同主族元素,根据元素周期表推测,此时乙单质可能是Si
D.若甲、乙元素是同周期元素,则该反应的化学方程式一定为:2F2 + 2H2O=4HF + O2
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市名校联盟高三三诊理综化学试卷(解析版) 题型:填空题
(14分)湿法炼锌的冶炼过程可用下图简略表示:
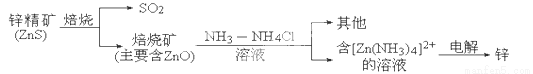
请回答下列问题:
(1)已知:N2(g)+2H2(g)===N2H4(l) ΔH=a kJ·mol-1,该反应不能自发进行,则a 0(填“>”、“<”或“=”).
(2)ZnS焙烧的反应2ZnS+3O2 2SO2+2ZnO所涉及的物质中,发生氧化反应的物质是 ,不含离子键的化合物是 .
2SO2+2ZnO所涉及的物质中,发生氧化反应的物质是 ,不含离子键的化合物是 .
(3)电解过程中析出锌的电极反应式为___________________________.
(4)产生的SO2可用Ba(NO3)2溶液吸收,部分产物可作为工业原料,其反应的离子方程式为 .
(5)锌-空气电池与锂电池相比,具有储存电量高、成本低、没有安全隐患等优点。该电池的总反应为2Zn+O2===2ZnO,电解质溶液为KOH溶液,则负极的电极反应式为 。25℃时,以该电池为电源,用两个等质量的铜棒作电极电解500 mL 0.1mol/L CuSO4溶液,一段时间后切断电源,对电极干燥并称量,测得两电极的质量差为9.6 g,则至少需要________L空气(折算成标准状况)进入该电池。
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市名校联盟高三三诊理综化学试卷(解析版) 题型:选择题
化学学习中,推理是一种重要的学习方法,下列推论正确的是
A.由“BF3和SO3互为等电子体”,可推知二者均为非极性分子
B.由“同主族元素性质相似,CO2为直线形分子”,可推知SiO2为直线形分子
C.由“SiH4的熔沸点比CH4高”,可推知PH3的熔沸点比NH3高
D.由“C、N、O三种元素的电负性C<N<O”,可推知第一电离能C<N<O
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市高三5月月考理综化学试卷(解析版) 题型:选择题
下列实验对应的结论正确的是:
| A | B | C | D |
装 置 |
|
|
|
|
结 论 | 实验室制取乙炔 | 能证明非金属性 Cl>C>Si | 分离出Cl2与KI溶 液反应生成的碘 | 白色沉淀是BaSO3 |
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市主城七区高三下学期第二次联考理综化学试卷(解析版) 题型:简答题
(16分)某药学杂志报道了一种具有明显抗癌活性的药物,其结构如图所示。J是其同分异构体,J的合成路线如下(部分产物已略去):
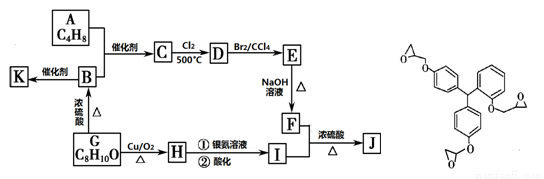
已知:① CH2=CHR1 + CH2=CHR2  CH2=CH2 + R1CH=CHR2
CH2=CH2 + R1CH=CHR2
② R—CH2—CH=CH2 + Cl2 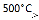 R—CHCl—CH=CH2 + HCl
R—CHCl—CH=CH2 + HCl
③ 核磁共振氢谱图显示A分子中不同环境氢原子个数比为3 :1;F是油脂水解的产物之一,能与水以任意比例混溶;K是一种高分子化合物。
请回答下列问题:
(1)该药物可能具有的性质是 (填字母编号)。
a.易溶于水 b.能发生加成反应 c.能发生水解反应 d.能发生取代反应
(2)H分子中含有官能团的名称是 ;G的结构简式为 。
(3)按照系统命名法,A的名称是 。
(4)C→D的反应类型为 。
(5)写出下列反应的化学方程式:
B→K ;F+I→J 。
(6)写出同时满足下列条件的I的所有同分异构体的结构简式 。
①分子中含有苯环结构;②能发生银镜反应;③苯环上的一氯代物有两种。
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆一中高二下学期期末考试化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.N2的电子式: B.氯化钠的分子式:NaCl
B.氯化钠的分子式:NaCl
C.S2-的结构示意图: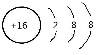 D. 乙烯的结构简式:C2H4
D. 乙烯的结构简式:C2H4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com