

���� ��1��SO42-��Ca2+��Mg2+�ȷֱ���BaCl2��Һ��Na2CO3��Һ��NaOH��Һ��Ӧ���ɳ���������ͨ�����˳�ȥ��Na2CO3��Һ�ܳ�ȥ������BaCl2��Һ�������ܳ�ȥ������Na2CO3��Һ��NaOH��Һ������Ӧ�ȼ�BaCl2��Һ�ټ�Na2CO3��Һ�����������ᣬ�ݴ˽��н��
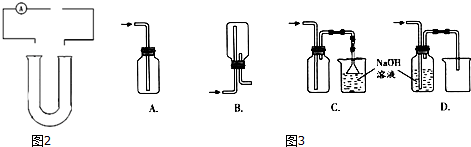
��2�����ݵ��ԭ������ⱥ��ʳ��ˮ�ķ�Ӧԭ����ͼ1����������Ȼ��д���缫��Ӧ���缫�ܷ�Ӧ����ʽ��
��3�������������������ʣ�������һ���ܶȴ��ڿ�����������ˮ���ж����壩��װ���ص���
����������ǿ�����ԣ�������������ʹ�������ɫ������ɫ��������ʪ�����ɫ��������������������Һ��ʪ��ĵ��۵⻯����ֽ�����������ݴ˽��н��
�������ܹ����������Ʒ�Ӧ�����Ȼ��ơ�������ƺ�ˮ���ݴ˿��Ƶ�Ư�۾���
��� �⣺��1��Ҫ�ȳ���������ӣ�Ȼ���ٳ������ӣ�Na2CO3���Գ�ȥ�����ı����ӣ���������ı����Ӳ�����ȫ���������ڼ�NaOH��ȥþ����˳�������ƣ��ɷ��ڼ���BaCl2֮ǰ��֮����Ϊ������NaOH��HCl�Ϳ��Ե����ˣ�ֻҪ������������ȫ��ȥ�����˼��ɣ�����HCl��ȥ����������������̼������ӣ���Ӧ�����ӷ���ʽΪ����������ȷ�IJ���˳��Ϊ��������BaCl2������NaOH������Na2CO3�����ˡ�����HCl�������BaCl2������Na2CO3������NaOH ���ˡ�����HCl��
�ʴ�Ϊ��AC�� H++OH-=H2O��2H++CO32-=H2O+CO2����
��2����ҵ���õ�ⱥ��ʳ��ˮ�ķ�����ȡ�ռ���������������缫Ϊ���Ե缫�����Դ����������Ϊ���������Դ����������Ϊ�������������У�����������ʧȥ������������������ˮ����������ӵõ����ӷ�����ԭ��Ӧ�����������缫��ӦʽΪ��2H++2e-=H2�����缫�ܷ�ӦΪ��2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$2NaOH+H2��+Cl2�����ݴ˽�ͼ��������Ϊ�� ��
��
�ʴ�Ϊ�� ��2H++2e-=H2������ԭ��Ӧ��2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$2NaOH+H2��+Cl2����
��2H++2e-=H2������ԭ��Ӧ��2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$2NaOH+H2��+Cl2����
��3����A��������λ����ȷ����Ϊ�����ȿ�����������������������ֻ�н����ڣ������ڣ����ų����壬��A����
B����װ���������ռ��ȿ���������壬���ռ���������Ҫ�̽���������B����
C��װ�ó����̳������ռ��ȿ����ص�����������ʣ��������ж���Ҫ������������Һ���գ�Ϊ��ֹ�������õ�����ˮ���©��������Ҫ��C��ȷ��
D������ͨ��NaOH��Һ�ᷢ����Ӧ�������������������գ������ռ�����������D����
�ʴ�Ϊ��C��
��A�������ڸ����ʯ����ֽ�ϲ��ᷢ����Ӧ��������ֽ�����ɫ�������飬��A����
B������Ҫ��ʪ��Ļ����²��ܷ�Ӧ����HClO��������ʹ��ɫ������ɫ���������ø������ɫ����������������B����
C����ʪ��ĵ��۵⻯���ԣ������ܹ��������������ɵⵥ�ʣ�ʹ��ֽ���������Լ�����������C��ȷ��
D��������ͨ����������Һ��������ˮ��Ӧ�����Ȼ���ʹ����ᣬ�Ȼ������������ӣ��ܹ�����������Һ��Ӧ�����Ȼ�����ɫ�������ݴ˿��Լ�����������D��ȷ��
�ʴ�Ϊ��CD��
���������������Ʒ�Ӧ�Ļ�ѧ����ʽΪ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��
�ʴ�Ϊ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��
���� ���⿼�������ʵķ������ᴿ�������Ļ�ѧ���ʼ���Ӧ�ã���Ŀ�Ѷ��еȣ����������ϴ��ۺ��Խ�ǿ��ע�����������Ļ�ѧ���ʣ���ֿ�����ѧ������ѧ֪ʶ�������������������������ѧ���ķ����������������Ӧ����ѧ֪ʶ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ������ | C�� | ����� | D�� | ǿ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ħ��������g | B�� | ���ʵ���Ũ�ȣ�L/mol | ||
| C�� | ���ʵ�����mol | D�� | ����Ħ�������L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | N2��NO��NO2���Ǵ�����Ⱦ���壬�ڿ����ж����ȶ����� | |
| B�� | ��AlCl3��Һ�еμӹ����İ�ˮ�ܿ����Ȳ�����ɫ������������ܽ� | |
| C�� | ����Ũ�������Ũ�����ȥ�����������ͭ�Ʋ� | |
| D�� | ��ϡ�����м���ͭ�ۣ�ͭ�۲��ܽ⣻�ټ���Cu��NO3��2���壬ͭ�۾ͻ��ܽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ƿ�����Ư���ͺ�������еĹ����� | |
| B�� | �ƺͼصĺϽ������ǹ��壬�����ڿ����ӷ�Ӧ�����Ƚ����� | |
| C�� | ̼�������DZ��Ƹ�����õķ��ͷ�֮һ��Ҳ������������θ����� | |
| D�� | �ȵ�̼������Һ����ȥ����Ʒ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| V��AgNO3��/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
| E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
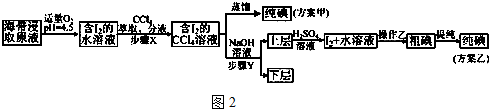
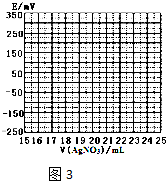
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��CN-����c��HCN�� | B�� | c��HCN��+c��CN-���T0.04 mol/L | ||
| C�� | c��OH-���Tc��H+��+c��HCN�� | D�� | c��Na+����c��CN-����c��H+����c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| Ca2+ | Mg2+ | Fe3+ | |
| ��ʼ����ʱ��pH | 11.9 | 9.1 | 1.9 |
| ��ȫ����ʱ��pH | 13.9 | 11.1 | 3.2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com