
(15分)(化学---选修物质结构与性质)Q、R、X、Y、Z五种元素的原子序数依次递增。已知:
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布msnmpn
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。
请回答下列问题:
(1)Z2+ 的核外电子排布式是 。
(2)在[Z(NH3)4]2+离子中,Z2+的空间轨道受NH3分子提供的 形成配位键。
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 。
A.稳定性:甲>乙,沸点:甲>乙 B.稳定性:甲>乙,沸点:甲<乙
C.稳定性:甲<乙,沸点:甲<乙 D.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小到大的顺序为 .(用元素符号作答)
(5)Q的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为 。
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于 。
(1)1s22s22p63s23p63d9(3分);(2) 孤对电子(孤电子对)(3分);(3)B (3分);
(4)Si < C <N (2分);(5) 3:2 (2分);(6)原子晶体(2分)。
【解析】
试题分析:根据题意可推知:Q是C;R是N;X是O;Y是Si;Z 是Cu。(1)Z2+ 的核外电子排布式是1s22s22p63s23p63d9;(2)在[Cu(NH3)4]2+离子中,Cu2+的空间轨道受NH3分子提供的孤对电子形成配位键。(3)Q与Y是同一主族的元素,由于元素的非金属性C>Si,所以形成的最简单气态氢化物分别为甲>乙,它们都是分子晶体,分子间作用力随温度的升高而增大,分子间作用力越大,物质的熔沸点就越高,所以放电乙>甲,因此选项是B;(4)Q、R、Y三种元素都是非金属的元素,一般情况下元素的非金属性越强,元素的原子序数越大,元素的第一电离能也就越大,但是由于N原子核外的电子处于该轨道的半充满的稳定状态,所以失去电子较难,所以电离能大于原子序数比其大1的O元素,因此这三种元素的第一电离能数值由小到大的顺序为Si < C <N;(5)Q的一种氢化物相对分子质量为26,则该分子是C2H2,其中分子中的σ键与π键的键数之比为3:2; (6)五种元素中,电负性最大的元素O与电负性最小的非金属元素Si这两种非金属元素形成的晶体SiO2,在原子间以共价键结合形成空间网状结构,属于原子晶体。
考点:考查元素的推断、物质稳定性和沸点的比较、元素的电离能大小比较、物质结构、晶体类型的知识。


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
常温下,下列溶液中的粒子浓度关系正确的是
A.NH4Cl溶液中:c(Cl-)=c(NH4+) >c(OH-)=c(H+)
B.Na2SO4溶液中:c(Na+)+ c(H+)=c(SO42-) + c(OH-)
C.NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)
D.浓度均为0.1mol·L-1CH3COOH与CH3COONa溶液等体积混合:2c(H+)-2c(OH-)=c (CH3COO-)-c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:选择题
对可逆反应4NH3(g)+ 5O2(g) 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是
A.达到化学平衡时,4υ正(O2)= 5υ逆(NO )
B.若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率增大,逆反应速率减少
D.化学反应速率关系是:2υ正(NH3)= 3υ正(H2O)
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市高三上学期9月质量检测化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W在元素周期表中的位置关系如图,下列推论合理的是

A.若Z的核电荷数是Y的两倍,则X为碳元素
B.若W的核电荷数是Y的两倍,则X是氮元素
C.原子半径:Z>Y>X
D.最简单氢化物的稳定性:Y>X>W
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市高三上学期9月质量检测化学试卷(解析版) 题型:选择题
下列物质中既存在共价键又离子键的是
A.Na2O2 B.MgCl2 C.SiO2 D.H2SO4
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市宁城县高三上学期摸底统一考试化学试卷(解析版) 题型:选择题
相同温度下,容积相同的甲、乙、丙3个恒容密闭容器中发生可逆反应:2SO2(g)+O2(g) 2SO3(g);
2SO3(g);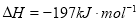 。实验测得起始、平衡时的有关数据如下表:
。实验测得起始、平衡时的有关数据如下表:
容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | |||
SO2 | O2 | SO3 | Ar | ||
甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2 |
丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
下列叙述正确的是 ( )
A.Q1=Q2=Q3=197 kJ
B.若在上述条件下反应生成2molSO3(s)的反应热为△H1,则△H1<-197 kJ·mol-1
C.甲、乙、丙3个容器中反应的平衡常数不相等
D.达到平衡时,丙容器中SO2的体积分数最大
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市宁城县高三上学期摸底统一考试化学试卷(解析版) 题型:选择题
常温下,下列溶液中可能大量共存的离子组是( )
A.加入金属镁能产生H2的溶液中: Na+、Fe3+、SO 、NO
、NO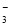
B.含有大量Fe2+的溶液中: K+、Mg2+、ClO-、SO
C.能使Al3+生成沉淀的溶液中: NH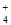 、Na+、SiO
、Na+、SiO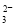 、HCO
、HCO
D.水电离产生的c(OH-)=1×10-10mol/L的溶液中: Al3+、SO 、NO
、NO 、Cl-
、Cl-
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古巴彦淖尔市高三10月月考化学试卷(解析版) 题型:选择题
下列现象或事实可用同一原理解释的是
A.浓硫酸和浓盐酸长期暴露在空气中浓度降低
B.铁在冷的浓硫酸中和铝在冷的浓硝酸中都没有明显变化
C.SO2、漂白粉、活性炭、过氧化钠都能使红墨水褪色
D.漂白粉和水玻璃长期暴露在空气中变质
查看答案和解析>>
科目:高中化学 来源:2014~2015江苏省高一上学期期中化学试卷(解析版) 题型:填空题
完成下列反应方程式(每空1分,共计3分)
(1)铁在氯气中燃烧:
(2)用氢氧化钠来吸收氯气尾气
(3)漂白粉的漂白原理:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com