

·ÖĪö £Ø1£©¢ŁĶŗĶÅØĮņĖį¼ÓČČ·“Ӧɜ³ÉĮņĖįĶ”¢¶žŃõ»ÆĮņŗĶĖ®£»
¢ŚŅĄ¾ŻĮ÷³ĢĶ¼·ÖĪöÅŠ¶Ļ£¬Ļ”ĮņĖį”¢ĶŗĶŃõ»ÆĢś·“Ó¦ŹĒŃõ»ÆĢśŗĶĻ”ĮņĖį·“Ӧɜ³ÉĮņĖįĢśŗĶĖ®£¬ĮņĖįĢśŗĶĶ·“Ӧɜ³ÉĀČ»ÆŃĒĢśŗĶĀČ»ÆĶ£»ĶØČėČȵÄæÕĘųŹĒĪŖĮĖŃõ»ÆŃĒĢśĄė×ÓĪŖČż¼ŪĢśĄė×Ó£¬µ÷ÕūČÜŅŗPH³żČ„ĢśĄė×Ó£»ČÜŅŗÖŠµĆµ½ČÜÖŹ¹ĢĢåµÄ·½·ØŹĒÕō·¢Ė®½į¾§Īö³ö£»
£Ø2£©¢ŁĪüŹÕĮņĖį¹¤ŅµĪ²ĘųÖŠµÄ¶žŃõ»ÆĮņ£¬Ķ¬Ź±ÖʵĆĮņĖįļ§£¬ĪüŹÕĖžÖŠĶØČėæÕĘųŹĒĄūÓĆŃõĘųŃõ»Æ¶žŃõ»ÆĮņĪŖĮņĖįŃĪ£»
¢Ś¼ģŃéļ§øłĄė×Ó£¬æɼÓČė¼ī²¢¼ÓČČ£¬Éś³É°±Ęų£¬ÓĆ¼ģŃé°±ĘųµÄ·½·Ø¼ģŃ飮
½ā“š ½ā£ŗ£Ø1£©¢ŁĶŗĶÅØĮņĖį¼ÓČČ·“Ӧɜ³ÉĮņĖįĶ”¢¶žŃõ»ÆĮņŗĶĖ®£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCu+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$CuSO4+SO2”ü+2H2O£¬
¹Ź“š°øĪŖ£ŗCu+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$CuSO4+SO2”ü+2H2O£»
¢ŚŅĄ¾ŻĮ÷³Ģ×Ŗ»ÆĶ¼·ÖĪö£¬ĶŠčŅŖĮņĖįŗĶŃõ»ÆĢś·“Ӧɜ³ÉµÄĢśĄė×ÓČܽāÉś³ÉĶĄė×Ó£¬ŌŁĶØČėæÕĘųŃõ»ÆŃĒĢśĄė×ÓĪŖĢśĄė×Ó£¬µ÷½ŚČÜŅŗPHŹ¹ĢśĄė×Ó³Įµķ³żČ„£¬µĆµ½ĮņĖįĶČÜŅŗ£»¼ÓČČÕō·¢ÅØĖõ½į¾§µĆµ½ĮņĖįĶ¾§Ģ壻·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗFe2O3+6H+ØT2Fe3++3H2O”¢2Fe3++CuØT2Fe2++Cu2+£Ø»ņFe2O3+Cu+6H+ØT3H2O+2Fe2++Cu2+£©£»ĶØČėæÕĘųµÄ×÷ÓĆŹĒŃõĘųŃõ»ÆŃĒĢśĄė×ÓĪŖĢśĄė×ӵķ“Ó¦£¬·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖ£ŗ4Fe2++4H++O2ØT4Fe3++2H2O£»·ÖĄėĄ¶É«ĀĖŅŗŗĶŗģŗÖÉ«³ĮµķµÄŹµŃé²Ł×÷ŹĒ¹żĀĖ£¬
¹Ź“š°øĪŖ£ŗFe2O3+6H+ØT2Fe3++3H2O£»2Fe3++CuØT2Fe2++Cu2+£»4Fe2++4H++O2ØT4Fe3++2H2O£»¹żĀĖ£»
£Ø2£©¢ŁŅĄ¾ŻĮ÷³ĢĶ¼·ÖĪö£¬ĪüŹÕĖžÖŠ·¢Éś·“Ó¦ŹĒ¶žŃõ»ÆĮņ”¢Ņ»Ė®ŗĻŃõĘų·“Ӧɜ³ÉĮņĖįļ§ŗĶĖ®£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ4NH3?H2O+2SO2+O2ØT2£ØNH4£©2SO4+2H2O£»
¹Ź“š°øĪŖ£ŗ4NH3?H2O+2SO2+O2ØT2£ØNH4£©2SO4+2H2O£»
¢Ś¼ģŃéļ§øłĄė×Ó£¬æɼÓČė¼ī²¢¼ÓČČ£¬Éś³É°±Ęų£¬ÓĆ¼ģŃé°±ĘųµÄ·½·Ø¼ģŃ飬Éę¼°µ½µÄĄė×Ó·½³ĢŹ½ĪŖNH4++OH-$\frac{\underline{\;\;”÷\;\;}}{\;}$NH3”ü+H2O£¬
¹Ź“š°øĪŖ£ŗNH4++OH-$\frac{\underline{\;\;”÷\;\;}}{\;}$NH3”ü+H2O£®
µćĘĄ ±¾Ģāæ¼²éĮĖÖʱø·½°øµÄÉč¼Ę£¬ĢāÄæÄѶČÖŠµČ£¬øł¾ŻÖʱøĮ÷³ĢĆ÷Č·ÖʱøŌĄķĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕÖʱø·½°øÉč¼ĘÓėĘĄ¼ŪµÄŌŌņ£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪöÄÜĮ¦¼°»ÆѧŹµŃéÄÜĮ¦£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+”¢Ca2+”¢Cl-”¢SO42- | B£® | Fe2+”¢H+”¢SO32-”¢ClO- | ||
| C£® | K+”¢NO3-”¢Fe2+”¢H+ | D£® | Mg2+”¢NH4+”¢Cl-”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū | B£® | ¢Ś¢Ū¢Ü | C£® | ¢Ū¢Ü¢Ż | D£® | ¢Ś¢Ū¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
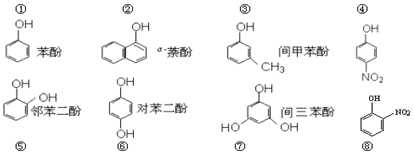
| A£® | ÄÜŠĪ³É·Ö×ÓÄŚĒā¼üµÄÓŠ¢Ż¢ą¢į | |
| B£® | ÄÜŠĪ³É·Ö×Ó¼äĒā¼üÓŠ¢Ł¢Ś¢Ū¢Ü¢Ž¢ß¢ā | |
| C£® | øł¾ŻĒā¼üŠĪ³ÉµÄĢõ¼ž£¬æÉŅŌĶĘ²ā»¹ÓŠŌŖĖŲLiµÄŌ×ÓæÉŅŌ“śĢęĒāŌ×Ó¶ųŠĪ³ÉĄąĖĘĒā¼üµÄ½į¹¹ | |
| D£® | C2H6O·Ö×ÓÖŠĶ¬Ź±“ęŌŚ¼«ŠŌ¼ü”¢·Ē¼«ŠŌ¼üŗĶĒā¼ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | XæÉŅŌŹĒµķ·Ū»ņĻĖĪ¬ĖŲ | |
| B£® | Y”śŅŅČ©ŹōÓŚĻūČ„·“Ó¦ | |
| C£® | YÓėCH3OCH3ŹĒĶ¬·ÖŅģ¹¹Ģå | |
| D£® | ĄūÓĆFeCl3ČÜŅŗ¼ų±š±½·ÓČÜŅŗŗĶYČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉųĪöŹµŃéæÉŅŌ¼ų±š½ŗĢåŗĶČÜŅŗ | |
| B£® | ÓÉ·Ö×Ó×é³ÉµÄĪļÖŹÖŠŅ»¶Ø“ęŌŚ¹²¼Ū¼ü | |
| C£® | Ė®µÄµēĄėŹĒĪüČČ¹ż³Ģ£¬ÉżøßĪĀ¶Č£¬Ė®µÄĄė×Ó»żŌö“ó”¢pH¼õŠ” | |
| D£® | ÓĆ½šŹō»ī¶ÆŠŌĖ³ŠņæɽāŹĶ·“Ó¦£ŗNa£Øl£©+KCl£Øl£©ØTNaCl£Øl£©+K£Øg£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2 L ·ś»ÆĒāĘųĢå·Ö½ā³É 1 L ĒāĘųÓė 1 L·śĘųĪüŹÕ 270 kJČČĮæ | |
| B£® | 1 molĒāĘųÓė 1 mol·śĘų·“Ӧɜ³É 2 molŅŗĢ¬·ś»ÆĒā·Å³öµÄČČĮæŠ”ÓŚ 270 kJ | |
| C£® | ŌŚĻąĶ¬Ģõ¼žĻĀ£¬1 molH2Óė 1 molF2µÄÄÜĮæ×ÜŗĶ“óÓŚ 2 molHF ĘųĢåµÄÄÜĮæ | |
| D£® | 1øöĒāĘų·Ö×ÓÓė 1 øö·śĘų·Ö×Ó·“Ӧɜ³É 2 øö·ś»ÆĒāĘųĢå·Ö×ӷųö 270 kJČČĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | -688.3 kJ/mol | B£® | -488.3 kJ/mol | C£® | -191 kJ/mol | D£® | +488.3 kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com