
| A. | 食盐 | B. | 山梨酸钾 | C. | 柠檬黄 | D. | 味精 |
分析 食品防腐剂是指保持食品原有的质量和食品营养价值为目的食品添加剂,它能抑制微生物的生长和繁殖;调味剂是指改善食品的感官性质,使食品更加美味可口,并能促进消化液的分泌和增进食欲的食品添加剂,可以做防腐剂的有:亚硝酸钠、食盐;可以做调味剂的有:食盐、味精,既可以做防腐剂,又可以做调味剂的是食盐.
A.氯化钠具有咸味,用食盐腌制食品可以防止食品腐烂变质;
B.山梨酸钾是常用的食品防腐剂;
C.柠檬酸黄为着色剂,不是调味剂;
D.味精不可以做防腐剂.
解答 解:A.食盐是一种常用的咸味调味剂,用食盐腌制食品可以防止食品腐烂变质,所以食盐是一种食品防腐剂,故A正确;
B.山梨酸钾是常用的食品防腐剂,有防止变质发酸、延长保质期的效果,在世界各国均被广泛使用,不可以做调味剂,故B错误;
C.柠檬酸黄外观为橙黄色粉末,可添加于饮料等食品,是用量有严格限制的染色剂,不是防腐剂,故C错误;
D.味精是应用很广的调味剂,但不是化学防腐剂,故D错误;
故选A.
点评 本题考查了常见食品添加剂的性质和作用,完成此题,可以依据物质的性质进行,平时注意知识的积累,题目较简单.


科目:高中化学 来源: 题型:多选题
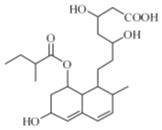
| A. | 能与FeCl3 溶液发生显色反应 | |
| B. | 能使酸性KMnO4 溶液褪色 | |
| C. | 能发生加成、取代、消去反应 | |
| D. | 1mol该物质最多可消耗4molNaOH、2molBr2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标况下,22.4LSO3和22.4LC2H4原子个数比为2:3 | |
| B. | 将78gNa2O2与过量CO2反应转移的电子数为2NA | |
| C. | 28g乙烯分子中含有极性共价键的数目为6NA | |
| D. | 1molNaCl晶体中含有NA个Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
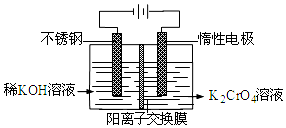
| A. | 在阴极式,发生的电极反应为:2H2O+2e-═2OH-+H2↑ | |
| B. | 在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+?Cr2O72-+H2O向右移动 | |
| C. | 该制备过程总反应的化学方程式为:4K2CrO4+4H2O$\frac{\underline{\;电解\;}}{\;}$2K2Cr2O7+4KOH+2H2↑+O2↑ | |
| D. | 铬原子的价电子排布式为3d44S2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称取53.0g Na2CO3固体 | |
| B. | 需要的玻璃仪器有500mL容量瓶、烧杯、玻璃棒、胶头滴管、量筒 | |
| C. | 转移溶液时有少量液体溅出,则最终溶液的浓度偏高 | |
| D. | 定容时仰视刻度线,则最终溶液的浓度偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在相同条件下,pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度不相同 | |
| B. | 反应NH3(g)+HCl(g)?NH4Cl(s)能自发进行,则该反应△H<0 | |
| C. | 锌与稀硫酸反应时加入少量硫酸铜,反应加快的主要原因是Cu2+水解增大了 c(H+) | |
| D. | 一定条件下,反应2SO2(g)+O2(g)?2SO3(g)△H<0达到平衡后,升高体系温度,应重新达到平衡前,有v正(O2)>2v逆(SO2) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com