
C”¢N”¢S¶¼ŹĒÖŲŅŖµÄ·Ē½šŹōŌŖĖŲ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø£©
A£® ČżÕ߶ŌÓ¦µÄŃõ»ÆĪļ¾łĪŖĖįŠŌŃõ»ÆĪļ
B£® ČżÕߵĵ„ÖŹÖ±½ÓÓėŃõĘų·“Ó¦¶¼ÄÜÖĮÉŁÉś³ÉĮ½ÖÖŃõ»ÆĪļ
C£® ĻąĶ¬ĪĀ¶ČĻĀ£¬µČĪļÖŹµÄĮæÅØ¶ČµÄNa 2CO3”¢NaNO3”¢Na2SO3ČÜŅŗµÄpH“óŠ”Ė³Šņ£ŗNaNO3£¼Na2S03£¼Na2CO3
2CO3”¢NaNO3”¢Na2SO3ČÜŅŗµÄpH“óŠ”Ė³Šņ£ŗNaNO3£¼Na2S03£¼Na2CO3
D£® CO2”¢NO2”¢SO2¶¼ÄÜÓėH2O·“Ó¦£¬Ęä·“Ó¦ŌĄķĻąĶ¬
æ¼µć£ŗ µŖµÄŃõ»ÆĪļµÄŠŌÖŹ¼°Ęä¶Ō»·¾³µÄÓ°Ļģ£»ŃĪĄąĖ®½āµÄÓ¦ÓĆ£»¶žŃõ»ÆĮņµÄ»ÆѧŠŌÖŹ£»Ģ¼×åŌŖĖŲ¼ņ½é£®
×ØĢā£ŗ ŃĪĄąµÄĖ®½ā×ØĢā£»Ńõ×åŌŖĖŲ£»µŖ×åŌŖĖŲ£»Ģ¼×åŌŖĖŲ£®
·ÖĪö£ŗ A£®ÄÜŗĶ¼ī·“Ӧɜ³ÉŃĪŗĶĖ®µÄŃõ»ÆĪļŹĒĖįŠŌŃõ»ÆĪļ£¬×¢Ņā²¢²»ŹĒĖłÓŠµÄ·Ē½šŹōŃõ»ÆĪļ¶¼ŹĒĖįŠŌŃõ»ÆĪļ£»
B£®ĮņŗĶŃõĘų·“Ӧֻɜ³É¶žŃõ»ÆĮņ£»
C£®ĻąĶ¬ĪĀ¶ČĻĀ£¬µČĪļÖŹµÄĮæÅØ¶ČµÄÄĘŃĪ£¬ĖįøłĄė×Ó¶ŌÓ¦µÄĖįŌ½Čõ£¬ĘäÄĘŃĪµÄpHŌ½“ó£»
D£®¶žŃõ»ÆµŖŗĶĖ®·¢ÉśŃõ»Æ»¹Ō·“Ó¦£®
½ā“š£ŗ ½ā£ŗA£®NO”¢CO¶¼²»ŹōÓŚĖįŠŌŃõ»ÆĪļ£¬ŹĒ²»³ÉŃĪŃõ»ÆĪļ£¬¹ŹA“ķĪó£»
B£®ĮņŗĶŃõĘų·“Ӧֻɜ³É¶žŃõ»ÆĮņ£¬¶žŃõ»ÆĮņ±»Ńõ»ÆÉś³ÉČżŃõ»ÆĮņŹ±±ŲŠėÓŠ“߻ƼĮŗĶ¼ÓČČĢõ¼ž£¬¹ŹB“ķĪó£»
C£®ĻąĶ¬ĪĀ¶ČŗĶĻąĶ¬ĪļÖŹµÄĮæÅØ¶ČµÄNa2CO3”¢NaNO3”¢Na2SO3ČÜŅŗÖŠ£¬ŅņĪŖĖįøłĄė×ÓµÄĖ®½ā³Ģ¶Č£ŗĢ¼ĖįøłĄė×Ó£¾ŃĒĮņĖįøłĄė×Ó£¬ĻõĖįøłĄė×Ó²»Ė®½ā£¬ĖłŅŌČÜŅŗµÄpH“óŠ”Ė³Šņ£ŗNaNO3£¼Na2S03£¼Na2CO3£¬¹ŹCÕżČ·£»
D£®¶žŃõ»ÆµŖŗĶĖ®µÄ·“Ó¦ŹōÓŚŃõ»Æ»¹Ō·“Ó¦£¬¶žŃõ»ÆĢ¼”¢¶žŃõ»ÆĮņŗĶĖ®µÄ·“Ó¦ŹōÓŚ»ÆŗĻ·“Ó¦£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ£ŗ ±¾Ģāæ¼²éĖįŠŌŃõ»ÆĪļµÄÅŠ¶Ļ”¢ŃĪĄąµÄĖ®½āµČÖŖŹ¶µć£¬ŅדķŃ”ĻīŹĒB£¬×¢ŅāĮņÓėŃõĘųÖ±½Ó·“Ó¦£¬ĪŽĀŪŃõĘųŹĒ·ń¹żĮæ¶¼Ö»Éś³É¶žŃõ»ÆĮņ£¬ĪŖŅדķµć£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ģå»żĻąĶ¬µÄ¼×£®ŅŅĮ½øöČŻĘ÷ÖŠ£¬·Ö±š¶¼³äÓŠµČĪļÖŹµÄĮæµÄSO2ŗĶO2£¬ŌŚĻąĶ¬ĪĀ¶ČĻĀ·¢Éś·“Ó¦£ŗ2SO2+O2⇌2SO3£¬²¢“ļµ½Ę½ŗā£®ŌŚÕā¹ż³ĢÖŠ£¬¼×ČŻĘ÷±£³ÖĢå»ż²»±ä£¬ŅŅČŻĘ÷±£³ÖŃ¹Ēæ²»±ä£¬Čō¼×ČŻĘ÷ÖŠSO2µÄ×Ŗ»ÆĀŹĪŖp%£¬ŌņŅŅČŻĘ÷ÖŠSO2µÄ×Ŗ»ÆĀŹ£Ø£©
A £® µČÓŚp% B£® “óÓŚp% C£® Š”ÓŚp% D£® ĪŽ·ØÅŠ¶Ļ
£® µČÓŚp% B£® “óÓŚp% C£® Š”ÓŚp% D£® ĪŽ·ØÅŠ¶Ļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ė®ŹĒÉśĆüÖ®Ō“£¬Ņ²ŹĒÖŲŅŖµÄ»·¾³ŅŖĖŲÖ®Ņ»”£
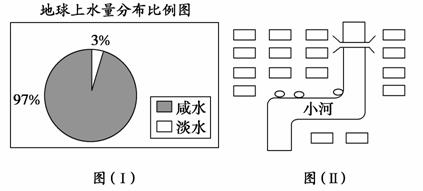
(1)¹Ū²ģĻĀĶ¼(¢ń)£¬ČōÓĆ1 LĖ®Ą““ś±ķµŲĒņÉĻµÄ×ÜĖ®Į棬ŅŖ±Č½Ļ¾«Č·µŲĮæČ”µŲ
ĒņÉĻµÄµĖ®Įæ£¬Ó¦Ń”ŌńµÄŅĒĘ÷ŹĒ__________”£
A£®100 mLÉÕ± B£®50 mLÉÕ±
C£®100 mLĮæĶ² D£®50 mLĮæĶ²
(2)Ķ¼(¢ņ)ŹĒij¾ÓĆńŠ”ĒųÖŠĄ¬»ųŹÕ¼Æµć(Š”Ȧ)µÄ²¼¾Ö£¬ĖüŌŚŃ”Ö·ÉĻ“ęŌŚµÄĪŹĢāÓŠ
________£»Ą¬»ųŹÕ¼ÆµćєַӦæ¼ĀĒµÄŅņĖŲ°üĄØ__________________________
_________________________________________________________________ӣ
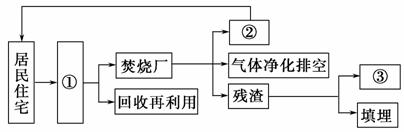
(3)ÓŠČĖÉčĻėŌŚ×”Õ¬Š”Ēųø½½ü½ØĮ¢Š”ŠĶÉś»īĄ¬»ų·ŁÉÕ³§£¬ĘäĮ÷³ĢČēĶ¼(¢ó)”£Ēė
½«Ķ¼(¢ó)ÖŠ¢Ł¢Ś¢ŪĖłŅŖ±ķ“ļµÄÄŚČŻĢīŌŚĻĀĆęµÄŗįĻßÉĻ”£
Ķ¼(¢ó)
¢Ł______________________________________________________________£»
¢Ś______________________________________________________________£»
¢Ū______________________________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖQÓėRµÄĦ¶ūÖŹĮæÖ®±ČĪŖ9£ŗ22£¬ŌŚ·“Ó¦X+2Y═2Q+RÖŠ£¬µ±1.6g XÓėYĶźČ«·“Ó¦ŗó£¬Éś³É4.4g R£¬Ōņ²ĪÓė·“Ó¦µÄYŗĶÉś³ÉĪļQµÄÖŹĮæ Ö®±ČĪŖ£Ø£©
Ö®±ČĪŖ£Ø£©
A£® 46£ŗ9 B£® 32£ŗ9 C£® 23£ŗ9 D£® 16£ŗ9
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
50mL 4mol•L﹣1µÄNaOHČÜŅŗĆܶČĪŖ1.6g•cm﹣3£¬Ōņ
£Ø1£©“ĖČÜŅŗµÄÖŹĮæ·ÖŹżŹĒ £®
£Ø2£©“ĖČÜŅŗ¼ÓĖ®Ļ”ŹĶÖĮ500mL£¬ŌŁČ”³ö50mL£¬Ōņ“Ė50mLČÜŅŗµÄĪļÖŹµÄĮæÅØ¶Č±äŹĒ Ėłŗ¬ČÜÖŹµÄÖŹĮæŹĒ g£®
£Ø3£©“ĖČÜŅŗÄÜĪüŹÕ±ź×¼×“æöĻĀµÄCl2µÄĢå»żŹĒ £¬Éś³ÉNaClµÄÖŹĮæŹĒ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
·ÖĄą·ØŌŚ»ÆѧѧæĘ·¢Õ¹ÖŠĘšµ½ĮĖ·Ē³£ÖŲŅŖµÄ×÷ÓĆ£¬ĻĀĮŠ·ÖĄąŅĄ¾ŻŗĻĄķµÄŹĒ£Ø£©
¢Łøł¾ŻŃõ»ÆĪļµÄŠŌÖŹ½«Ńõ»ÆĪļ·Ö³ÉĖįŠŌŃõ»ÆĪļ”¢¼īŠŌŃõ»ÆĪļŗĶĮ½ŠŌŃõ»ÆĪļµČ
¢Śøł¾Ż·“Ó¦ÖŠŹĒ·ńÓŠµē×Ó×ŖŅĘ½«»Æѧ·“Ó¦·ÖĪŖŃõ»Æ»¹Ō·“Ó¦ŗĶ·ĒŃõ»Æ»¹Ō·“Ó¦
¢Ūøł¾Ż·ÖÉ¢ĻµŹĒ·ńÓŠ¶”“ļ¶ūĻÖĻó·ÖĪŖČÜŅŗ”¢½ŗĢåŗĶ×ĒŅŗ
¢Üøł¾Ż×é³ÉŌŖĖŲµÄÖÖĄą½«“æ¾»Īļ·ÖĪŖµ„ÖŹŗĶ»ÆŗĻĪļ
¢Żøł¾Żµē½āÖŹµÄĖ®ČÜŅŗµ¼µēÄÜĮ¦µÄĒæČõ½«µē½āÖŹ·ÖĪŖĒæµē½āÖŹŗĶČõµē½āÖŹ£®
A£® ¢Ś¢Ü B£® ¢Ś¢Ū¢Ü C£® ¢Ł¢Ū¢Ż D£® ¢Ł¢Ś¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½ųŠŠ»ÆѧŹµŃ飬¹Ū²ģŹµŃéĻÖĻó£¬Ķعż·ÖĪöĶĘĄķµĆ³öÕżČ·µÄ½įĀŪŹĒ»ÆѧѧĻ°µÄ·½·ØÖ®Ņ»£®¶ŌĻĀĮŠŹµŃéŹĀŹµµÄ½āŹĶ“ķĪóµÄŹĒ£Ø£©
ĻÖĻó ½āŹĶ»ņ½įĀŪ
A SO2Ź¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ« SO2±ķĻÖ»¹ŌŠŌ
B ÅØĻõĖįŌŚ¹āÕÕĢõ¼žĻĀ±ä»Ę ÅØĻõĖį²»ĪČ¶Ø£¬Éś³ÉÓŠÉ«ĪļÖŹÉś³ÉĒŅÄÜČÜÓŚÅØĻõĖį
C ijČÜŅŗÖŠ¼ÓČėÅØNaOHČÜŅŗ¼ÓČČ£¬·Å³öĘųĢåÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶ øĆČÜŅŗÖŠŅ»¶Øŗ¬ÓŠNH4+
D ½«Ķʬ·ÅČėÅØĮņĖįÖŠ£¬ĪŽĆ÷ĻŌŹµŃéĻÖĻó ĶŌŚĄäµÄÅØĮņĖįÖŠ·¢ Éś¶Ū»Æ
A£® A B£® B C£® C D£® D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½±ķŹ¾ÕżČ·µÄŹĒ£Ø£©
A£® ³ĪĒåŹÆ»ŅĖ®ÖŠĶØČė¹żĮ涞Ńõ»ÆĢ¼£ŗOH﹣+CO2═HCO3﹣
B£® ĶʬøśČżĀČ»ÆĢśČÜŅŗ·“Ó¦£ŗFe3++Cu═Cu2++Fe2+
C£® ĘÆ°×·ŪČÜŅŗÖŠĶØČėÉŁĮæSO2£ŗCa2++2ClO﹣+SO2+H2O═CaSO3”ż+2HClO
D£® Fe3O4ÓėĻ”HNO3·“Ó¦£ŗFe3O4+8H+═Fe2++2Fe3++4H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠŹµŃé²Ł×÷¾łŅŖÓĆ²£Į§°ō£¬ĘäÖŠ²£Į§°ōÓĆ×÷ŅżĮ÷µÄŹĒ£Ø£©
¢Ł¹żĀĖ ¢ŚÕō·¢ ¢ŪČܽā ¢ÜĻņČŻĮæĘæ×ŖŅĘŅŗĢ壮
A£® ¢ŁŗĶ¢Ś B£® ¢ŁŗĶ¢Ū C£® ¢ŪŗĶ¢Ü D£® ¢ŁŗĶ¢Ü
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com