
【题目】我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染.PETG的结构简式如下:

这种材料可采用下图所示的合成路线;

已知;(1)![]()
(2)![]() (R、
(R、![]() 、
、![]() 表示烃基)
表示烃基)
请回答下列问题:
(1)⑦的反应类型是_____________,试剂X为_____________.
(2)写出Ⅰ的结构简式:____________
(3)合成时应控制的单体的物质的量:![]() _____________(用m,n表示).
_____________(用m,n表示).
(4)写出反应②的化学方程式:____________________________________.
(5)与E的分子式相同,且满足下列条件的同分异构体有_____________种.
①能与![]() 溶液反应产生
溶液反应产生![]() ②能发生银镜反应 ③遇
②能发生银镜反应 ③遇![]() 溶液显紫色
溶液显紫色
(6)D和E在催化剂作用下可生产一种聚酯纤维——涤纶,请写出生产该物质的化学方程式:__________
【答案】取代反应 NaOH水溶液 ![]() m:(m+n):n BrCH2CH2Br+2NaOH
m:(m+n):n BrCH2CH2Br+2NaOH![]() HOCH2CH2OH+2NaBr 10
HOCH2CH2OH+2NaBr 10 ![]()
![]()
【解析】
由PETG的结构可知它是由HOCH2CH2OH与![]() 和
和![]() 发生酯化反应得到的,再由转化关系可推知烃A是CH2=CH2,C是CH2=CH2与Br2发生加成反应得到的BrCH2CH2Br,BrCH2CH2Br在碱性溶液、加热条件下发生水解反应生成D:HOCH2CH2OH,B被酸性KMnO4溶液氧化得到酸(E),再由B最终转化为H的过程中碳原子数不变可推知B是
发生酯化反应得到的,再由转化关系可推知烃A是CH2=CH2,C是CH2=CH2与Br2发生加成反应得到的BrCH2CH2Br,BrCH2CH2Br在碱性溶液、加热条件下发生水解反应生成D:HOCH2CH2OH,B被酸性KMnO4溶液氧化得到酸(E),再由B最终转化为H的过程中碳原子数不变可推知B是![]() ,则E是
,则E是![]() ,
,![]() 分子中甲基上的氢在光照条件下与Cl2发生取代反应生成F:
分子中甲基上的氢在光照条件下与Cl2发生取代反应生成F:![]() 在碱性溶液、加热条件下发生水解反应生成G:
在碱性溶液、加热条件下发生水解反应生成G:![]() ,
,![]() 与H2发生加成反应生成H:
与H2发生加成反应生成H:![]() ,
,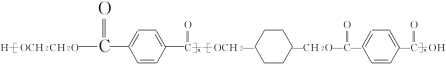 与CH3OH发生取代反应再生得到D:HOCH2CH2OH、H:
与CH3OH发生取代反应再生得到D:HOCH2CH2OH、H:![]() 和I:
和I:![]() ;据此判断。
;据此判断。
(1)PETG和甲醇反应生成D、I和H的反应属于取代反应;通过以上分析知,卤代烃在氢氧化钠的水溶液中能生成醇,所以X是NaOH溶液;
(2)Ⅰ的结构简式为:![]() ;
;
(3)由结构可知1 mol PETG由m mol D、(m+n) mol E、n mol H发生缩聚反应得到,合成时应控制的单体的物质的量:n(D):n(E):n(H)=m:(m+n):n;
(4)反应②为BrCHspan>2CH2Br在氢氧化钠的水溶液中加热反应生成乙二醇和溴化钠,反应的化学方程式为:BrCH2CH2Br+2NaOH![]() HOCH2CH2OH+2NaBr;
HOCH2CH2OH+2NaBr;
(5)能与NaHCO3溶液反应生成CO2说明含有羧基,能发生银镜反应说明含有醛基,遇FeCl3溶液显紫色说明含有酚羟基,再由E的结构可知符合条件的苯环上正好有三个独立的基团:—COOH、—CHO、—OH,当—COOH和—CHO位于邻位和间位时,—OH都分别有4种不同的位置,当—COOH和—CHO位于对位时,—OH有2种不同的位置,所以符合条件的同分异构体数目共有10种;
(6)![]() 可以与HOCH2CH2OH发生缩聚反应生成高分子:
可以与HOCH2CH2OH发生缩聚反应生成高分子: ,反应的方程式为
,反应的方程式为![]()
![]() 。
。


 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】现有硫酸铁、硫酸亚铁和硫酸混合溶液200mL,现将其分成两等份,往其中一份中滴加足量BaCl2溶液,产生25.63g白色沉淀,往另一份中投入足量铁片,放出1.12L气体(标准状况)。下列判断错误的是( )
A.原溶液中离子有3c(Fe3+)+c(H+)+2c(Fe2+)=2c(SO42-)+c(OH-)
B.原混合液中c(Fe3+)可能为0.1molL-1
C.原混合液中c(H+)=0.5molL-1
D.溶解的铁最多不超过3.92g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下不能实现的是
①S![]() SO3
SO3![]() H2SO4
H2SO4
②N2![]() NO
NO![]() NO2
NO2![]() HNO3
HNO3
③MgCl(aq)![]() 无水MgCl2
无水MgCl2![]() Mg
Mg
④Fe![]() Fe2O3
Fe2O3![]() Fe2(SO4)3
Fe2(SO4)3
⑤铝土矿![]() NaAlO2溶液
NaAlO2溶液![]() Al(OH)2
Al(OH)2![]() Al2O2
Al2O2![]() Al
Al
A.①③⑤
B.②③④
C.③④⑤
D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,装置Ⅰ为新型电池,放电时B电极的反应式为NaBr3+2Na++2e-=3NaBr,装置Ⅱ为铅蓄电池。首先闭合K1和K2,当铅蓄电池充电结束后,断开K1,闭合K2。下列说法正确的是

A.装置Ⅰ放电时的A电极反应式为2Na2S2-2e-=Na2S4+2Na+
B.闭合K1、K2时,每有0.1molNa+通过离子交换膜,装置Ⅱ溶液中有0.1mol电子转移
C.断开K1、闭合K2时,b电极的电极反应式为PbO2+2e-+SO42-+4H+=PbSO4+2H2O
D.断开K1、闭合K2时,装置Ⅱ中SO42-向a电极迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为元素周期表中前四周期元素,且原子序数依次增大.W的基态原子中占据哑铃形原子轨道的电子数为3,![]() 与
与![]() 具有相同的电子层结构;W与X的最外层电子数之和等于Y的最外层电子数;Z元素位于元素周期表的第11列.请回答:
具有相同的电子层结构;W与X的最外层电子数之和等于Y的最外层电子数;Z元素位于元素周期表的第11列.请回答:
(1)Z的基态原子M层的电子排布式为____________________.
(2)W的简单氢化物分子中W原子的__________轨道与氢原子的__________轨道重叠形成![]() 键.(填轨道名称)
键.(填轨道名称)
(3)比较Y的含氧酸的酸性:![]() __________
__________![]() (填“>”或“<”),原因为___________________.
(填“>”或“<”),原因为___________________.
(4)关于Z的化合物![]() (EDTA的结构简式如下图)的说法正确的是_____选项字母).
(EDTA的结构简式如下图)的说法正确的是_____选项字母).
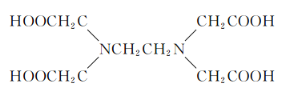
A.![]() 中所含的化学键有离子键、共价键、配位键和氢键
中所含的化学键有离子键、共价键、配位键和氢键
B.EDTA中碳原子的杂化轨道类型为![]() 、
、![]()
C.![]() 的组成元素的第一电离能顺序为
的组成元素的第一电离能顺序为![]()
D.![]() 与
与![]() 互为等电子体,空间构型均为正四面体形
互为等电子体,空间构型均为正四面体形
(5)某离子型氢化物![]() 的晶胞结构如图所示:
的晶胞结构如图所示:
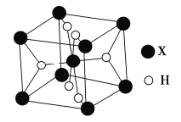
①![]() 的配位数为__________________.
的配位数为__________________.
②![]() 是一种储氢材料,遇水会缓慢反应,该反应的化学方程式为____________.
是一种储氢材料,遇水会缓慢反应,该反应的化学方程式为____________.
③若该晶胞的密度为![]() ,则晶胞的体积为______________
,则晶胞的体积为______________![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学中很多“规律”都有适用范围,下列根据有关“规律”推出的结论错误的有( )
序号 | 规律 | 结论 |
① | 活泼金属的氧化物为碱性氧化物 |
|
② | 酸与酸性氧化物不能发生反应 | 氢氟酸可以储存在玻璃试剂瓶中 |
③ | 较弱酸不能制取较强酸 | 氢硫酸不能制取硫酸 |
④ | 复分解反应均不是氧化还原反应 | 酸碱中和反应中没有电子的转移 |
A.①②③B.②③④C.①③④D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5 表示。有关说法正确的是 ( )
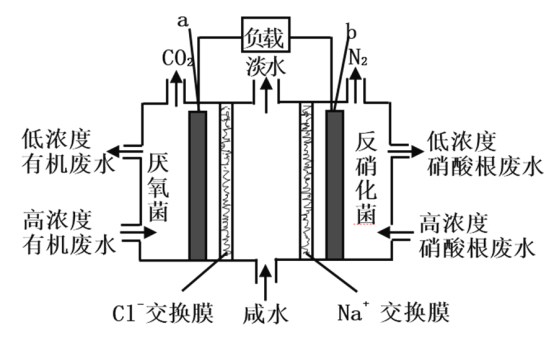
A.该装置为原电池,b为原电池的负极
B.a极区溶液的pH减小,中间室Na+移向左室
C. 当左室有4.48L(标准状况下)CO2生成时,右室产生的N2为0.8mol
D.a电极反应式:C6H10O5-24e-+7H2O===6CO2↑+24H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,计算下列溶液的pH,并将计算结果填在横线上:
(1)c(OH-)=1×10-4mol·L-1的溶液_______________。
(2)将0.1 mol HCl溶于水制成100 mL溶液______________。
(3)将pH=2的HCl溶液和pH=2的H2SO4溶液以体积比3∶1混合_____________。
(4)将0.23 g金属钠溶于水并配制成100 mL的溶液_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1 L 1 mol·L-1的氨水中,下列说法正确的是( )
A.含1 mol NH3·H2OB.含1 mol![]() 和OH-
和OH-
C.含![]() 和NH3·H2O的和为1 molD.含NH3、NH3·H2O、
和NH3·H2O的和为1 molD.含NH3、NH3·H2O、![]() 之和为1 mol
之和为1 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com