
ÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄŹżÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®1 mol NaÓė×ćĮæO2·“Ó¦£¬Éś³ÉNa2OŗĶNa2O2µÄ»ģŗĻĪļ£¬¹²×ŖŅĘNAøöµē×Ó
B£®±ź×¼×“æöĻĀ£¬5.6 LŅ»Ńõ»ÆµŖŗĶ5.6 LŃõĘų»ģŗĻŗóµÄ·Ö×Ó×ÜŹżĪŖ0.5NA
C£®±ź×¼×“æöĻĀ£¬11.2 L HFŗ¬ÓŠ0.5 NAøöHF·Ö×Ó
D£®500mL 12mol£®L-1µÄŃĪĖįÓė×ćĮæ MnO2¼ÓČČ³ä·Ö·“Ó¦£¬Éś³ÉCl2 ·Ö×ÓŹżÄæ1.5 NA

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¶¼ŹĒ½šŹōŌŖĖŲ | B£® | Ō×Ó°ė¾¶Ļą²ī²»“ó | ||
| C£® | ×īĶā²ćµē×ÓŹżĻąĶ¬ | D£® | »ÆŗĻ¼ŪĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”øßČżÉĻµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÓŠ¹Ųµē»ÆѧĖµ·Ø“ķĪóµÄŹĒ
A£®1 mol H2ŗĶ0£®5 mol O2·“Ó¦·Å³öµÄČČĮæ¾ĶŹĒH2µÄČ¼ÉÕČČ
B£®µČÖŹĮæµÄĮņÕōĘųŗĶĮņ¹ĢĢå·Ö±šĶźČ«Č¼ÉÕ£¬ĻąĶ¬Ģõ¼žĻĀ£¬Ē°Õ߷ųöµÄČČĮæ¶ą
C£®Ė®ÖŠµÄøÖÕ¢ĆÅĮ¬½ÓµēŌ“µÄøŗ¼«£¬ŹōÓŚĶā¼ÓµēĮ÷µÄŅõ¼«±£»¤·Ø
D£®ĢśÓöĄäÅØĻõĖį±ķĆę¶Ū»Æ£¬æɱ£»¤ÄŚ²æ²»±»øÆŹ“
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”øßČżÉĻµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻņCuSO4ČÜŅŗÖŠÖšµĪ¼ÓČėKIČÜŅŗÖĮ¹żĮ棬¹Ū²ģµ½²śÉś°×É«³ĮµķCuI£¬ČÜŅŗ±äĪŖ×ŲÉ«”£ŌŁĻņ·“Ó¦ŗóµÄ»ģŗĻĪļÖŠ²»¶ĻĶØČėSO2ĘųĢ壬ČÜŅŗÖš½„±ä³ÉĪŽÉ«”£ĻĀĮŠ·ÖĪöÕżČ·µÄŹĒ
A£®ÉĻŹöŹµŃéĢõ¼žĻĀ£¬ĪļÖŹµÄŃõ»ÆŠŌ£ŗCu2£«>I2>SO2
B£®ĶØČėSO2Ź±£¬SO2ÓėI2·“Ó¦£¬I2×÷»¹Ō¼Į
C£®ĶØČėSO2ŗóČÜŅŗÖš½„±ä³ÉĪŽÉ«£¬ĢåĻÖĮĖSO2µÄĘư׊Ō
D£®µĪ¼ÓKIČÜŅŗŹ±£¬×ŖŅĘ2 mol e£Ź±Éś³É1 mol°×É«³Įµķ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓ±±Ź”øßČżÉĻµŚ¶ž“ĪÄ£Äā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
ij Š£»Æѧъ¾æŠŌѧĻ°Š”×é²éŌÄ׏ĮĻĮĖ½āµ½ŅŌĻĀÄŚČŻ£ŗ
Š£»Æѧъ¾æŠŌѧĻ°Š”×é²éŌÄ׏ĮĻĮĖ½āµ½ŅŌĻĀÄŚČŻ£ŗ
ŅŅ¶žĖį£ØHOOC©COOH£¬æɼņŠ“ĪŖH2C2O4£©Ė×³Ę²ŻĖį£¬Ņ×ČÜÓŚĖ®£¬ŹōÓŚ¶žŌŖÖŠĒæĖį£ØĪŖČõµē½āÖŹ£©£¬ĒŅĖįŠŌĒæÓŚĢ¼Ėį£¬ĘäČŪµćĪŖ101.5”ę£¬ŌŚ157”ęÉż»Ŗ£®ĪŖĢ½¾æ²ŻĖįµÄ²æ·Ö»ÆѧŠŌÖŹ£¬½ųŠŠĮĖČēĻĀŹµŃé£ŗ
£Ø1£©ĻņŹ¢ÓŠ1mL±„ŗĶNaHCO3ČÜŅŗµÄŹŌ¹ÜÖŠ¼ÓČė×ćĮæŅŅ¶žĖįČÜŅŗ£¬¹Ū²ģµ½ÓŠĪŽÉ«ĘųÅŻ²śÉś£®øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ______________£®
£Ø2£©ĻņŹ¢ÓŠŅŅ¶žĖį±„ŗĶČÜŅŗµÄŹŌ¹ÜÖŠµĪČė¼øµĪĮņĖįĖį»ÆµÄKMnO4ČÜŅŗ£¬Õńµ“£¬·¢ĻÖĘäČÜŅŗµÄ×ĻŗģÉ«ĶŹČ„ £¬ĒėÅäĘ½øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ
£¬ĒėÅäĘ½øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ
______MnO4©+______ H2C2O4+______ H+ØT______ Mn2++______ CO2”ü+______ H2O
£Ø3£©½«Ņ»¶ØĮæµÄŅŅ¶žĖį·ÅÓŚŹŌ¹ÜÖŠ£¬°“ĻĀĶ¼ĖłŹ¾×°ÖĆ½ųŠŠŹµŃé£Ø×¢£ŗŗöĀŌ²ŻĖįµÄÉż»Ŗ£¬ĒŅ¼Š³Ö×°ÖĆĪ“±ź³ö£©£ŗ
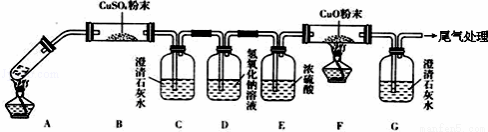
ŹµŃé·¢ĻÖ£ŗ×°ÖĆC”¢GÖŠ³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£¬BÖŠCuSO4·ŪÄ©±äĄ¶£¬FÖŠCuO·ŪÄ©ÓŠŗŚÉ«±äĪŖŗģ É«£®¾Ż“Ė»Ų“š£ŗ
É«£®¾Ż“Ė»Ų“š£ŗ
ÉĻŹö×°ÖĆÖŠ£¬DµÄ×÷ÓĆŹĒ_________£®ŅŅ¶žĖį·Ö½āµÄ»Æѧ·½³ĢŹ½ĪŖ_________£®Ö»øł¾ŻGÖŠ³ĪĒåŹÆ»ŅĖ®±ä»ė×ĒÄÜ·ńµĆ³ö”°²ŻĖį·Ö½ā²śĪļÖŠŅ»¶ØÓŠCO”±µÄ½įĀŪ_________£ØĢī”° ÄÜ»ņ²»ÄÜ”±£©
ÄÜ»ņ²»ÄÜ”±£© Čō²»ÄÜÓ¦ŌõŃłøĽų£æ______________£®
Čō²»ÄÜÓ¦ŌõŃłøĽų£æ______________£®
£Ø4£©øĆŠ”×éĶ¬Ń§½«2.52g²ŻĖį¾§Ģå£ØH2C2O4•2H2O£©¼ÓČėµ½100mL 0.2mol/LµÄNaOHČÜŅŗÖŠ³ä·Ö·“Ó¦£¬²āµĆ·“Ó¦ŗóČÜŅŗ³ŹĖįŠŌ£ØŗöĀŌČÜŅŗĢå»ż±ä»Æ£©£®ŌņĻĀĮŠ¹ŲĻµŗĻĄķµÄŹĒ_________
A£®c£ØNa+£©+c£ØH+£©=c£ØHC2O4©£©+c£ØOH©£©+c£ØC2O42©£©
B£®c£ØHC2O4©£©+c£ØC2O42©£©=0.2mol•L ©1
©1
C£®c£ØHC2O4©£©£¾c£ØC2O42©£©£¾c£ØH2C2O4£©
D£®c£ØNa+£©=c£ØH2C2 O4£©+c£ØHC2O4©£©+c£ØC2O42©£©
O4£©+c£ØHC2O4©£©+c£ØC2O42©£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĖįŠŌ£ŗHClO4£¾HBrO4£¾HIO4 | B£® | ¼īŠŌ£ŗNaOH£¾Mg£ØOH£©2£¾Al£ØOH£©3 | ||
| C£® | ĪČ¶ØŠŌ£ŗPH3£¾H2S£¾HCl | D£® | Ō×Ó°ė¾¶£ŗBr£¾Cl£¾F |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com