
| A. | 结构简式为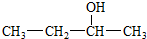 的有机物其名称为 2-丁醇 的有机物其名称为 2-丁醇 | |
| B. | 分子式为C4H8Br2结构中含一个一CH3的同分异构体(不考虑立体异构)有4种 | |
| C. | 某有机物球棍结构模型为: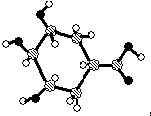 ,则该有机物能发生消去反应和氧化反应 ,则该有机物能发生消去反应和氧化反应 | |
| D. | 二十碳五烯酸和二十二碳六烯酸是鱼油的主要成分,它们含有相同的官能团,是同系物,化学性质相似 |
分析 A、醇类的命名,选取含有羟基的最长碳链为主链,编号从醇类羟基最近的一端开始;
B、二溴代物的同分异构体可以采用“定一议二”法解题,先找出所有的同分异构体,再找出只含一个“-CH3”的;
C、分子中含有羟基,且羟基邻位碳原子连接氢原子;
D、碳碳双键数目不同,不是同系物.
解答 解:A、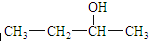 中含有羟基的最长碳链含有4个C,主链为丁醇,在2号C含有羟基,该有机物名称为2-丁醇,故A正确;
中含有羟基的最长碳链含有4个C,主链为丁醇,在2号C含有羟基,该有机物名称为2-丁醇,故A正确;
B、C4H8Br2的同分异构体可以采取“定一议二”法确定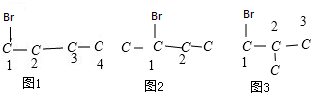 ,由图可知C4H8Br2共有9种同分异构体,其中图1中只含一个“-CH3”的为1、2、3三种,图2中都含有2个“-CH3”,图3中只含一个“-CH3”的为3只有一种,则只含一个“-CH3”的C4H8Br2的同分异构体共4种,故B正确;
,由图可知C4H8Br2共有9种同分异构体,其中图1中只含一个“-CH3”的为1、2、3三种,图2中都含有2个“-CH3”,图3中只含一个“-CH3”的为3只有一种,则只含一个“-CH3”的C4H8Br2的同分异构体共4种,故B正确;
C、分子中含有羟基,且羟基邻位碳原子连接氢原子,该有机物能发生消去反应和氧化反应,故C正确;
D.碳碳双键数目不同,不是同系物,故D错误.
故选D.
点评 本题考查有机物结构和性质,侧重于有机物结构和性质的综合应用,为高考常见题型,注意把握有机物的结构特点和官能团的性质,为解答该题的关键,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H5O-+CO2+H2O→C6H5OH+HCO3- | |
| B. | C6H5OH+OH-→C6H5O-+H2O | |
| C. | CH3CHO+2[Ag(NH3)2]++2OH-→CH3COONH4+2Ag↓+3NH3+H2O | |
| D. | CH3CHO+2[Ag(NH3)2]++2OH-→CH3COO-+NH4++2Ag↓+3NH3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
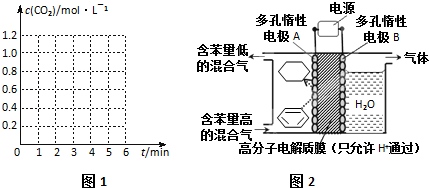
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| H2O | CO | CO2 | |||
| 1 | 500 | 4 | 8 | 3.2 | 4 |
| 2 | 750 | 2 | 4 | 0.8 | 3 |
| 3 | 750 | 2 | 4 | 0.8 | 1 |
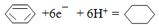 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | C | |
| B |
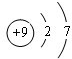 ,比较B、C的原子半径:B>C;
,比较B、C的原子半径:B>C;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com