
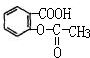
 它的化学式为C9H8O4,其分子中含有羧基和酯基两种官能团(写官能团的名称),下列反应能发生的是(填字母):A、B、D(选项:A取代反应、B水解反应、C消去反应、D加成反应),该化合物1mol最多能跟3molNaOH反应.
它的化学式为C9H8O4,其分子中含有羧基和酯基两种官能团(写官能团的名称),下列反应能发生的是(填字母):A、B、D(选项:A取代反应、B水解反应、C消去反应、D加成反应),该化合物1mol最多能跟3molNaOH反应. 分析 (1)金属的电化学腐蚀分为析氢腐蚀和吸氧腐蚀,在正极上都是得电子的还原反应,负极反应都为铁失电子生成二价铁离子的反应,反应式为Fe-2e-=Fe2+,所以总反应为:2Fe+2H2O+O2=2Fe(OH)2,最后生成铁锈(主要成分Fe2O3)的两个化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,2Fe(OH)3=Fe2O3+3H2O;
(2)NaHCO3与Al2(SO4)3发生相互促进的水解反应生成二氧化碳和氢氧化铝;
(3)阿司匹林 它的化学式为C9H8O4,含有官能团有酯基和羧基;羧基能发生酯化反应,酯基能发生水解反应,苯环能加成反应;1mol与羧基与1molNaOH反应,1mol酯基能与2molNaOH反应发生水解反应;
它的化学式为C9H8O4,含有官能团有酯基和羧基;羧基能发生酯化反应,酯基能发生水解反应,苯环能加成反应;1mol与羧基与1molNaOH反应,1mol酯基能与2molNaOH反应发生水解反应;
解答 解:(1)金属的电化学腐蚀分为析氢腐蚀和吸氧腐蚀,在正极上都是得电子的还原反应,析氢腐蚀中,正极上的电极反应式为:2H++2e-=H2↑,吸氧腐蚀中,正极反应为:O2+4e-+2H2O═4OH-,负极反应都为铁失电子生成二价铁离子的反应,反应式为Fe-2e-=Fe2+,所以总反应为:2Fe+2H2O+O2=2Fe(OH)2,最后生成铁锈(主要成分Fe2O3)的两个化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,2Fe(OH)3=Fe2O3+3H2O;
故答案为:2H++2e-=H2↑;O2+4e-+2H2O═4OH-;2Fe+2H2O+O2=2Fe(OH)2;4Fe(OH)2+O2+2H2O=4Fe(OH)3;2Fe(OH)3=Fe2O3+3H2O;
(2)NaHCO3与Al2(SO4)3发生相互促进的水解反应生成二氧化碳和氢氧化铝,其反应的离子方程式为:Al3++3HCO3-=Al(OH)3↓+3CO2↑;
故答案为:Al3++3HCO3-=Al(OH)3↓+3CO2↑;
(3)阿司匹林 它的化学式为C9H8O4,含有官能团有酯基和羧基;羧基能发生酯化反应,酯基能发生水解反应,苯环能加成反应,所以选ABD;1mol与羧基与1molNaOH反应,1mol酯基能与2molNaOH反应发生水解反应,所以化合物1mol最多能跟3molNaOH反应,故答案为:C9H8O4;羧基、酯基;A、B、D; 3.
它的化学式为C9H8O4,含有官能团有酯基和羧基;羧基能发生酯化反应,酯基能发生水解反应,苯环能加成反应,所以选ABD;1mol与羧基与1molNaOH反应,1mol酯基能与2molNaOH反应发生水解反应,所以化合物1mol最多能跟3molNaOH反应,故答案为:C9H8O4;羧基、酯基;A、B、D; 3.
点评 本题考查了金属的腐蚀和防护知识,泡沫灭火器的原理,有机物的结构判断其具有的性质,难度不大,根据官能团确定其性质进行分析解答即可.


科目:高中化学 来源: 题型:选择题
| A. | 氯气可以使湿润的有色布条褪色,是因为氯气具有漂白性 | |
| B. | SO2溶于水,其水溶液能导电,说明SO2是电解质 | |
| C. | 石墨转化为金刚石的反应是吸热反应,说明等量的石墨比金刚石能量高 | |
| D. | 某溶液用盐酸酸化无明显现象,再滴加氯化钡溶液有白色沉淀产生,说明溶液中有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+结构示意图: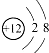 | B. | CCl4分子的比例模型: | ||
| C. | NH4Cl的电子式: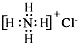 | D. | 2-甲基丁醇的结构简式: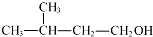 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
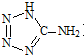 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
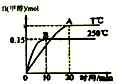
| A. | 混合气体的密度不变能说明该反应到达平衡状态 | |
| B. | a>0 | |
| C. | 其他条件不变,若减小容积体积,CO质量分数增大 | |
| D. | 平衡常数K:T℃时大于250℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | I元素的质量数是131 | B. | I元素的中子数是78 | ||
| C. | I原子5p亚层有一个未成对电子 | D. | I原子有53个能量不同的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的铝与足量的烧碱和盐酸反应生成氢气的质量相同 | |
| B. | 等质量的铜与足量的浓硫酸和浓硝酸反应生成气体的物质的量相同 | |
| C. | 相同物质的量的烧碱和纯碱与足量盐酸反应,消耗盐酸的体积相同 | |
| D. | 相同质量的硫与足量烧碱、浓硫酸、浓硝酸反应,转移电子数相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com