
下列有关等离子体的说法中,不正确的是( )
A.等离子体内部全部是带电荷的微粒
B.等离子体中正、负电荷大致相等
C.等离子体具有很好的导电性
D.等离子体用途十分广泛
科目:高中化学 来源: 题型:
A、B、C、D、E、F分别是氧化铁、二氧化碳、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液中的一种;已知C在日常生活中常用来灭火。六种物质之间有如图所示的反应关系,图中相连的两圆表示相应物质间能发生反应。回答下列问题:

(1)E与F反应的实验现象是 ________________。
(2)A与D反应的化学方程式为 ____________。
(3)B能转化成A,反应的化学方程式为 _________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ、一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g) FeO(s)+CO(g) ΔH>0。
FeO(s)+CO(g) ΔH>0。
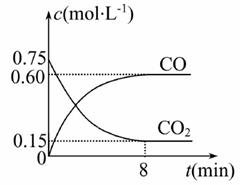
(1)下列措施中能使平衡时c(CO)/c(CO2)增大的是_________(填序号)。
A.升高温度 B.增大压强
C.充入一定量氮气 D.再加入一些铁粉
(2)反应达到平衡后,若保持容器体积不变时,再通入一定量的CO2,使CO2的浓度成为原来的2倍,则CO2的转化率将_______(填“增大”“减小”或“不变”)。
Ⅱ、在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:C(s)+H2O(g) CO(g)+H2(g),试分析和回答下列问题:
CO(g)+H2(g),试分析和回答下列问题:
(1)可认定上述可逆反应在一定条件下已达到化学平衡状态的是______(选填序号)。
A.体系的压强不再发生变化
B.v正(CO)=v逆(H2O)
C.生成n mol CO的同时生成n mol H2
D.1 mol H—H键断裂的同时断裂2 mol H—O键
(2)若上述化学平衡状态从正反应开始建立,达到平衡后,给平衡体系加压(缩小容积、其他条件不变),则容器内气体的平均相对分子质量将______(填写“不变”“变小”或“变大”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z是元素周期表中的三种短周期元素,三者的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
| X | ||
| Z | Y |
A.Z一定是活泼的金属元素
B.Y不存在最高价氧化物
C.1 mol Y的单质溶于足量水时,反应转移的电子为1 mol
D.Y的氢化物稳定性大于Z的氢化物稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。请根据下表所列数据判断,错误的是( )
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4 600 | 6 900 | 9 500 |
| Y | 580 | 1 800 | 2 700 | 11 600 |
A.元素X的常见化合价是+1
B.元素Y是ⅢA族元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第3周期,它可与冷水剧烈反应
查看答案和解析>>
科目:高中化学 来源: 题型:
纳米材料是21世纪最有前途的新型材料之一,世界各国对这一新材料给予了极大的关注。纳米粒子是指直径为1~100 nm的超细粒子(1 nm=10-9m)。由于表面效应和体积效应,其常有奇特的光、电、磁、热等性质,可开发为新型功能材料。下列有关纳米粒子的叙述不正确的是( )
A.因纳米粒子半径太小,故不能将其制成胶体
B.一定条件下纳米粒子可催化水的分解
C.一定条件下,纳米TiO2陶瓷可发生任意弯曲,可塑性好
D.纳米粒子半径小,表面活性高
查看答案和解析>>
科目:高中化学 来源: 题型:
分析化学中常用X射线研究晶体结构,有一种蓝色晶体可表示为:MxFey(CN)z,研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN一位于立方体的棱上,其晶体中的阴离子结构如图示,下列说法正确的是
A.该晶体是原子晶体
B.M的离子位于上述立方体的面心,呈+2价
C.M的离子位于上述立方体的体心,呈+1价,且M+空缺率(体心中没有M+的占总体心的百分比)为50%
D.晶体的化学式可表示为MFe2(CN)3,且M为+1价
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com