

| ·“Ó¦Ź±¼ä£Ømin£© | n£ØCO£©£Ømol£© | N£ØH2O£©£Ømol£© |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
·ÖĪö £Ø1£©¢ŁĘ½ŗā³£ŹżĪŖÉś³ÉĪļĘ½ŗāÅØ¶Č»Æѧ¼ĘĮæŹżĆŻ³Ė»żÓė·“Ó¦ĪļĘ½ŗāÅØ¶Č»Æѧ¼ĘĮæŹżĆŻ³Ė»żÖ®±Č£»
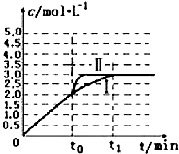
¢ŚÓÉĶ¼æŖŹ¼£¬ÉżøßĪĀ¶Č¼×ĶéµÄĢå»ż·ÖŹż¼õŠ”£¬ĖµĆ÷ÉżøßĪĀ¶ČĘ½ŗāÕżĻņŅĘ¶Æ£¬Ę½ŗā³£ŹżŌö“ó£»
Õż·“Ó¦ĪŖĘųĢåĪļÖŹµÄĮæŌö“óµÄ·“Ó¦£¬Ōö“óŃ¹ĒæĘ½ŗāÄęĻņŅĘ¶Æ£¬¼×ĶéµÄĢå»ż·ÖŹżŌö“ó£»
£Ø2£©¢Łt1minŹ±£¬·“Ó¦µÄCOĪŖ1.2mol-0.8mol=0.4mol£¬ÓÉ·½³ĢŹ½æÉÖŖ·“Ó¦µÄĖ®ĪŖ0.4mol£¬Ōņ“ĖŹ±Ė®µÄĪļÖŹµÄĮæĪŖ0.6mol-0.4mol=0.2mol£¬¶ųt2minŹ±Ė®ĪŖ0.2mol£¬¹Źt1min”¢t2min¾ł“¦ÓŚĘ½ŗāדĢ¬£¬Ę½ŗāŹ±¶žŃõ»ÆĢ¼ĪŖ0.4mol£¬
±£³ÖT1ĪĀ¶Č²»±ä£¬ČōĻņŌČŻĘ÷ÖŠĶØČė 0.60mol COŗĶ1.20mol H2O£Øg£©£¬ÓėŌĘ½ŗāĻą±Č·“Ó¦ĪļµÄĮæĻą»„½»»»£¬¶žÕß°“1£ŗ1·“Ó¦£¬Ę½ŗā³£ŹżK=$\frac{c£ØC{O}_{2}£©”Įc£Ø{H}_{2}£©}{c£ØCO£©”Įc£Ø{H}_{2}O£©}$²»±ä£¬ŌņĘ½ŗāŹ±¶ŌӦɜ³ÉĪļµÄĮæÓėŌĘ½ŗāĻąĶ¬£»
¢ŚČō“ļµ½Ę½ŗāŗ󣬱£³ÖĘäĖūĢõ¼ž²»±ä£¬Ö»ŹĒĻņŌĘ½ŗāĢåĻµÖŠŌŁĶØČė0.20mol H2O£Øg£©£¬
a£®Ę½ŗāÕżĻņŅĘ¶Æ£¬COµÄ×Ŗ»ÆĀŹ½«Ōö“ó£»
b£®µČŠ§ĪŖæŖŹ¼ĶØČė1.6molCO”¢0.8molĖ®µ½“ļĘ½ŗāŗóŌŁŅĘ×ß0.4molCO£¬¶ųæŖŹ¼ĶØČė1.6molCO”¢0.8molĖ®ÓėŌĘ½ŗāĪŖµČŠ§Ę½ŗā£¬Ę½ŗāŹ±Ė®µÄĢå»ż·ÖŹżĻąĶ¬£»
c£®»ģŗĻĘųĢå×ÜÖŹĮæŌö“ó£¬ČŻĘ÷µÄČŻ»ż²»±ä£»
d£®»ÆŃ§Ę½ŗā³£ŹżÖ»ŹÜĪĀ¶ČÓ°Ļģ£®
½ā“š ½ā£ŗ£Ø1£©¢ŁCH4£Øg£©+H2O£Øg£©?CO£Øg£©+3H2£Øg£©µÄĘ½ŗā³£Źż±ķ“ļŹ½K=$\frac{c£ØCO£©”Į{c}^{3}£Ø{H}_{2}£©}{c£ØC{H}_{4}£©”Įc£Ø{H}_{2}O£©}$£¬
¹Ź“š°øĪŖ£ŗ$\frac{c£ØCO£©”Į{c}^{3}£Ø{H}_{2}£©}{c£ØC{H}_{4}£©”Įc£Ø{H}_{2}O£©}$£»
¢ŚÓÉĶ¼æŖŹ¼£¬ÉżøßĪĀ¶Č¼×ĶéµÄĢå»ż·ÖŹż¼õŠ”£¬ĖµĆ÷ÉżøßĪĀ¶ČĘ½ŗāÕżĻņŅĘ¶Æ£¬Ę½ŗā³£ŹżŌö“ó£»
Õż·“Ó¦ĪŖĘųĢåĪļÖŹµÄĮæŌö“óµÄ·“Ó¦£¬Ōö“óŃ¹ĒæĘ½ŗāÄęĻņŅĘ¶Æ£¬¼×ĶéµÄĢå»ż·ÖŹżŌö“ó£¬ŌņP1£¾P2£¬
¹Ź“š°øĪŖ£ŗŌö“󣻣¾£»
£Ø2£©¢Łt1minŹ±£¬·“Ó¦µÄCOĪŖ1.2mol-0.8mol=0.4mol£¬ÓÉ·½³ĢŹ½æÉÖŖ·“Ó¦µÄĖ®ĪŖ0.4mol£¬Ōņ“ĖŹ±Ė®µÄĪļÖŹµÄĮæĪŖ0.6mol-0.4mol=0.2mol£¬¶ųt2minŹ±Ė®ĪŖ0.2mol£¬¹Źt1min”¢t2min¾ł“¦ÓŚĘ½ŗāדĢ¬£¬Ę½ŗāŹ±¶žŃõ»ÆĢ¼ĪŖ0.4mol£¬
±£³ÖT1ĪĀ¶Č²»±ä£¬ČōĻņŌČŻĘ÷ÖŠĶØČė 0.60mol COŗĶ1.20mol H2O£Øg£©£¬ÓėŌĘ½ŗāĻą±Č·“Ó¦ĪļµÄĮæĻą»„½»»»£¬¶žÕß°“1£ŗ1·“Ó¦£¬Ę½ŗā³£ŹżK=$\frac{c£ØC{O}_{2}£©”Įc£Ø{H}_{2}£©}{c£ØCO£©”Įc£Ø{H}_{2}O£©}$²»±ä£¬ŌņĘ½ŗāŹ±¶ŌӦɜ³ÉĪļµÄĮæÓėŌĘ½ŗāĻąĶ¬£¬¹ŹÉś³É¶žŃõ»ÆĢ¼ĪŖ0.4mol£¬
¹Ź“š°øĪŖ£ŗ0.4mol£»
¢ŚČō“ļµ½Ę½ŗāŗ󣬱£³ÖĘäĖūĢõ¼ž²»±ä£¬Ö»ŹĒĻņŌĘ½ŗāĢåĻµÖŠŌŁĶØČė0.20mol H2O£Øg£©£¬
a£®Ę½ŗāÕżĻņŅĘ¶Æ£¬COµÄ×Ŗ»ÆĀŹ½«Ōö“󣬹ŹaÕżČ·£»
b£®ŌŁĶØČė0.20mol H2O£Øg£©µČŠ§ĪŖæŖŹ¼ĶØČė1.6molCO”¢0.8molĖ®µ½“ļĘ½ŗāŗóŌŁŅĘ×ß0.4molCO£¬ŅĘ×ß0.4molCOŗóµÄĘ½ŗāÓėæŖŹ¼ĶØČė1.6molCO”¢0.8molĖ®µ½“ļĘ½ŗāĻą±Č£¬Ę½ŗāÄęĻņŅĘ¶Æ£¬Ė®µÄĢå»ż·ÖŹżŌö“󣬶ųæŖŹ¼ĶØČė1.6molCO”¢0.8molĖ®ÓėŌĘ½ŗāĪŖµČŠ§Ę½ŗā£¬Ę½ŗāŹ±Ė®µÄĢå»ż·ÖŹżĻąĶ¬£¬¹ŹĻņŌĘ½ŗāĢåĻµÖŠŌŁĶØČė0.20mol H2O£Øg£©Ź±£¬H2O£Øg£©µÄĢå»ż·ÖŹż½«Ōö“󣬹ŹbÕżČ·£»
c£®»ģŗĻĘųĢå×ÜÖŹĮæŌö“ó£¬ČŻĘ÷µÄČŻ»ż²»±ä£¬ĆܶČŌö“󣬹Źc“ķĪó£»
d£®ĪĀ¶Č²»±ä£¬Ę½ŗā³£Źż²»±ä£¬¹Źd“ķĪó£¬
¹ŹŃ”£ŗab£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗā¼ĘĖć”¢»ÆŃ§Ę½ŗāÓ°ĻģŅņĖŲµČ£¬£Ø2£©ÖŠ¢Ł×¢Ņā¶Ō¹ęĀɹéÄÉ×ܽį£¬£Ø2£©ÖŠ¢ŚbŃ”Ļī×¢ŅāĄūÓƵȊ§Ė¼Ļė¹¹½ØĘ½ŗā½ØĮ¢µÄĶ¾¾¶£¬ÄѶČÖŠµČ£®


 ĶõŗóŠŪѧ°ø½Ģ²ÄĶźČ«½ā¶ĮĻµĮŠ“š°ø
ĶõŗóŠŪѧ°ø½Ģ²ÄĶźČ«½ā¶ĮĻµĮŠ“š°ø ŗ£µķæĪŹ±ŠĀ×÷Ņµ½š°ń¾ķĻµĮŠ“š°ø
ŗ£µķæĪŹ±ŠĀ×÷Ņµ½š°ń¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČŻĮæĘæÄŚÓŠĖ®£¬Ī“¾¹żøÉŌļ“¦Ąķ | |
| B£® | ¶ØČŻŹ±£¬ŃöŹÓæĢ¶ČĻß | |
| C£® | ÓĆĮæĶ²ĮæČ”ÅØŃĪĖįŹ±£¬ÓĆĖ®Ļ“µÓĮæĶ²2”«3“Ī£¬Ļ“Ņŗµ¹ČėÉÕ±ÖŠ | |
| D£® | ¶ØČŻŗóµ¹×ŖČŻĮæĘæ¼ø“Ī£¬·¢ĻÖŅŗĢå×īµĶµćµĶÓŚæĢ¶ČĻߣ¬ŌŁ²¹¼Ó¼øµĪĖ®µ½æĢ¶ČĻß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| n/mol t/min | NO | N2 | CO2 |
| 0 | 2.00 | 0 | 0 |
| 10 | 1.16 | 0.42 | 0.42 |
| 20 | 0.80 | 0.60 | 0.60 |
| 30 | 0.80 | 0.60 | 0.60 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ”śŗĻ³É”śĖ®ČČ“¦Ąķ”ś¹żĀĖ”śĖ®Ļ“”ś±ķĆꓦĄķ”ś¹żĀĖĖ®Ļ“”śøÉŌļ
”śŗĻ³É”śĖ®ČČ“¦Ąķ”ś¹żĀĖ”śĖ®Ļ“”ś±ķĆꓦĄķ”ś¹żĀĖĖ®Ļ“”śøÉŌļ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼Ó³É·“Ó¦ | B£® | Ńõ»Æ·“Ó¦ | C£® | Ė®½ā·“Ó¦ | D£® | Ėõ¾Ū·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ¼×“¼¶ŌĖ®ÖŹ»įŌģ³ÉŅ»¶ØµÄĪŪČ¾£¬ÓŠŅ»ÖÖµē»Æѧ·ØæÉĻū³żÕāÖÖĪŪČ¾£¬ĘäŌĄķŹĒĶصēŗ󣬽«Co2+Ńõ»Æ³ÉCo3+£¬Č»ŗóŅŌCo3+×÷Ńõ»Æ¼Į°ŃĖ®ÖŠµÄ¼×“¼Ńõ»Æ³ÉCO2¶ų¾»»Æ£®ŹµŃéŹŅÓĆČēĶ¼×°ÖĆÄ£ÄāÉĻŹö¹ż³Ģ£ŗ
¼×“¼¶ŌĖ®ÖŹ»įŌģ³ÉŅ»¶ØµÄĪŪČ¾£¬ÓŠŅ»ÖÖµē»Æѧ·ØæÉĻū³żÕāÖÖĪŪČ¾£¬ĘäŌĄķŹĒĶصēŗ󣬽«Co2+Ńõ»Æ³ÉCo3+£¬Č»ŗóŅŌCo3+×÷Ńõ»Æ¼Į°ŃĖ®ÖŠµÄ¼×“¼Ńõ»Æ³ÉCO2¶ų¾»»Æ£®ŹµŃéŹŅÓĆČēĶ¼×°ÖĆÄ£ÄāÉĻŹö¹ż³Ģ£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com