
| A.用物质A表示的反应的平均速率为0.3mol?L-1?s-1 |
| B.用物质B表示的反应的平均速率为0.6mol?L-1?s-1 |
| C.2s时物质A的转化率为70% |
| D.2s时物质B的浓度为0.7mol?L-1 |
科目:高中化学 来源:不详 题型:单选题

| A.a% > b% | B.a%< b% | C.a%=" b%" | D.无法判定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
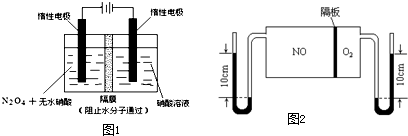
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol?L-1 | 5.00 | 3.52 | 2.48 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
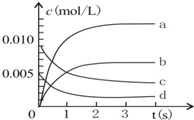
 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
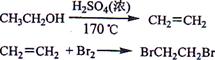
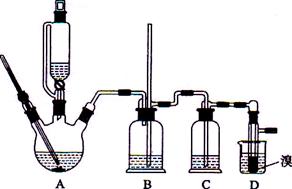
| | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 状态 | 色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.石油和天然气的主要成分都是碳氢化合物 |
| B.乙醇、乙酸和乙酸乙酯可以用饱和碳酸钠溶液鉴别 |
| C.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
| D.甘氨酸(NH2-CH2-COOH)既能与NaOH反应,又能与盐酸反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
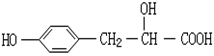
| A.①②③⑤⑥⑦ | B.②③④⑥⑧ | C.①②③④⑥ | D.③⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
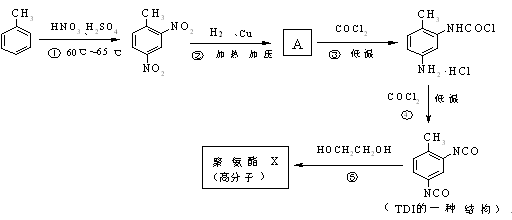
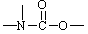 结构。第⑤步反应类型为 ,
结构。第⑤步反应类型为 , 的结构简式。
的结构简式。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com