
| A. | 在相同温度下,Na2CO3比NaHCO3的溶解度小 | |
| B. | 可用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液 | |
| C. | 可用加热的方法除去Na2CO3中混有的NaHCO3杂质 | |
| D. | Na2CO3和NaHCO3固体分别与盐酸反应产生等量的CO2时,后者消耗的H+多 |
分析 A.NaHCO3不稳定,溶解度比Na2CO3小;
B.Na2CO3和NaHCO3两种溶液与石灰水反应均生成碳酸钙白色沉淀;
C.NaHCO3加热易分解,而Na2CO3不能;
D.都生成1mol的二氧化碳,碳酸钠需2mol的盐酸,碳酸氢钠需1mol的盐酸.
解答 解:A.在饱和Na2CO3溶液中通入过量二氧化碳可生成NaHCO3沉淀,可说明水中的溶解度:Na2CO3>NaHCO3,故A错误;
B.Na2CO3和NaHCO3两种溶液与石灰水反应均生成碳酸钙白色沉淀,不能鉴别,应选氯化钙,故B错误;
C.NaHCO3加热易分解,而Na2CO3不能,则可采用加热的方法除去Na2CO3固体中混有的NaHCO3,故C正确;
D.都生成1mol的二氧化碳,碳酸钠需2mol的盐酸,碳酸氢钠需1mol的盐酸,所以前者消耗的H+多,故D错误;
故选C.
点评 本题考查Na2CO3和NaHCO3性质的异同,题目难度不大,注意把握Na2CO3和NaHCO3性质,易错点为B,注意区分二者与碱的反应.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:填空题
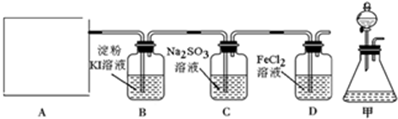

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 负极发生氧化反应 | B. | 烧杯中的溶液变为蓝色 | ||
| C. | 电子由铜片通过导线流向锌片 | D. | 该装置能将电能转变为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解法、热还原法、热分解法 | B. | 热还原法、热分解法、电解法 | ||
| C. | 热分解法、热还原法、电解法 | D. | 电解法、热分解法、热还原法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
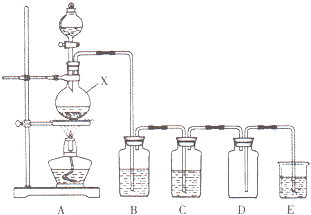 实验室中常用二氧化锰与浓盐酸共热制取氯气.某化学兴趣小组为制取较为纯净、干燥的氯气,设计了如下实验装置.
实验室中常用二氧化锰与浓盐酸共热制取氯气.某化学兴趣小组为制取较为纯净、干燥的氯气,设计了如下实验装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 0~t2时,v正始终大于v逆 | |
| B. | Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ>Ⅱ | |
| C. | Ⅰ、Ⅱ两过程达到平衡时,平衡常数Ⅰ<Ⅱ | |
| D. | t2时刻改变的条件可以是向密闭容器中加C |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com