
| A. | v(SiF4)消耗=4v(HF)生成 | B. | HF 的体积分数不再变化 | ||
| C. | 容器内气体压强不再变化 | D. | 容器内气体总质量不再变化 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、平衡时应有4v(SiF4)消耗=v(HF)生成,故A错误;
B、HF 的体积分数不再变化,说明各组分的物质的量不变,反应达平衡状态,故B正确;
C、容器内气体压强不再变化,说明气体的总物质的量不变,说明反应达平衡状态,故C正确;
D、当容器内气体总质量不再变化,根据质量守恒,说明固体二氧化硅的物质的量不变,正逆反应速率相等,故D正确;
故选A.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.


科目:高中化学 来源: 题型:选择题
| A. | 苯分子中含有碳碳双键 | B. | 氨基酸分子中可能含有手性碳原子 | ||
| C. | 己烷有3种同分异构体 | D. | 乙酸分子中所有原子处于同一平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,8.0gCH4中含有的氢原子数为NA | |
| B. | 1mol氯气跟水完全反应,转移的电子数为2NA | |
| C. | 1 molNa2O2跟足量CO2完全反应,转移的电子数为NA | |
| D. | 0.1mol/L MgCl2溶液中含氯离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NH4+、NO3-、Al3+、Cl- | B. | Na+、AlO2-、K+、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | AlO2-、K+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 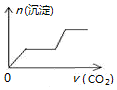 | B. | 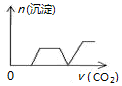 | C. | 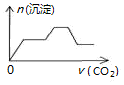 | D. | 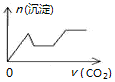 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
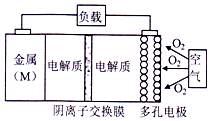 电池的“理论比能量”指单位质量的电极材料理论上能释放的最大电能.“金属(M)〜空气电池”(如下图)具有原料易得、能量密度高等优点.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.下列说法不正确的是( )
电池的“理论比能量”指单位质量的电极材料理论上能释放的最大电能.“金属(M)〜空气电池”(如下图)具有原料易得、能量密度高等优点.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.下列说法不正确的是( )| A. | “金属(M)〜空气电池”放电过程的正极反应式:O2+2H2O+4e-=4M(OH)n | |
| B. | 比较Mg、Al、Zn三种“金属-空气电池”,“Al-空气电池”的理论比能量最高 | |
| C. | 电解质溶液中的阴离子从负极区移向正极区 | |
| D. | 在“M-空气电池”中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 有关物质的转化关系如图所示(部分物质与条件己略去).A是最常见的无色液体,B、C是常见的金属单质,D、E是气体单质,且D在空气中的含量最多,F 是一种具有磁性的化合物,H是既能与强酸反应又能与强碱反应的氧化物:I具有耐高温、抗冲击、导热性好的优良性质,广泛应用于电子工业、陶瓷工业中.
有关物质的转化关系如图所示(部分物质与条件己略去).A是最常见的无色液体,B、C是常见的金属单质,D、E是气体单质,且D在空气中的含量最多,F 是一种具有磁性的化合物,H是既能与强酸反应又能与强碱反应的氧化物:I具有耐高温、抗冲击、导热性好的优良性质,广泛应用于电子工业、陶瓷工业中. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝及其合金广泛应用,是因为铝的性质稳定,不易被腐蚀 | |
| B. | 用乙烯作为水果的催熟剂,以使生水果尽快成熟 | |
| C. | 工业上燃烧煤时,加入少量石灰石是为了减少SO2的排放 | |
| D. | 误食重金属盐引起人体中毒,可喝牛奶或豆浆解毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com