
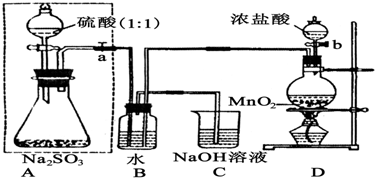
| ||
| ||
| 126b |
| 233 |
| 126b |
| 233a |
| 126b |
| 233a |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1mol NaHSO4���庬��2NA������ |
| B��1L2mol/L������Һ��ˮ��ɵõ����������������ӵ���ĿΪ2NA�� |
| C��1mol CH3+��̼�����ӣ��к��еĵ�����Ϊ10NA |
| D����O2����ķ�Ӧ�У�1molO2��������ʱ�õ��ĵ�����һ����4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��14C��12C��Ϊͬ�������� |
| B���Ҵ�������ͼ�ȩ�㷺Ӧ����ʳƷ�ӹ� |
| C����ά�ء��ϳ���ά�����ά�����л��߷��ӻ����� |
| D����������ֲ��ϲ������Ͻ������Ͻ�ǿ�ȴ������ᡢ����ʴ����ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
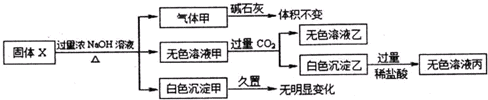
| A�������һ���Ǵ����� |
| B����ɫ���������ǻ���� |
| C������X��һ������AlCl3����NH4��2SO4��MgCl2 |
| D������������ɫ��Һ�Һ�������ɫ��Һ����ϼ�����ɫ�������ɣ�Ҳ�а�ɫ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
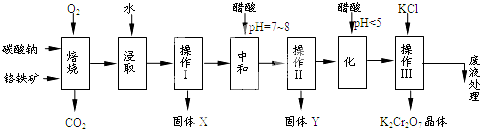
| 750�� |
| 750�� |
| ���� | �ܽ��/��g/100gˮ�� | ||
| 0�� | 40�� | 80�� | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O | 163 | 215 | 376 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| t/min | 2 | 4 | 7 | 9 |
| n��Y��/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A����Ӧǰ2min��ƽ�����ʦͣ�Z��=0.04mol?L-1?min-1 |
| B�������������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰ�ͣ��棩���ͣ����� |
| C�����¶��´˷�Ӧ��ƽ�ⳣ��K=90L/mol |
| D�������������䣬�ٳ���0.2molZ��ƽ��ʱX�����������С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| 1 |
| 3 |
| a |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
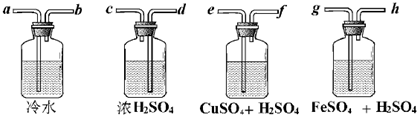
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NH3 |
| B��PCl5 |
| C��COCl2 |
| D��BF3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com