
【题目】有人设想以N2和H2为反应物,以溶有X的稀盐酸为电解质溶液,制造出新型燃料电池,装置如图所示。下列说法正确的是
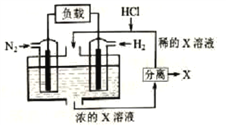
A. 放电时H+向左移动,生成的物质X是NH4Cl
B. 通入H2的一极为正极
C. 通入N2的电极反应为:N2+6H+-6e-=2NH3
D. 放电过程右边区域溶液pH逐渐增大
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
【题目】将Cu片放入0.1mol/LFeCl3溶液中,反应一定时间后取出(溶液体积变化忽略不计),所得溶液Q中的![]() ,下列有关说法正确的是
,下列有关说法正确的是
A. 溶液Q比原溶液增重了1.92g.
B. Q中n(Cu2+):n(Fe3+)=3:4
C. 反应中转移的电子数为0.04mol
D. n(Cu2+)=0.03mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】塑化剂是一种对人体有害的物质。增塑剂DCHP可由邻苯二甲酸酐与环己醇反应制得:

下列说法正确的是
A. DCHP的分子式为C20H24O4
B. 环己醇分子的核磁共振氢谱有4个吸收峰
C. DCHP能发生加成反应和取代反应,不能发生酯化反应
D. 1mol DCHP可与4mol NaOH完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用铁与水蒸气反应后的固体物质进行了如下实验:

(1)铁与水蒸气反应的化学方程式为______________________________________。
(2)加入试剂1后溶液呈淡红色,则淡黄色溶液中含有________(填离子符号)。加入试剂1后溶液呈红色的原因是(用离子方程式表示)________________。
(3)加入新制氯水后溶液红色加深的原因是(结合离子方程式说明) ___________________。
(4)一段时间后深红色溶液褪色的原因可能是①溶液中+3铁被氧化为更高的价态;②_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学计量在化学中占有重要地位。请回答下列问题:
(1)0.3 mol NH3分子中所含原子数与约__________个H2O分子中所含原子数相等。
(2)V mL含a g Al3+的Al2(SO4)3溶液中所含SO42的物质的量浓度为_____ mol·L1。
(3)在一定温度和压强下,1体积气体X2与3体积Y2化合生成2体积气态化合物,该化合物的化学式为_________。
(4)将各0.3 mol的钠、镁、铝分别放入100 mL 1 mol·L1的盐酸中,同温同压下产生气体的体积比为_____________。
(5)锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,当生成1 mol硝酸锌时,参加反应的硝酸的物质的量为_________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。请回答下列问题:
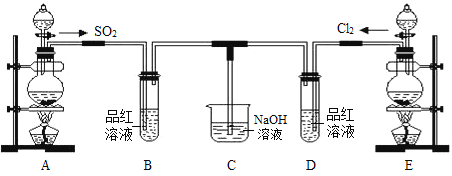
(1)实验室用装置E制备Cl2,其反应的化学方程式为MnO2+4HCl(浓) ![]() MnCl2 + Cl2↑ + 2H2O。将上述化学方程式改写为离子方程式_______________________________。
MnCl2 + Cl2↑ + 2H2O。将上述化学方程式改写为离子方程式_______________________________。
(2)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现__________的现象(填选项序号,下同)。
A.品红溶液都褪色 B.品红溶液都不褪色
C.B中品红溶液褪色,D中不褪色 D.D中品红溶液褪色,B中不褪色
②停止通气后,再给B、D两个试管分别加热,两个试管中的溶液呈现的颜色分别为________。
A.无色、红色 B.无色、无色 C.红色、红色 D.红色、无色
(3)C烧杯中氢氧化钠溶液的作用是_____________________________,写出Cl2通入NaOH溶液中的化学方程式_______________________________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按物质的量之比1︰1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请分析该现象的原因(用离子方程式表示)_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl溶液的电解产物可用于生产盐酸、漂白粉、氢氧化钠等产品。下列说法错误的是
A. HCl的电子式:![]()
B. NaOH中既含离子键又含共价键
C. 电解NaCl溶液时,阴极区pH增大的原因:2H2O +2e-=2OH-+H2↑
D. 漂白粉露置在空气中:Ca(ClO)2+CO2+H2O=CaCO3+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六氟化硫分子(如图)呈正八面体,难以水解,在电器工业方面有着广泛用途。下列有关SF6的推测正确的是( )
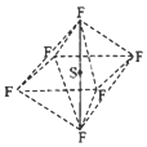
A. 高温条件下,SF6微弱水解生成H2SO4和HF
B. SF6易燃烧生成二氧化硫
C. SF6中各原子均达到 8 电子稳定结构
D. 六氟化硫分子中的S—F键都是σ键,键长、键能不完全相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道美国准备试验绿色航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,结构如图,它比肼燃烧释放能量更高,更安全、环保。下列说法不正确的是( )

A.羟基硝酸铵中各原子共平面
B.固态时羟基硝酸铵是离子晶体
C.羟基硝酸铵中含有离子键和共价键
D.9.6g羟基硝酸铵中含有0.2NA个离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com