
| A、① | B、①②④ |
| C、①②③ | D、①②③④ |


科目:高中化学 来源: 题型:

| 3 |
| 2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
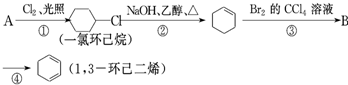
查看答案和解析>>
科目:高中化学 来源: 题型:
 全钒氧化还原液流电池是一种新型电能储存和高效转化装置,该电池是将具有不同价态的钒离子溶液分别作为正极和负极的活性物质,分别储存在各自的酸性电解液储罐中.其结构原理如图所示,该电池放电时,右槽中的电极反应为:V2+-e-═V3+,下列说法正确的是( )
全钒氧化还原液流电池是一种新型电能储存和高效转化装置,该电池是将具有不同价态的钒离子溶液分别作为正极和负极的活性物质,分别储存在各自的酸性电解液储罐中.其结构原理如图所示,该电池放电时,右槽中的电极反应为:V2+-e-═V3+,下列说法正确的是( )| A、放电时,右槽发生还原反应 |
| B、放电时,左槽电解液pH升高 |
| C、充电时,阴极的电极反应式:VO2++2H++e-═VO++H2O |
| D、充电时,每转移1mol电子,n(H+)的变化量为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、具有较高能量的分子是活化分子 |
| B、活化分子间的碰撞一定是有效碰撞 |
| C、反应的活化能大小不会影响化学反应速率 |
| D、不同化学反应需要的活化能有可能差别很大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用移液管移取10mL NaOH溶液并放于锥形瓶中,移液管的尖嘴和锥形瓶的内壁 |
| B、减压过滤时,布氏漏斗下端管口与吸滤瓶的内壁 |
| C、实验室将HCl气体溶于水时,倒扣的三角漏斗口与烧杯内的水面 |
| D、分液操作分出下层液体时,分液漏斗下端管口和烧杯的内壁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、产生的气体是0.2 mol NO2 |
| B、硝酸的物质的量浓度为12 mol?L-1 |
| C、反应中被还原和未被还原的硝酸物质的量之比为3:2 |
| D、要使产生的气体恰好完全被水吸收需要通入氧气0.075 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该元素原子处于能量最低状态时,原子中共有3个未成对电子 |
| B、该元素原子核外共有5个能级 |
| C、该元素原子的M能层共有18个电子 |
| D、该元素原子最外能层共有3个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com