
【题目】25℃时,将浓度均为0.1mol/L、体积分别为Va和Vb和的HX溶液与NH3·H2O溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示。下列说法不正确的是( )
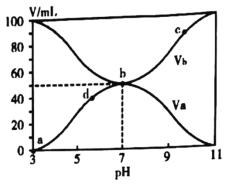
A.HX为弱酸
B.b点:![]()
C.b→c点过程中存在:![]()
D.c、d两点: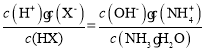 值相等
值相等
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F都是元素周期表中前36号的元素,它们的原子序数依次增大。A单质是密度最小的气体。B是周期表已知元素中非金属性最强的元素,且和C属同一主族。D、E、F属同一周期,D、F为主族元素,又知E、F的原子序数分别是29、33。D跟B可形成离子化合物,其晶胞结构如图:
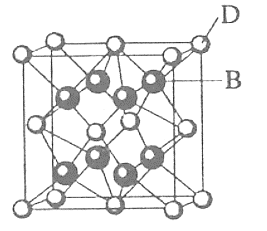
(1)比C元素质子数少1的原子的价层电子的轨道表示式为__________。
(2)E元素在周期表中第_____周期,第_____族的元素,它的+2价离子的电子排布式为________。写出E的单质与稀硝酸反应的离子方程式___________。
(3)F元素的名称是_____。与F同一主族的第二、三周期元素与A形成的化合物沸点的高低为___________>__________(用化学式表示),判断的理由____________。
(4)写出D跟A形成的化合物的电子式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将7.68g铜与50mL一定浓度的硝酸恰好完全反应,收集到标准状况下4.48L气体。
请回答:
(1)NO的体积为__L,NO2的体积为__L;
(2)被还原的硝酸的物质的量是__mol;
(3)硝酸的物质的量浓度是__mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知浓硫酸和木炭粉在加热条件下反应:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O,根据如图回答问题:
CO2↑+2SO2↑+2H2O,根据如图回答问题:
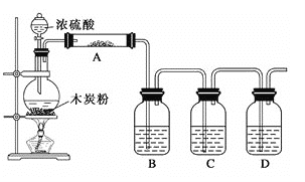
(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气?__。
(2)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
①A中加入的试剂是___,作用是___;
②B中加入的试剂是___,作用是___;
③C中加入的试剂是___,作用是___;
④D中加入的试剂是___,作用是___。
(3)实验时,C中应观察到的现象是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,水的电离达到平衡:H2O![]() H++OH- △H>0,下列叙述正确的是
H++OH- △H>0,下列叙述正确的是
A. 向水中加入少量固体硫酸氢钠,c (H+)增大,Kw不变
B. 向水中加入氨水,平衡逆向移动,c (OH-)降低
C. 向水中加入金属钠,平衡逆向移动,c (H+)减小
D. 将水加热,Kw增大,pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氨的叙述中不正确的是( )
A. 氨分子中氮元素的化合价只能升高,氨具有还原性
B. 氨的催化氧化反应的化学方程式是4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
C. 氨的催化氧化反应中若氧气过量则有红棕色气体生成
D. 氨的催化氧化属于人工氮的固定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“磷酸氯喹”是抗击新型冠状病毒的潜在药物,其合成路线如下:
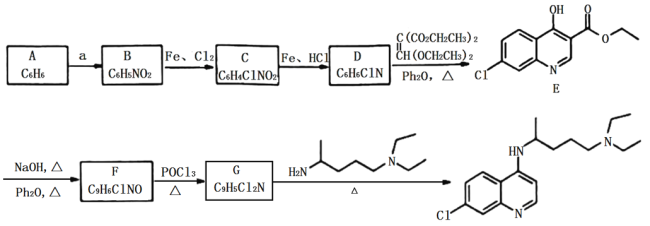
已知: 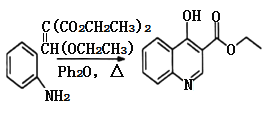
![]()

(1)A是一种芳香烃,试剂a为:____________________。
(2)B反应生成C的反应化学方程式为____________________。
(3)由C生产D和由F生成G的反应类型分别为__________、___________。
(4)D的结构简式为_________。
(5)E中含氧官能团的名称为________。
(6)I与E互为同分异构体,且具有完全相同的官能团,符合下列条件的I有____种。(不考虑立体异构)
①分子结构中含有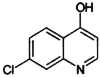 ;②分子中环状结构上只有三个取代基。写出其中任意两种结构简式____、______。
;②分子中环状结构上只有三个取代基。写出其中任意两种结构简式____、______。
(7)有机物J(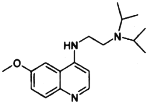 )是治疗血吸虫病的药物,参照上述
)是治疗血吸虫病的药物,参照上述![]() 的合成路线,设计由4-甲氧基苯氨(
的合成路线,设计由4-甲氧基苯氨(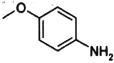 )和N,N-二异丙基乙二胺(
)和N,N-二异丙基乙二胺(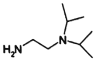 )为起始原料制备有机J的合成路线_______________________(无机试剂任意选用)。
)为起始原料制备有机J的合成路线_______________________(无机试剂任意选用)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学反应方程式为
H2(g)+![]() O2(g)=H2O(l) △H1
O2(g)=H2O(l) △H1
C(s)+O2(g)=CO2(g) △H2
CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H3
2C(s)+2H2(g)+O2(g)=CH3COOH(l) △H4
则△H4的正确表达式为
A. △H3-2△H1-2△H2B. 2△H1+2△H2-△H3
C. 2△H1-2△H2+△H3D. 2△H1-2△H2-△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向10mL0.1mol/LCuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,已知:lg2=0.3,Ksp(ZnS)=3×10-25mol2/L2,下列有关说法正确的是( )

A.a、b、c三点中,水的电离程度最大的为b点
B.如不考虑CuS的溶解,则c点溶液有:2[c(S2-)+c(HS-)+c(H2S)]═c(Cl-)
C.该温度下Ksp(CuS)=2×10-18mol2/L2
D.该温度下,反应:![]() 的平衡常数为
的平衡常数为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com