

���� ��1��������裺����������ϡ�Ȼ�������Һ�У�����1��2��Һ�壬���������ӱ��嵥������Ϊ��������ˮ��Һ���ǻ�ɫ�ģ������嵥������ˮ�γɵ���Һ��ɫ��
���ʵ�鷽������Һ��ɫ���ܽ��嵼�£������������Ȼ�̼��ȡ����֤��
��Һ��ɫ��Fe3+���£�����KSCN��Һ��Ӧ����Ѫ��ɫ���ʣ�
��2���嵥�������Խ�ǿ���ܽ�������������ΪFe3+��
�嵥�ʡ�Fe3+���Խ�����������Ϊ�ⵥ�ʣ�
��3��Fe3+���Խ�����������Ϊ�ⵥ�ʣ�����������ԭ��Ӧ����ʯī���缫���������ҺΪ�Ȼ�����Һ��KI��Һ����KCl�������ӣ�
��� �⣺��1����������衿����1����Һ�ʻ�ɫ���Ƿ�����ѧ��Ӧ���£�����Һ��Br2����ģ�
����2����Һ�ʻ�ɫ�Ƿ�����ѧ��Ӧ���£�����Һ��Fe3+����ģ�
�ʴ�Ϊ��Br2��Fe3+��
�����ʵ�鷽��������1���������ɫ��Һ����CCl4�������ã��²���Һ�ʳȺ�ɫ��
����2���������ɫ��Һ�μ�KSCN��Һ����Һ��ΪѪ��ɫ��
�ʴ�Ϊ�����ɫ��Һ����CCl4�������ã��²���Һ�ʳȺ�ɫ�����ɫ��Һ�μ�KSCN��Һ����Һ��ΪѪ��ɫ��
��2���嵥�������Խ�ǿ���ܽ�������������ΪFe3+������1������������2���ƶ���ȷ��
�嵥�ʡ�Fe3+���Խ�����������Ϊ�ⵥ�ʣ������õ��۵⻯����Һ��֤��
�ʴ�Ϊ������2����
��3��Fe3+���Խ�����������Ϊ�ⵥ�ʣ���Ӧ���ӷ���ʽΪ��2Fe3++2I-=2Fe2++I2������������ԭ��Ӧ����ʯī���缫���������ҺΪ�Ȼ�����Һ��KI��Һ����KCl�������ӣ����װ��ʾ��ͼΪ��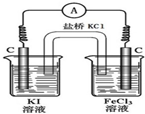 ��
��
�ʴ�Ϊ��2Fe3++2I-=2Fe2++I2�� ��
��
���� ���⿼���������ʵ�̽�����������ʵ��������ʵ�鷽������������Ԫ�ػ��������ʣ�ע�����������װ�õļ滭��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
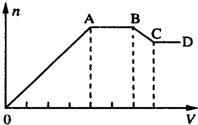 ij��Һ�У����ܺ����±����������е�ij���֣�
ij��Һ�У����ܺ����±����������е�ij���֣�| ������ | Al3+��Mg2+��NH4+��Na+ |
| ������ | CO32-��SiO32-��[Al��OH��4]-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
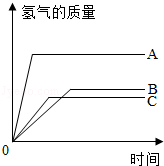
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
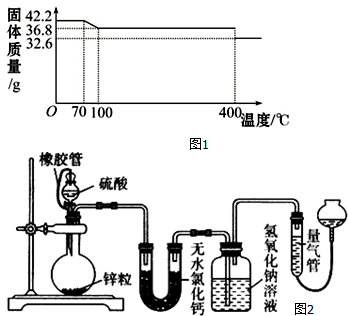
| ʵ�� ��Һ | A | B | C | D | E |
| 5mol/LH2SO4 mL | 40 | V1 | V2 | V3 | V4 |
| ����CuSO4Һ mL | 0 | 1 | 2 | V5 | 10 |
| H2O mL | V6 | V7 | V8 | 5 | 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 51.2% | B�� | 36.8% | C�� | 41.5% | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 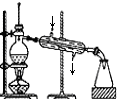 ��ˮ����õ���ˮ | |
| B�� | 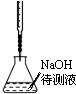 �к͵ζ� | |
| C�� | 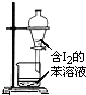 ����ȡ��ˮ��I2���ֳ�ˮ���IJ��� | |
| D�� | 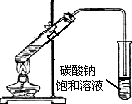 �Ʊ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���������ᷴӦ�Ļ�ѧ����ʽΪK4Fe��CN��6+6H2SO4+6H2O$\frac{\underline{\;\;��\;\;}}{\;}$2K2SO4+FeSO4+3��NH4��2SO4+6CO��
���������ᷴӦ�Ļ�ѧ����ʽΪK4Fe��CN��6+6H2SO4+6H2O$\frac{\underline{\;\;��\;\;}}{\;}$2K2SO4+FeSO4+3��NH4��2SO4+6CO���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
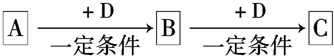
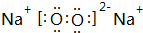 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com