
下列有关物质性质的描述和该性质的应用均正确的是
A.氨气具有氧化性,用浓氨水检验氯气管道是否泄漏
B.铜的金属活泼性比铁的弱,可在铁闸上装若干铜块以减缓其腐蚀
C.二氧化硫具有还原性,用二氧化硫水溶液吸收溴蒸气
D.二氧化锰具有较强的的氧化性,可作H2O2分解的氧化剂
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015广东省高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列关于煤、石油、天然气等资源的说法正确的是
A.石油裂解得到的汽油是纯净物
B.石油产品都可用于聚合反应
C.天然气是一种清洁的化石燃料
D.水煤气是通过煤的液化得到的气体燃料
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市秦安县高三第一次模拟考试化学试卷(解析版) 题型:填空题
(14分)锌是一种常用金属,冶炼方法有火法和湿法。
I.镓(Ga)是火法冶炼锌过程中的副产品,镓与铝同主族且相邻,化学性质与铝相似。氮化镓(GaN)是制造LED的重要材料,被誉为第三代半导体材料。
(1)Ga的原子结构示意图为____________________。
(2)GaN可由Ga和NH3在高温条件下合成,该反应的化学方程式为______________
(3)下列有关镓和镓的化合物的说法正确的是____________________(填字母序号)。
A.一定条件下,Ga可溶于盐酸和氢氧化钠
B.常温下,Ga可与水剧烈反应放出氢气
C.Ga2O3可由Ga(OH)3受热分解得到
D.一定条件下,Ga2O3可与NaOH反应生成盐
II.工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO等氧化物)湿法制取金属锌的流程如图所示,回答下列问题:

已知:Fe的活泼性强于Ni
(4)ZnFe2O4可以写成ZnO·Fe2O3,写出ZnFe2O4与H2SO4反应的化学方程式_______________________。
(5)净化I操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,只使Fe3+转化为Fe(OH)3沉淀。净化I生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是_____________________________________________________。
(6)净化II中加入Zn的目的是______________________________________________。
(7)常温下,净化I中,如果要使c(Fe3+) < 10-5 mol/L,则应控制溶液pH的范围为_______________________。已知:Ksp[Fe(OH)3] = 8.0 × 10-38;lg5 = 0.7
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高三第一次诊断考试理综化学试卷(解析版) 题型:选择题
分子式为C4Hl0烷烃与氯气在光照条件下发生取代反应,生成物中含有两个氯原子且位于相邻碳原子上的同分异构体共有
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省六校联盟高三第三次联考理科综合化学试卷(解析版) 题型:推断题
(16分)香豆素是用途广泛的香料,合成香豆素的路线如下(其他试剂、产物及反应条件均省略):

(1)Ⅰ的分子式为 ;1molⅠ与足量氧气完全燃烧消耗氧气的物质的量为 mol。
(2)物质Ⅳ中含氧官能团的名称 ,反应④的反应类型是 。
(3)香豆素在过量NaOH溶液中完全反应的化学方程式为 。
(4)Ⅴ是香豆素的同分异构体,写出符合下列条件的Ⅴ的结构简式 。
①苯环上只有两个处于对位的取代基②能使氯化铁溶液呈紫色 ③能发生银镜反应
(5)一定条件下,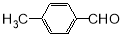 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 。
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省皖北协作区高三3月联考理综化学试卷(解析版) 题型:实验题
(14分)锡酸钠(NaBiO3)常用作Mn2十鉴定的强氧化剂。某研究小组用浮选过的辉铋矿(主要成分是Bi2S3.还含少量Bi2O3, SiO2等杂质)制备铋酸钠,其流程如下:
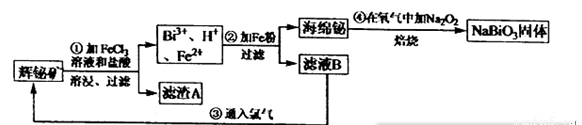
己知:①铋酸钠是一种难溶于水的物质;②BiC13极易水解生成不溶性的BiOCl沉淀,在浓盐酸中几乎不水解;FeC13溶液开始沉淀的pH值为2.7,沉淀完全时的pH值为3.7。
请回答下列问题:
(1)为了提高溶浸工序中原料的浸出率,可以采取的措施 (选滨字母序号)。
a.加入足量的蒸馏水 b.搅拌 c.粉碎矿石 d.升高温度
(2)溶浸时通常加入FeC13溶液和浓盐酸,向其中加入过量浓盐酸的目的是 。
滤渣A的主要成分为 。
(3)铋酸钠可在酸性介质中将Mn2+氧化为MnO4一,故可用于M2+的鉴定。已知NaBiO3被还原为Bi3+试写出该反应的离子方程式: 。
(4)实验室为了测定NaBiO3样品的纯度,需要配制250mL 2.0mo1L-1,FeSO4溶液,所需要的玻璃仪器除烧杯、量筒、玻璃棒外,还需要 、 配制2.0 mo1L-1FeSO4溶液定容时具体的操作步骤为 。
(5)取上述NaBiO3样品10.0g,加入稀硫酸和MnSO4溶液使其完全溶解,然后用新配制的2.0 mo1L-1FeSO4;溶液对生成的MnO4一进行滴定,滴定完成后消耗31.00mL FeSO4溶液。则该样品中NaBiO3纯度为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省皖北协作区高三3月联考理综化学试卷(解析版) 题型:选择题
硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,下列有关说法正确的是
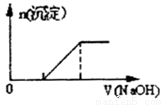
A.Na+、Fe3+、NO3-、Cl2都可在该物质的溶液中大量共存
B.向0.1mo1/L该物质的溶液中清加0.L/molNaOH溶液,生成沉淀的物质的量与逐滴加入NaOH溶液体积关系如上图所示
C.检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色
D.向该物质的溶液中摘加Ba(OH)2溶液,恰好使SO42--完全沉淀的离子方程式为:Fe2++2SO42-+2Ba2++2OH-=2BaSO4↓+Fe(OH)2↓
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省上饶市高三上学期第一次联考化学试卷(解析版) 题型:填空题
(15分)2013年以来,我国多地频现种种极端天气。二氧化碳、氮氧化物、二氧化硫是导致极端天气的重要因素。
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解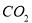 ,发生反应:
,发生反应: =2CO(g)+
=2CO(g)+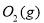 △H>0,该反应的
△H>0,该反应的 S 0(填“>”“<”或“=”),在低温下,该反应 (填“能”或“不能”)自发进行。
S 0(填“>”“<”或“=”),在低温下,该反应 (填“能”或“不能”)自发进行。
(2)活性炭可用于处理大气污染物NO。在1 L恒容密闭容器中加入0.100 mol NO和2.030 mol固体活性炭(无杂质),生成气体E和气体F。当温度分别在 和
和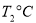 时,测得平衡时各物质的物质的量如下表:
时,测得平衡时各物质的物质的量如下表:
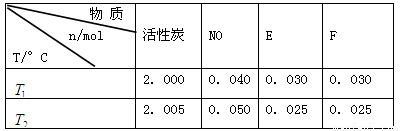
①请结合上表数据,写出NO与活性炭反应的化学方程式: 。
②上述反应在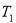 ℃时的平衡常数为
℃时的平衡常数为 ,在
,在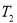 ℃时的平衡常数为
℃时的平衡常数为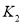 。
。
计算 = 。根据上述信息判断,
= 。根据上述信息判断, 和
和 的关系是 。
的关系是 。
a.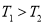 b.
b.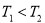 c.无法比较
c.无法比较
③在 ℃下反应达到平衡后,下列措施不能改变NO的转化率的是____。
℃下反应达到平衡后,下列措施不能改变NO的转化率的是____。
a.增大c(NO) b.增大压强 c.升高温度 d.移去部分F
(3)碘循环工艺不仅能吸收 降低环境污染,同时又能制得氢气,具体流程如下:
降低环境污染,同时又能制得氢气,具体流程如下:
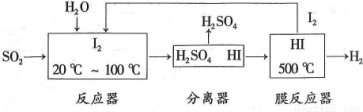
①用离子方程式表示反应器中发生的反应 。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出 的目的是: 。
的目的是: 。
(4)开发新能源是解决大气污染的有效途径之一。直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC工作原理如图所示:
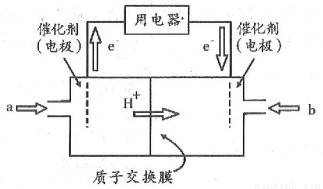
通过a气体的电极是原电池的 极(填“正”或“负”),其电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期末考试化学试卷(解析版) 题型:选择题
下列有关物质的性质与应用的对应关系正确的是
A.碳酸钠溶液显碱性,用热的碳酸钠溶液可去除金属表面的油污
B.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
C.铝的熔点很高,可用于制作耐高温材料
D.浓硫酸具有吸水性,可用于干燥氨气、二氧化碳等气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com