
某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)  Z(g)+W(s);ΔH>0
Z(g)+W(s);ΔH>0
下列叙述正确的是( )
A.加入少量W,逆反应速率增大 B.当容器中气体压强不变时,反应达到平衡
C.升高温度,平衡逆向移动 D.平衡后加入X,上述反应的ΔH增大
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源:2017届山东省新泰市高三上学期第一次阶段考化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.将铜插入稀硝酸中:Cu+4H++2NO3 -=Cu2++2NO2↑+H2O
B.向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe=2Fe3+
C.向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3﹒H2O=Al(OH)3↓+3NH4+
D.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+3Na+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上第一次月考化学试卷(解析版) 题型:选择题
有等体积、等pH的Ba(OH)2、KOH和NH3·H2O三种碱溶液,滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是( )
A.V3>V2>V1 B.V3=V2=V1 C.V3>V2=V1 D.V1=V2>V3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上第一次月考化学试卷(解析版) 题型:选择题
一定温度下,水中存在H2O?H++OH- △H>0的平衡,下列叙述一定正确的是
A.向水中滴入少量稀盐酸,平衡逆向移动,Kw减小
B.将水加热,Kw增大,pH减小
C.向水中加入少量CH3COONa固体,平衡逆向移动,c(H+)降低
D.向水中加入少量Na2SO4固体,平衡不移动,c(H+)一定为10-7 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东实验中学顺德学校高二上阶段质检化学试卷(解析版) 题型:选择题
在某容积一定的密闭容器中,有下列可逆反应:A(g)+B(g)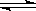 xC(g)ΔH未知,有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )
xC(g)ΔH未知,有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )

A.P3<P4,y轴表示A的转化率
B.P3<P4,y轴表示B的体积分数
C.P3<P4,y轴表示混合气体的密度
D.P3>P4,y轴表示混合气体的平均摩尔质量
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东实验中学顺德学校高二上阶段质检化学试卷(解析版) 题型:选择题
100℃时,将0.1 mol N2O4置于1 L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) 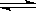 2NO2 (g)。下列结论
2NO2 (g)。下列结论 不能说明上述反应在该条件下已经达到反应限度的是 ( )
不能说明上述反应在该条件下已经达到反应限度的是 ( )
A.N2O4的消耗速率与NO2的生成速率之比为1∶2
B.烧瓶内气体的颜色不再加深
C.烧瓶内气体的平均相对分子质量不再变化
D.烧瓶内气体的压 强不再变化。
强不再变化。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高一上第一次学段考试化学卷(解析版) 题型:实验题
下面是用98%的浓H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的稀H2SO4500ml的操作,实验操作如下,
①将配好的稀硫酸倒入试剂瓶中,贴好标签;
②盖好容量瓶塞,反复颠倒摇匀;
③用量筒量取 ml的98% 的浓硫酸;
④将浓硫酸稀释;
⑤用少量蒸馏水洗涤烧杯2~3次,并将洗涤液也全部转移到容量瓶中;
⑥将已冷却至室温的硫酸溶液沿玻璃棒注入 __________;
⑦改用__________ 逐滴加蒸馏水,使溶液的____________ 正好跟刻度相平。
⑧继续向容量瓶中加蒸馏水,直到液面接近刻度线1~2cm处;
请完成下列问题:
(1)正确操作步骤的顺序是(填序号)③④ ⑦②①
(2)③中所需浓硫酸的体积 ml,⑥中所需仪器名称是 。
(3)简述④中浓硫酸的稀释方法 。
(4)完成⑦中的填空 、 。
(5)若在操作中没有把少量洗涤烧杯的洗涤液全部转移到容量瓶中,会使稀硫酸溶液的浓度(填“大于”、“小于”或“等于”) 0.5mol/L,配制成稀H2SO4时若加蒸馏水超过了刻度线,倒出一些溶液,再重新加蒸馏水到刻度线,会使稀硫酸溶液的浓度 (填“大于”、“小于”或“等于”) 0.5mol/L.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上第一次月考化学试卷(解析版) 题型:填空题
在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g) X(g) △H=-dkJ·mol-1(d>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
X(g) △H=-dkJ·mol-1(d>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
实验 | 甲 | 乙 | 丙 |
初始投料 | 2 molA2、1 molBC | 1 molX | 4 molA2、2 molBC |
平衡时n(X) | 0.5mol | n2 | n3 |
反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
体系的压强 | P1 | P2 | P3 |
反应物的转化率 | α1 | α2 | α3 |
(1)在该温度下,假设甲容器从反应开始到平衡所需时间为4 min,则该时间段内A2的平均反应速率v(A2) 。
(2)该温度下此反应的平衡常数K的值为 。
(3)三个容器中的反应分别达平衡时各组数据关系正确的是 (填序号)。
A.α1+α2=1
B.Q1+Q2=d
C.α3<α1
D.P3<2P1=2P2
E.n2<n3<1.0mol
F.Q3=2Q1
(4)在其他条件不变的情况下,在第5min将甲容器的体系体积压缩到1L,若在第8min达到新的平衡时A2的总转化率为65.5%,请在下图中画出第5min到新平衡时X的物质的量浓度的变化曲线。
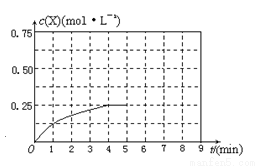
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市如东县徐州市丰县高三10月联考化学卷(解析版) 题型:选择题
建设“碧水蓝天”的生态城市,下列措施中不合理的是
A.大力实施矿物燃料“脱硫、脱硝技术”,减少硫的氧化物和氮的氧化物污染
B.积极推广太阳能、风能等新能源的使用,减少化石燃料的使用
C.加强城市生活污水脱氮除磷处理,遏制水体富营养化
D.加高烟囱,减少烟尘对周围环境的影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com