
����Ŀ��ij�о���ѧϰС��Ϊȷ��һ�ִ�ú����ȡ��Һ̬��X����ɣ��������̽����
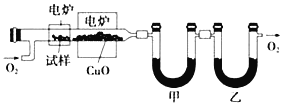
ʵ�鲽�����£�
![]() ������װ��ͼ���Ӻø�����������װ�õ������ԡ�
������װ��ͼ���Ӻø�����������װ�õ������ԡ�
![]() ��װ����ͨ��������һ��ʱ���������¯�ﵽһ���¶ȣ��л���X����������ͨ�����ȵ�����ͭ����������ַ�Ӧ��
��װ����ͨ��������һ��ʱ���������¯�ﵽһ���¶ȣ��л���X����������ͨ�����ȵ�����ͭ����������ַ�Ӧ��
![]() ���ɵ���������ͨ���ס�������U�ιܱ���ȫ���ա�
���ɵ���������ͨ���ס�������U�ιܱ���ȫ���ա�
![]() �رյ�¯��һ��ʱ���ֹͣͨ����������üס�������U�ι����طֱ�Ϊ
�رյ�¯��һ��ʱ���ֹͣͨ����������üס�������U�ι����طֱ�Ϊ![]() ��
��![]() ��
��
![]() ͨ�������������X����Է�������Ϊ106��
ͨ�������������X����Է�������Ϊ106��
�ش��������⣺
![]() �ķ���ʽΪ______��
�ķ���ʽΪ______��
![]() ���е��Լ�Ϊ
���е��Լ�Ϊ![]() д��ѧʽ
д��ѧʽ![]() ______��ijͬѧ��Ϊ����װ�ò���������������______��
______��ijͬѧ��Ϊ����װ�ò���������������______��
![]() д��������������������X�Ľṹ��ʽ______��
д��������������������X�Ľṹ��ʽ______��
![]() ������
������![]() �����ϵ�һ�ȴ���������
�����ϵ�һ�ȴ���������
![]() �Դ���Ϊ�ܼ��ڴ�������������������X��ijһͬ���칹��õ���һ����Ҫ�Ļ���ԭ��PTA���������ϵ�֪PTA���ܽ�ȣ�
�Դ���Ϊ�ܼ��ڴ�������������������X��ijһͬ���칹��õ���һ����Ҫ�Ļ���ԭ��PTA���������ϵ�֪PTA���ܽ�ȣ�![]() ʱ
ʱ![]() ��
��![]() ʱ
ʱ![]() ��
��![]() ʱ
ʱ![]() ���õ��Ĵֲ�Ʒ���в��ֲ��������ʣ��ᴿPTA��Ʒ��ʵ�鲽��Ϊ����PTA��Ʒ����������ˮ��______��______�����ˡ�ϴ�ӡ����
���õ��Ĵֲ�Ʒ���в��ֲ��������ʣ��ᴿPTA��Ʒ��ʵ�鲽��Ϊ����PTA��Ʒ����������ˮ��______��______�����ˡ�ϴ�ӡ����
���𰸡�![]()
![]() �����е�
�����е�![]() ��
��![]() Ҳ���ܽ������У��Բⶨ�����������
Ҳ���ܽ������У��Բⶨ����������� ![]() ��
�� ���ȹ��� ���½ᾧ
���ȹ��� ���½ᾧ
��������
ʽ����������ȼ�գ������ɶ�����̼��ˮ��������CO������CuO��Ӧ���ɶ�����̼����Ϊ�Ȼ��ƣ�����������ˮ����Ϊ��ʯ�ң��������ն�����̼����װ�ú�Ӧ���������տ����е�![]() ��
��![]() ��װ�ã��������ʵ�������ɶ�����̼Ϊ
��װ�ã��������ʵ�������ɶ�����̼Ϊ![]() ������ˮΪ
������ˮΪ![]() ����n(C)��
����n(C)��![]() ��
��![]() ��5�������ʽΪ
��5�������ʽΪ![]() ����
����![]() ��
��![]() ������ʽΪ
������ʽΪ![]() ����Ϊ���������ұ����ϵ�һ�ȴ��������֣���ӦΪ�ұ������ױ����Դ˽����⡣
����Ϊ���������ұ����ϵ�һ�ȴ��������֣���ӦΪ�ұ������ױ����Դ˽����⡣
![]() �����Ϸ�����֪���ɶ�����̼Ϊ
�����Ϸ�����֪���ɶ�����̼Ϊ![]() ������ˮΪ
������ˮΪ![]() ����n(C)��
����n(C)��![]() ��
��![]() ��5�������ʽΪ
��5�������ʽΪ![]() ����
����![]() ��
��![]() ������ʽΪ
������ʽΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
![]() ��Ϊ�Ȼ��ƣ�����������ˮ����Ϊ��ʯ�ң��������ն�����̼����װ�ú�Ӧ���������տ����е�
��Ϊ�Ȼ��ƣ�����������ˮ����Ϊ��ʯ�ң��������ն�����̼����װ�ú�Ӧ���������տ����е�![]() ��
��![]() ��װ�ã��������ʵ�����ʴ�Ϊ��
��װ�ã��������ʵ�����ʴ�Ϊ��![]() �������е�
�������е�![]() ��
��![]() Ҳ���ܽ������У��Բⶨ����������ţ�
Ҳ���ܽ������У��Բⶨ����������ţ�
![]() ��ͬ���칹���������������
��ͬ���칹���������������![]() ��������
��������![]() ������һ�ȴ��������֣�����������ͬ���칹���У�
������һ�ȴ��������֣�����������ͬ���칹���У�![]() ��
�� ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
�� ��
��
![]() ���ܽ�����¶����߶�����Ҵֲ�Ʒ�����ʲ�����ˮ���ᴿPTA��ʵ�鷽�������ֲ�Ʒ����������ˮ�У����ȹ��˳����������ʣ���Һ��ȴ�ᾧ�����˳����壬�ʴ�Ϊ�����ȹ��ˣ����½ᾧ��
���ܽ�����¶����߶�����Ҵֲ�Ʒ�����ʲ�����ˮ���ᴿPTA��ʵ�鷽�������ֲ�Ʒ����������ˮ�У����ȹ��˳����������ʣ���Һ��ȴ�ᾧ�����˳����壬�ʴ�Ϊ�����ȹ��ˣ����½ᾧ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ャҺ��Al(OH)3��MnO2������Na2CrO4�����ǵ��������������ʹNa2CrO4������ȫ��ˮ������ij�о�С��������Ƶĵ�����װ�ã���ͼ2����ʹ��Һ����ɹ�������ͺ���Ԫ����Һ�����������á��ش��͢��е����⡣

��������ķ�������ã�����ͼ�еIJ��ַ�������ͷ�Ӧ����δ������
��1����Ӧ�������Լ�NaOH�ĵ���ʽΪ_________��B��C�ķ�Ӧ����Ϊ__________��C��Al���Ʊ�������Ϊ______________��
��2����С��̽����Ӧ�ڷ�����������D��Ũ�����ϣ������ȣ��ޱ仯��������Cl2���ɣ�����Ӧֹͣ������ʣ�࣬��ʱ�μ����ᣬ�ֲ���Cl2���ɴ��ж�Ӱ��÷�Ӧ��Ч���е������У�����ţ�___________��
a���¶� b��Cl-��Ũ�� c����Һ�����
��3��0.1 mol Cl2�뽹̿��TiO2��ȫ��Ӧ������һ�ֻ�ԭ�������һ����ˮ���TiO2��xH2O��Һ̬���������4.28 kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ__________��
����Ԫ����Һ�ķ��������
��4���ö��Ե缫���ʱ��CrO42-�ܴӽ�Һ�з��������ԭ����__________�������Ԫ�ص�������_________�����������ɵ�����Ϊ___________��д��ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ĩ����FeSO4��Fe2(SO4)3��CuSO4��CaCO3��SiO2��NaCl�е���������ɣ�ȡһ�����Ĺ����������ʵ�飺
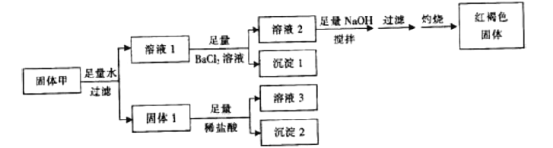
����1����Ϊ11g������1����Ϊ23.3g������2����Ϊ6g�����ɫ��������Ϊ8g������˵����ȷ����( )
A. ��Һ�����KSCN��Һ�ʺ�ɫ
B. ȡ������Һ2�����ữ����������Һ�����ɰ�ɫ�����������һ����NaCl
C. �������ϡ���ᷴӦʱ�������˱�״��������1.12L
D. ����2�������κ�����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ�ϲ��ᾧ�����ɿɱ�ʾΪ![]() ��Ϊ�ⶨx��ֵ����������ʵ�飺
��Ϊ�ⶨx��ֵ����������ʵ�飺
![]() ��ȡWg�����ᾧ�壬�������Ƴ�100mLˮ��ҺΪ����Һ��
��ȡWg�����ᾧ�壬�������Ƴ�100mLˮ��ҺΪ����Һ��
![]() ȡ25mL����Һ������ƿ�У��ټ���������ϡ
ȡ25mL����Һ������ƿ�У��ټ���������ϡ![]() ��
��
![]() ��Ũ��Ϊa
��Ũ��Ϊa![]() ��
��![]() ����Һ���еζ�
����Һ���еζ�![]() �ζ���������
���������![]() ��
��![]() ����
����![]() ��
��
��ش�(1)д���ζ�ʱ�����ķ�Ӧ�����ӷ���ʽΪ��______��
(2)�ζ�ʱ����![]() ��Һװ�� ______ ʽ�ζ����С�
��Һװ�� ______ ʽ�ζ����С�
(3)����ζ��յ�ʱ����ȥVmL![]() ��Һ������������Һ�����ʵ���Ũ��Ϊ ______
��Һ������������Һ�����ʵ���Ũ��Ϊ ______ ![]() ��
��
(4)������ʵ���У����в���![]() ����������ȷ
����������ȷ![]() ����ɲⶨ���xֵƫ�ߵ��� ______
����ɲⶨ���xֵƫ�ߵ��� ______ ![]() ����ĸ
����ĸ![]() ��
��
A.�ζ��յ����ʱ���Ӷ���![]() ��ʽ�ζ���ʹ��ǰ��ˮϴ��δ�ñ�Һ��ϴ
��ʽ�ζ���ʹ��ǰ��ˮϴ��δ�ñ�Һ��ϴ
C.��ƿˮϴ�����ô���Һ��ϴ![]() �ζ�ʱ���õ�
�ζ�ʱ���õ�![]() ��Һ����ö�����Ũ�ȱ�С��
��Һ����ö�����Ũ�ȱ�С��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����õ�����ࣨ��Ҫ����Fe2O3��CuO��Cr2O3�������������ʣ�����ͭ���Ƚ�����������������ͼ��
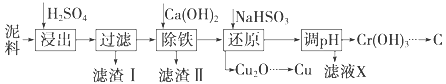
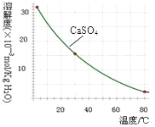
��֪�������ʳ�����pH��CaSO4���ܽ���������£�
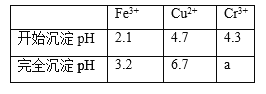
��1���ڽ��������г�������Fe2(SO4)3��Cr2(SO4)3�⣬��Ҫ����_____
��2���ڳ��������У���Ҫ��ȥFe3+��CaSO4���������ز������ټ���ʯ�������pH��__���ڽ���Һ���ȵ�80�棬______��
��3��д����ԭ�����м���NaHSO3����Cu2O��������ӷ�Ӧ����ʽ___________���˲����м���NaHSO3�õ�Cu2O�IJ���Ϊ95%����NaHSO3�����������˷��Լ��⣬������ֵ�������________��
��4��������Ũ����1��10��5 molL��1��Ϊ������ȫ����ҪʹCr3+��ȫ������Ҫ����c��OH������_______����֪��Ksp[Cr(OH)3]=6.3��10��31��![]() ��4.0��
��4.0��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ѧ��.���й��������е�������Ͳ���������
A.ʳ�β��������� ��Ȼ���Ļ�����,�۲쵽��ɫ����,��ԭ��:2Na+O2![]() Na2O2
Na2O2
B.մˮ������Ʒ����������ջᷢ�ڣ������ԭ��3Fe+4H2O![]() Fe3O4+4H2
Fe3O4+4H2
C.Al(OH)3�������к����θ�ᣬ��ԭ��Al(OH)3+3HCl=AlCl3+3H2O
D.�������Ծ�ˮ������Ϊ����[KAl(SO4)2��H2O]����ˮ������Al(OH)3����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���1 L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ������������ȷ����
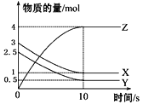
A.��Ӧ�Ļ�ѧ����ʽΪ2X��g��+Y��g��![]() 2Z��g��
2Z��g��
B.��Ӧ��ʼ��10 s����Z��ʾ�ķ�Ӧ����Ϊ0.3 mol��L-1��s-1
C.10 s�÷�Ӧֹͣ����
D.��Ӧ��ʼ��10 sʱ����Ӧ���ʣ�����X��=����Y��=0.2 mol��L-1��s-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼����������һ����Ҫ�����Ӽ�����ṹ��ʽΪ![]() ���û�������ϳ�̼���������ķ�ӦΪ��
���û�������ϳ�̼���������ķ�ӦΪ��![]() ������˵���������
������˵���������
A.������Ӧ���ڼӳɷ�Ӧ
B.̼���������Ķ��ȴ���ֻ������
C.̼���������е�����ԭ�Ӵ���ͬһƽ����
D.1mol̼����������������2molNaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ijˮ��Һ�е�![]() ��
��![]() Ũ�ȱ仯������ͼ��ʾ������˵������ȷ����
Ũ�ȱ仯������ͼ��ʾ������˵������ȷ����
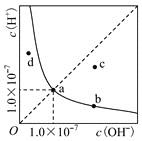
A.������ˮ�м���NaOH�������ܽ��ָ������£���Һ���տ�������b��
B.![]() ��HCl�Ļ����Һ��ˮ�������
��HCl�Ļ����Һ��ˮ�������![]() Ũ�ȿ��ܵ���d������
Ũ�ȿ��ܵ���d������
C.��b���ʾ��NaR��ˮ��Һ����������ε��������HR��Һ��������b��c�ı仯
D.��c���ʾij�¶�����NaHA��ˮ��Һ����![]()
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com