
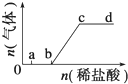
 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )| A. | a点对应的溶液中:Na+、OH-、SO42-、NO3- | |
| B. | b点对应的溶液中:Al3+、Fe3+、SCN-、Cl- | |
| C. | c点对应的溶液中:Na+、Ca2+、NO3-、Cl- | |
| D. | d点对应的溶液中:SO32-、Na+、Cl-、NO3- |
分析 向Na2CO3、NaHCO3,a点溶液中含有CO32-和HCO3-,b点全部为HCO3-,c点恰好完全反应生成NaCl,溶液呈中性,d点盐酸过量,呈酸性,结合对应离子的性质解答该题.
解答 解:向Na2CO3、NaHCO3,a点溶液中含有CO32-和HCO3-,b点全部为HCO3-,c点恰好完全反应生成NaCl,溶液呈中性,d点盐酸过量,呈酸性,
A.a点溶液中含有CO32-和HCO3-,HCO3-与OH-反应不能大量共存,故A错误;
B.b点全部为HCO3-,Al3+、Fe3+与HCO3-发生互促水解反应而不能大量共存,故B错误;
C.c点恰好完全反应生成NaCl,溶液呈中性,离子之间不发生任何反应,可大量共存,故C正确;
D.d点呈酸性,酸性条件下,NO3-与SO32-发生氧化还原反应而不能大量共存,故D错误.
故选C.
点评 本题考查离子共存问题,为高考常见题型,侧重于元素化合物知识的综合考查和学生的分析能力、审题的能力的考查,注意把握常见离子的性质以及反应类型的判断,答题时注意题中各阶段溶液的成分,题目难度不大.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 现象 | 结论 |
| A | 将乙醇和苯配成相同物质的量浓度的水溶液 | 加入大小相同的金属钠,观察反应快慢 | 两者的羟基活性不同 |
| B | 向Na2SiO3溶液中通入CO2气体 | 溶液变浑浊 | 碳的非金属性比硅强 |
| C | 将过量的铁粉和氯气反应,将反应后的固体溶于盐酸后,滴加KSCN溶液 | 溶液不显红色 | 过量铁与氯气反应产物为FeCl2 |
| D | 向Al(SO4)3溶液中滴入氨水至过量 | 溶液先变浑浊后又澄清 | Al(SO4)3溶液既有酸性又有碱性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | C生成的速率与C分解的速率相等 | |
| B. | 单位时间内消耗a mol A,同时生成3a mol C | |
| C. | 容器内的压强不再变化 | |
| D. | 混合气体中B物质的量不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室以2一丁醇(
实验室以2一丁醇( )为原料制备2-氯丁烷
)为原料制备2-氯丁烷 ),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:
),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:| 物质 | 熔点 (℃) | 沸点(℃) |
| 2-丁醇 | -114.7 | 99.5 |
| 2-氯乙烷 | -131.3 | 68.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下,5L CH4气体与5L NH3气体的原子个数之比为5:4 | |
| B. | 常温常压下,11.2L O3中所含氧原子个数大于1.5NA | |
| C. | 同温、同压下,相同体积的N2和CO气体具有相同的分子数和相同的密度 | |
| D. | 同温、同压下,等质量的一氧化碳和二氧化碳的密度比为11:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用氯胺处理自来水:NH2Cl+H2O?NH2OH+HCl | |
| B. | 在含有Mg2+、HCO3-的自来水中加入过量的澄清石灰水:Ca2++Mg2++2OH-+2HCO3-═CaCO3↓+MgCO3↓+2H2O | |
| C. | 长时间煮沸含Mg2+、HCO3-的自来水:Mg2++2HCO3-$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+2CO2↑ | |
| D. | Na2FeO4既是混凝剂、又可作消毒剂,作混凝剂的作用原理为:Fe3++3H2O═Fe(OH)3(胶体)+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学学习小组发现在碱性溶液中,NO2会发生如下反应:
某化学学习小组发现在碱性溶液中,NO2会发生如下反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  分子中至少有9个碳原子处于同一平面上 分子中至少有9个碳原子处于同一平面上 | |
| B. |  的核磁共振氢谱有5个峰 的核磁共振氢谱有5个峰 | |
| C. | 某烯烃与氢气加成后得到2,2-二甲基丁烷,该烯烃的名称是3,3-二甲基-1-丁烯 | |
| D. | 能够测定分子化学键的方法是核磁共振谱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com