
·ÖĪö £Ø1£©¢Ł2Al2O3£Øs£©ØT4Al£Øg£©+3O2£Øg£©”÷H1=3351KJ•mol-1
¢Ś2C£Øs£©+O2£Øg£©ØT2CO£Øg£©”÷H2=-221KJ•mol-1
¢Ū2Al£Øg£©+N2£Øg£©ØT2AlN£Øs£©”÷H3=-318KJ•mol-1
øĒĖ¹¶ØĀɼĘĖć£¬£Ø¢Ł+¢Ś”Į3+¢Ū”Į2£©”Į$\frac{1}{2}$µĆµ½Ģ¼ČČ»¹ŌAl2O3ŗĻ³ÉAlNµÄ×ÜČČ»Æѧ·½³ĢŹ½£¬·“Ó¦×Ō·¢½ųŠŠµÄÅŠ¶ĻŅĄ¾ŻŹĒ”÷H-T”÷S£¼0£»
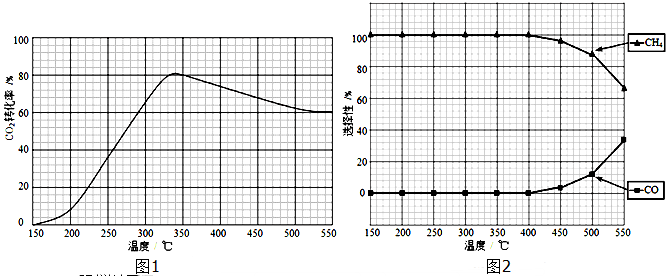
£Ø2£©¢ŁA£®Ķ¼ĻóÖŠ¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹĖęĪĀ¶ČÉżøß¼õŠ”£¬ĖµĆ÷Õż·“Ó¦ĪŖ·ÅČČ·“Ó¦£»
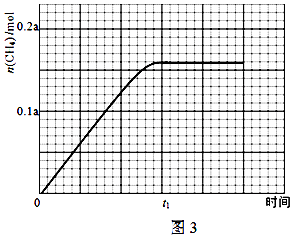
B£®Ķ¼Ļó2·ÖĪöĖęĪĀ¶ČÉżøßµ½400”ćCŅŌÉĻ£¬Ń”ŌńŠŌŹÜĪĀ¶ČÓ°Ļģ£»
C£®¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹĻČŌö“óŹĒ·“Ó¦ÕżĻņ½ųŠŠĪ““ļµ½Ę½ŗāדĢ¬£»
D£®Į½ÖÖ·“Ó¦ĪļŌö“óŅ»ÖÖ»įĢįøßĮķŅ»ÖÖµÄ×Ŗ»ÆĀŹ£¬±¾Éķ×Ŗ»ÆĀŹ¼õŠ”£»
¢Ś350”ꏱ£¬·“Ó¦¢ńŌŚt1Ź±æĢ“ļµ½Ę½ŗā£¬Ę½ŗāŹ±ČŻĘ÷Ģå»żĪŖVL£¬¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹĪŖ80%£¬½įŗĻČżŠŠ¼ĘĖć¼ĘĖćĘ½ŗāÅØ¶Č£¬K=$\frac{Éś³ÉĪļĘ½ŗāÅضČĆŻ“Ī·½³Ė»ż}{·“Ó¦ĪļĘ½ŗāÅضČĆŻ“Ī·½³Ė»ż}$£»
¢Ū·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ÉżĪĀĘ½ŗāÄęĻņ½ųŠŠ£¬¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹ¼õŠ”£¬Ķ¼ÖŠ·ÖĪöæÉÖŖ½Ó½ü72.5%£¬¼×ĶéĪļÖŹµÄĮæ¼õŠ”Š”ÓŚ350”ćCŹ±¼×ĶéĪļÖŹµÄĮ棬“ļµ½Ę½ŗāĖłŠčŅŖŹ±¼äĖõ¶Ģ£»
£Ø3£©CO2æÉŅŌŌŚ¼īŠŌĖ®ČÜŅŗÖŠµē½āÉś³É¼×Ķ飬½įŗĻµēŗÉŹŲŗćŗĶŌ×ÓŹŲŗć£¬ÓĆĒāŃõøłĄė×ÓÅضČÅäĘ½µēŗÉŹŲŗćµĆµ½µē¼«·“Ó¦£®
½ā“š ½ā£ŗ£Ø1£©¢Ł2Al2O3£Øs£©ØT4Al£Øg£©+3O2£Øg£©”÷H1=3351KJ•mol-1
¢Ś2C£Øs£©+O2£Øg£©ØT2CO£Øg£©”÷H2=-221KJ•mol-1
¢Ū2Al£Øg£©+N2£Øg£©ØT2AlN£Øs£©”÷H3=-318KJ•mol-1
øĒĖ¹¶ØĀɼĘĖć£¬£Ø¢Ł+¢Ś”Į3+¢Ū”Į2£©”Į$\frac{1}{2}$µĆµ½£¬
Ģ¼ČČ»¹ŌAl2O3ŗĻ³ÉAlNµÄ×ÜČČ»Æѧ·½³ĢŹ½£ŗ3C£Øs£©+Al2O3£Øs£©+N2£Øg£©=2AlN£Øs£©+3CO£Øg£©”÷H=+1026KJ/mol/L£¬·“Ó¦”÷S£¾0£¬”÷H£¾0£¬ŌņĀś×ć”÷H-T”÷S£¼0£¬·“Ó¦×Ō·¢½ųŠŠµÄĢõ¼žŹĒøßĪĀĢõ¼žĻĀ£¬
¹Ź“š°øĪŖ£ŗ3C£Øs£©+Al2O3£Øs£©+N2£Øg£©=2AlN£Øs£©+3CO£Øg£©”÷H=+1026KJ/mol/L£»øßĪĀ£»
£Ø2£©¢ŁA£®Ķ¼ĻóÖŠ£¬¶žŃõ»ÆĢ¼ĻČŌö“óŹĒ·“Ó¦ÕżĻņ½ųŠŠ£¬µ½Ņ»¶ØĪĀ¶Č“ļµ½Ę½ŗāדĢ¬£¬ÉżĪĀĘ½ŗāÄęĻņ½ųŠŠ£¬¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹĖęĪĀ¶ČÉżøß¼õŠ”£¬Ę½ŗāĖµĆ÷Õż·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬”÷H4Š”ÓŚĮć£¬¹ŹAÕżČ·£»
B£®Ķ¼Ļó2·ÖĪöæÉÖŖ£¬Ķ¼Ļó±ä»ÆĒ÷ŹĘĖęĪĀ¶ČÉżøßµ½400”ćCŅŌÉĻ£¬CH4ŗĶCOŃ”ŌńŠŌŹÜĪĀ¶ČÓ°Ļģ¼×Ķé¼õŠ”£¬Ņ»Ńõ»ÆĢ¼Ōö“ó£¬ĪĀ¶ČæÉÓ°Ļģ²śĪļµÄŃ”ŌńŠŌ£¬¹ŹBÕżČ·£»
C£®¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹĻČŌö“óŹĒ·“Ó¦ÕżĻņ½ųŠŠĪ““ļµ½Ę½ŗāדĢ¬£¬“ļµ½Ę½ŗāדĢ¬£¬ĖęĪĀ¶ČÉżø߶žŃõ»ÆĢ¼×Ŗ»ÆĀŹ¼õŠ”£¬¹ŹC“ķĪó£»
D£®CO2ŗĶH2»ģŗĶĘųĢå£ØĢå»ż±Č1£ŗ4£¬×ÜĪļÖŹµÄĮæa mol£©½ųŠŠ·“Ó¦£¬½«CO2ŗĶH2µÄ³õŹ¼Ģå»ż±ČøıäĪŖ1£ŗ3£¬¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹ¼õŠ”£¬¹ŹD“ķĪó£»
¹Ź“š°øĪŖ£ŗCD£»
¢ŚŌŚ³£Ń¹”¢Ru/TiO2“ß»ÆĻĀ£¬CO2ŗĶH2»ģŗĶĘųĢå£ØĢå»ż±Č1£ŗ4£¬×ÜĪļÖŹµÄĮæa mol£©½ųŠŠ·“Ó¦£¬350”ꏱ£¬·“Ó¦¢ńŌŚt1Ź±æĢ“ļµ½Ę½ŗā£¬Ę½ŗāŹ±ČŻĘ÷Ģå»żĪŖVL£¬¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹĪŖ80% CO2£Øg£©+4H2£Øg£©?CH4£Øg£©+2H2O£Øg£©
ĘšŹ¼Įæ£Ømol£© 0.2a 0.8a 0 0
±ä»ÆĮæ£Ømol£© 0.16a 0.64a 0.16a 0.32a
Ę½ŗāĮæ£Ømol£© 0.04a 0.16a 0.16a 0.32a
Ę½ŗā³£ŹżK=$\frac{\frac{0.16a}{V}”Į£Ø\frac{0.32a}{V}£©^{2}}{\frac{0.04a}{V}”Į£Ø\frac{0.16a}{V}£©^{4}}$=$\frac{625{V}^{2}}{{a}^{2}}$£¬
¹Ź“š°øĪŖ£ŗ$\frac{625{V}^{2}}{{a}^{2}}$£»
¢Ū·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ÉżĪĀĘ½ŗāÄęĻņ½ųŠŠ£¬¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹ¼õŠ”£¬Ķ¼ÖŠ·ÖĪöæÉÖŖ½Ó½ü72.5%£¬¼×ĶéĪļÖŹµÄĮæ¼õŠ”Š”ÓŚ350”ćCŹ±¼×ĶéĪļÖŹµÄĮ棬“ļµ½Ę½ŗāĖłŠčŅŖŹ±¼äĖõ¶Ģ
CO2£Øg£©+4H2£Øg£©?CH4£Øg£©+2H2O£Øg£©
ĘšŹ¼Įæ£Ømol£© 0.2a 0.8a 0 0
±ä»ÆĮæ£Ømol£© 0.145a 0.58 a 0.145a 0.29a
Ę½ŗāĮæ£Ømol£© 0.055 0.22a 0.145a 0.29a
»³öĶ¼Ļ󣬓ļµ½Ę½ŗāדĢ¬¼×Ķé 0.145a mol£¬ÉżĪĀ¼Óæģ·“Ó¦ĖŁĀŹ£¬“ļµ½Ę½ŗāĖłŠčŹ±¼äĖõ¶Ģ£¬µĆµ½Ķ¼ĻóĪŖ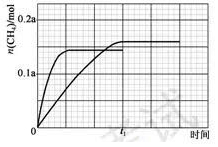 £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø3£©CO2æÉŅŌŌŚ¼īŠŌĖ®ČÜŅŗÖŠµē½āÉś³É¼×Ķ飬½įŗĻµēŗÉŹŲŗćŗĶŌ×ÓŹŲŗć£¬ÓĆĒāŃõøłĄė×ÓÅضČÅäĘ½µēŗÉŹŲŗćµĆµ½µē¼«·“Ó¦ĪŖ£ŗCO2+6H2O+8e-ØTCH4+8OH-£¬
¹Ź“š°øĪŖ£ŗCO2+6H2O+8e-ØTCH4+8OH-£®
µćĘĄ ±¾Ģāæ¼²éĮĖČČ»Æѧ·½³ĢŹ½ŹéŠ“·½·Ø”¢Ó°Ļģ»ÆŃ§Ę½ŗāŅņĖŲ·ÖĪö”¢Ķ¼ĻóµÄĄķ½āŗĶÓ¦ÓĆ”¢Ę½ŗā³£Źż¼ĘĖć”¢µē½ā³Ųµē¼«·“Ó¦ŹéŠ“£¬Ö÷ŅŖŹĒÓ°ĻģŅņĖŲ¶Ō»ÆŃ§Ę½ŗāÓ°ĻģµÄĶ¼Ļó»ęÖĘ£¬ÕĘĪÕ»ł“”ŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄŃ¶Č½Ļ“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³ĘČ”12.5gµØ·ÆÅä³É500mLČÜŅŗ | B£® | ³ĘČ”8.0gµØ·ÆÅä³É500mLČÜŅŗ | ||
| C£® | ³ĘČ”8.0gĮņĖįĶ£¬¼ÓČė500mLĖ® | D£® | ³ĘČ”7.68gĮņĖįĶ£¬¼ÓČė500mLĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 £ØÉĢĘ·Ćū³ĘĪŖ·śĄļ°ŗ-12£¬Ņ»ÖÖĻŽÖĘŹ¹ÓƵÄÖĘĄä¼Į£¬ĄąĖĘÓŚ¼×ĶéµÄ½į¹¹£©µÄŠšŹöÕżČ·µÄŹĒ£Ø””””£©
£ØÉĢĘ·Ćū³ĘĪŖ·śĄļ°ŗ-12£¬Ņ»ÖÖĻŽÖĘŹ¹ÓƵÄÖĘĄä¼Į£¬ĄąĖĘÓŚ¼×ĶéµÄ½į¹¹£©µÄŠšŹöÕżČ·µÄŹĒ£Ø””””£©| A£® | ÓŠĮ½ÖÖĶ¬·ÖŅģ¹¹Ģå | B£® | ŹĒĶéĢž | ||
| C£® | Ö»ÓŠŅ»ÖÖ½į¹¹ | D£® | ÓŠĖÄÖÖĶ¬·ÖŅģ¹¹Ģå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Cl2ÄÜÓėĖ®·“Ó¦£¬ŌŚ·“Ó¦ÖŠCl2Ö»ÄÜ×÷Ńõ»Æ¼Į | |
| B£® | Ńõ»ÆŠŌCl2£¾Br2£¾I2£¬»¹ŌŠŌCl-£¾Br-£¾I- | |
| C£® | ŹµŃéŹŅÖʱøCl2£¬æÉÓĆÅű„ŗĶŹ³ŃĪĖ®¼ÆĘų·ØŹÕ¼Æ | |
| D£® | ĀČĖ®¾ßÓŠĖįŠŌ£¬æÉÓĆpHŹŌÖ½²āĮæĘäpHÖµ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĖÄ“ØŹ”øßŅ»ÉĻ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹµŃé²Ł×÷ÖŠ£¬ĖłÓĆŅĒĘ÷ŗĻĄķµÄŹĒ£Ø £©
A. ŌŚŪįŪöÖŠ·ÅČėNaClČÜŅŗ£¬¼ÓČČ”¢Õō·¢µĆµ½NaCl¾§Ģå
B. ÓĆ10 mLµÄĮæĶ²ĮæČ”4.8 mLµÄŃĪĖį
C. ÓĆĶŠÅĢĢģĘ½³ĘČ”25.20 g NaCl
D. ÓĆ1000 mLČŻĮæĘæÅäÖĘ450 mL 0.1 mol”¤L-1µÄŃĪĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĖÄ“ØŹ”ø߶žÉĻ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø1£©æÉÄę·“Ó¦2Cl2(g)+2H2O(g  4HCl(g)+O2(g) £Ø”÷H£¾0£©£¬ŌŚŅ»¶ØĢõ¼žĻĀ“ļµ½Ę½ŗāŗ󣬷ֱš²ÉČ”ĻĀĮŠ“ėŹ©£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©£ŗ
4HCl(g)+O2(g) £Ø”÷H£¾0£©£¬ŌŚŅ»¶ØĢõ¼žĻĀ“ļµ½Ę½ŗāŗ󣬷ֱš²ÉČ”ĻĀĮŠ“ėŹ©£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©£ŗ
¢Ł½µµĶĪĀ¶Č£¬Cl2µÄ×Ŗ»ÆĀŹ___ _______£»¦Ō(Äę)______________£»
¢Ś±£³ÖČŻĘ÷Ģå»ż²»±ä£¬¼ÓČėHe£¬ŌņHClµÄĪļÖŹµÄĮæ__________”£
¢Ū±£³ÖČŻĘ÷Ń¹Ēæ²»±ä£¬¼ÓČėHe£¬ŌņO2µÄĪļÖŹµÄĮæ__________£»
¢ÜČōĪĀ¶ČŗĶĢå»ż²»±ä£¬·“Ó¦“ÓCl2ŗĶH2OæŖŹ¼ÖĮĘ½ŗā£¬ŌŚÕāøö±ä»Æ¹ż³ĢÖŠ£¬ČŻĘ÷ÄŚĘųĢåµÄĆÜ¶Č ____£¬Ļą¶Ō·Ö×ÓÖŹĮæ_________”£
£Ø2£©µŖ»Æ¹č£ØSi3N4£©ŹĒŅ»ÖÖŠĀŠĶĢՓɲÄĮĻ£¬ĖüæÉÓÉŹÆÓ¢Óė½¹ĢæŌŚøßĪĀµÄµŖĘųĮ÷ÖŠ£¬ĶعżŅŌĻĀ·“Ó¦ÖĘµĆ£ŗ3SiO2£Øs£©+ 6C(s) + 2N2(g) Si3N4(s)+ 6CO(g)
Si3N4(s)+ 6CO(g)
¢ŁøĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖ K£½ £»
¢ŚČōÖŖÉĻŹö·“Ó¦ĪŖĪüČČ·“Ó¦£¬ÉżøßĪĀ¶Č£¬ĘäĘ½ŗā³£ŹżÖµ £ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©£»ČōŅŃÖŖCOÉś ³ÉĖŁĀŹĪŖ¦Ō(CO)£½18mol”¤L-1”¤min-1£¬ŌņN2ĻūŗÄĖŁĀŹĪŖ¦Ō(N2)£½ ”£
³ÉĖŁĀŹĪŖ¦Ō(CO)£½18mol”¤L-1”¤min-1£¬ŌņN2ĻūŗÄĖŁĀŹĪŖ¦Ō(N2)£½ ”£
¢Ū“ļµ½Ę½ŗāŗó£¬øıäijŅ»Ķā½ēĢõ¼ž£Ø²»øıäN2”¢COµÄĮ棩£¬·“Ó¦ĖŁĀŹ¦ŌÓėŹ±¼ätµÄ¹ŲĻµČēĻĀĶ¼”£Ķ¼ÖŠt4Ź±ŅżĘšĘ½ŗāŅĘ¶ÆµÄĢõ¼žæÉÄÜŹĒ £»Ķ¼ÖŠ±ķŹ¾Ę½ŗā»ģŗĻĪļÖŠCOµÄŗ¬Įæ×īøßµÄŅ»¶ĪŹ±¼äŹĒ ”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĖÄ“ØŹ”ø߶žÉĻ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖ£ŗ£Ø1£©CH3COOH£Øl£©+2O2£Øg£©=2CO2£Øg£©+2H2O£Øl£©”÷H1
£Ø2£©C£Øs£©+O2£Øg£©=CO2£Øg£©”÷H2
£Ø3£©2H2£Øg£©+O2£Øg£©=2H2O£Øl£©”÷H3
£Ø4£©2CO2£Øg£©+4H2£Øg£©=CH3COOH£Øl£©+2H2O£Øl£©”÷H4
£Ø5£©2C£Øs£©+2H2£Øg£©+O2£Øg£©=CH3COOH£Øl£©”÷H5
ĻĀĮŠ¹ŲÓŚÉĻŹö·“Ó¦µÄģŹ±äµÄÅŠ¶ĻÕżČ·µÄŹĒ( )
A£®”÷H1£¾0£¬”÷H2£¼0 B£®”÷H5=2”÷H2+”÷H3©”÷H1
C£®”÷H3£¾0£¬”÷H5£¼0 D£®”÷H4=”÷H1©2”÷H3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğÉĀĪ÷Ī÷²ŲĆń×åѧŌŗø½ÖŠø߶žÉĻŌĀ漶ž»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ŃŠ¾æ»Æѧ·“Ó¦ÖŠµÄÄÜĮæ±ä»ÆÓŠÖŲŅŖŅāŅ唣Ēėøł¾ŻŃ§¹żµÄÖŖŹ¶»Ų“šĻĀĮŠĪŹĢā:
¢ń.£Ø1£©ŅŃÖŖŅ»Ńõ»ÆĢ¼ÓėĖ®ÕōĘų·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾:
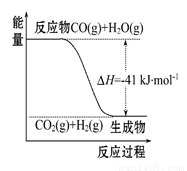
¢Ł·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ ”£
¢ŚŅŃÖŖ:C£Øs£©+H2O£Øg£©£½CO£Øg£©+H2£Øg£© ¦¤H=+131 kJ”¤mol-1,
ŌņC£Øs£©+CO2£Øg£©£½2CO£Øg£© ¦¤H= ”£
£Ø2£©»Æѧ·“Ó¦æÉŹÓĪŖ¾É¼ü¶ĻĮŃŗĶŠĀ¼üŠĪ³ÉµÄ¹ż³Ģ”£»Æѧ¼üµÄ¼üÄÜŹĒŠĪ³É£Ø»ņ²šæŖ£©1 mol»Æѧ¼üŹ±ŹĶ·Å£Ø»ņĪüŹÕ£©µÄÄÜĮ攣ŅŃÖŖ:N”ŌN¼üµÄ¼üÄÜŹĒ948.9 kJ”¤mol-1,H”ŖH¼üµÄ¼üÄÜŹĒ436.0 kJ”¤mol-1;N”ŖH¼üµÄ¼üÄÜŹĒ391
mol»Æѧ¼üŹ±ŹĶ·Å£Ø»ņĪüŹÕ£©µÄÄÜĮ攣ŅŃÖŖ:N”ŌN¼üµÄ¼üÄÜŹĒ948.9 kJ”¤mol-1,H”ŖH¼üµÄ¼üÄÜŹĒ436.0 kJ”¤mol-1;N”ŖH¼üµÄ¼üÄÜŹĒ391 .55 kJ”¤mol-1”£ŌņN
.55 kJ”¤mol-1”£ŌņN 2£Øg£©+3H2£Øg£©£½2NH3£Øg£© ¦¤H= ”£
2£Øg£©+3H2£Øg£©£½2NH3£Øg£© ¦¤H= ”£
¢ņ.ĻĀĶ¼ŹĒŅ»øö»Æѧ¹ż³ĢµÄŹ¾ŅāĶ¼,»Ų“šĻĀĮŠĪŹĢā:

£Ø1£©¼×³ŲŹĒ ×°ÖĆ,ŅŅ×°ÖĆÖŠµē¼«AµÄĆū³Ę ”£
£Ø2£©¼××°ÖĆÖŠĶØČėCH4µÄµē¼«·“Ó¦Ź½ĪŖ £¬ŅŅ×°ÖĆÖŠµē¼«B£ØAg£©µÄµē¼«·“Ó¦Ź½ĪŖ £¬±ū×°ÖĆÖŠD¼«µÄ²śĪļŹĒ £ØŠ“»ÆѧŹ½£©”£
£Ø3£©Ņ»¶ĪŹ±¼ä,µ±±ū³ŲÖŠ²śÉś112 mL£Ø±ź×¼×“æöĻĀ£©ĘųĢåŹ±,¾łŌČ½Į°č±ū³Ų,ĖłµĆČÜŅŗŌŚ25”ꏱµÄpH= ”££ØŅŃÖŖ:NaClČÜŅŗ×ćĮæ,µē½āŗóČÜŅŗĢå»żĪŖ500 mL£©”£ČōŅŖŹ¹±ū³Ų»Öø“µē½āĒ°µÄדĢ¬,Ó¦Ļņ±ū³ŲÖŠĶØČė £ØŠ“»ÆѧŹ½£©”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com