
| A����ȥCu2+��aq���л��е�����Fe3+����������ͨ�������NH3 |
| B�����к��Ȳⶨ��ʵ���У�������ƽ��ʵ������Ҫʹ��6���¶ȼ� |
| C��FeCl3��Һ��KSCN��Һ��ϣ���������ƽ�⣺FeCl3+3KSCN?Fe��SCN��3+3KCl���ﵽƽ��ʱ�����������������䣬�������м������KCl����̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�� |
| D�������£���pH�Ʋ��������ʵ���Ũ�ȵ�NaHC03��NaHS03��Һ��pH����̽��H2CO3��H2SO3���Ե����ǿ�� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na+��K+��Ag+��NO3- Ҫ����εμӰ�ˮ���г����������������ʧ |
| B��Fe3+��NO3-��I-��HCO3- Ҫ����εμ������������������ |
| C��K+��AlO2-��Cl-��MnO4- Ҫ����ɫ������Һ |
| D��NH4+��Al3+��SO42-��CH3COOH Ҫ����εμ�NaOH��Һ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��1mol M��������2mol Br2������Ӧ |
| B��M��һ�������¿��Է�����ȥ��Ӧ��ȡ����Ӧ�ͼӳɷ�Ӧ |
| C��һ��M�����������8��̼ԭ����ͬһƽ���� |
| D��1mol M��������NaOH��Һ��Ӧ������������3mol NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ֻ�Тڢ� | B��ֻ�Т� |
| C��ֻ�Тڢۢ� | D��ֻ�Т٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��84g NaHCO3�������NA��CO32- |
| B��0.1mol?L-1K2CO3��Һ�У���������������0.1NA |
| C��1.8gʯī��C60�Ļ�����У�̼ԭ����ĿΪ0.15NA |
| D����״���£�22.4L CCl4�к��еĹ��õ��Ӷ���ĿΪ4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������Ӧ�ų���������Һ�У�K+��Al3+��Cl-��SO42- |
| B��ˮ���������c��H+��=10-12mol/L����Һ Na+��Cl-��Br-��Ba2+ |
| C����������ΪNa2SO4����Һ K+��CO32-��NO3-��Al3+ |
| D�������£�pH=1����ɫ��Һ�У�Na+��Fe3+��NO3-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ϡ�����м�������������2Na+2H2O�T2Na++2OH-+H2�� |
| B�����Ȼ�����Һ�еμ�ƫ��������Һ��Fe3++3AlO2-+6H2O�TFe��OH��3��+3Al��OH��3�� |
| C����Ư����Һ����β����SO2��Ca2++2ClO-+SO2+H2O�TCaSO3��+2HClO |
| D�����Ȼ������Ȼ�þ��Һ�м�������þ��Al3++MgO+H2O�TAl��OH��3��+Mg2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
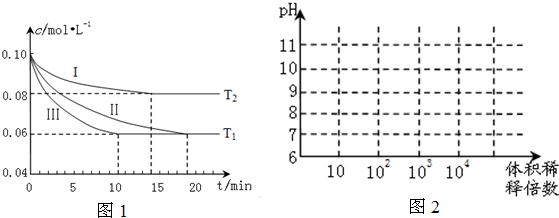
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Mg2++2HCO3-+2Ca+4OH-�TMg��OH��2��+2CaCO3��+2H2O |
| B��Cu2++H2S�TCuS��+2H+ |
| C��FeS+2H+�TH2S��+Fe2+ |
| D��H2PO3-+C2O42-�THPO32-+HC2O4- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com