
����Ŀ��(1)ijУ�о���ѧϰС���ѧ������ȡ���ռ���������̽���������й����ʣ��������ش�ʵ���е��й����⡣
��Ҫ�ռ��ϴ��ĸ��ﰱ����ʹ�õķ�����__________________________��
�ڼס�����С���ѧ������ͬ�ݻ���Բ����ƿ���ռ�һƿ���ﰱ��,����ʵ��.�������������Ȫ,˵������______����ˮ��Բ����ƿ����Һ���ɫ,˵����_____���������ɡ�
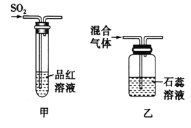
(2)ij��ȤС��Ϊ��֤SO2��Cl2��Ư����,��������·���,�������ش���������(β������װ��δ����)_____��
����ͼ����ʾ����Ʒ����Һ��ͨ��SO2,ͬѧ�Ƿ���Ʒ����Һ��ɫ��,ֹͣͨ����,�����Թ�,������Һ�ֱ�Ϊ��ɫ��˵��SO2��Ư����__________(�����ɻָ������������ɻָ�����)��
����ͼ����ʾ,�������Cl2��SO2���������1:1���,ͨ��ʯ����Һ��,����ʯ����Һ���,����ɫ,���û�ѧ����ʽ����֮:_____________________________________________________
���𰸡������ſ����� (��)�� �� �� �ɻָ��� SO2+Cl2+2H2O==H2SO4+2HCl
��������
��1���ٸ��ݰ����������ж����ռ�������
�ڼ������ڸ���Һ���������γ���Ȫ�����ݰ��������ʷ����жϣ�
��2���ٸ��ݶ��������Ư���ص�����жϣ�
�ڸ���������������������������
��1���ٰ�����������ˮ���ܶ�С�ڿ�������Ҫ�ռ��ϴ��ĸ��ﰱ����ʹ�õķ����������ſ�������
�ڰ�����������ˮ������ܲ�����Ȫ����������ˮ����һˮ�ϰ�����Һ�Լ��ԣ�����Բ����ƿ����Һ���ɫ��
��2���ٶ����������Ư������ʹƷ����Һ��ɫ�������������Ư���Dz��ȶ��ģ����Ⱥ���Һ�ָֻ���ԭ������ɫ�����˵��SO2��Ư���ǿɻָ��ġ�
����������ǿ�����ԣ��ܰѶ�����������Ϊ���ᣬͬʱ�����Ȼ��⣬�Ӷ�ʧȥƯ���ԣ����Խ������Cl2��SO2���������1:1��ϣ�ͨ��ʯ����Һ�У�����ʯ����Һ��죬������ɫ����Ӧ�ķ���ʽΪSO2+Cl2+2H2O��H2SO4+2HCl��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��ı�0.1mol��L-1��Ԫ����H2A��Һ��pH����Һ�е�H2A��HA-��A2-�����ʵ�������![]() (X)��pH�ı仯��ͼ��ʾ[��֪
(X)��pH�ı仯��ͼ��ʾ[��֪![]() (X) =
(X) =![]() ]�����������������( )
]�����������������( )

A. pH=1.2ʱ��c(K+)+c(H+)=c(H2A)+c(OH-)
B. �����£�H2A�ĵ���ƽ�ⳣ��Ka2=10-42
C. pH=2.7ʱ��c(HA-)��c(H2A)=c(A2-)
D. KHA��Һ������Ũ��Ϊc(K+)��c(HA-)��c(OH-)��c(H2A)��c(H+)��c(A2-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���Ӧ![]() +H2O
+H2O![]() H2CO3+OH��ƽ�ⳣ��K=2.2��108����NH4HCO3��Һ�Ͱ�ˮ��һ��������ϣ������ڽ�ȡ�����е�ZnO������Һ������������仯�ɺ��ԣ�����ʱ����ָ����Һ�������ʵ���Ũ�ȹ�ϵ��ȷ����
H2CO3+OH��ƽ�ⳣ��K=2.2��108����NH4HCO3��Һ�Ͱ�ˮ��һ��������ϣ������ڽ�ȡ�����е�ZnO������Һ������������仯�ɺ��ԣ�����ʱ����ָ����Һ�������ʵ���Ũ�ȹ�ϵ��ȷ����
A. 0.2mol��L1��ˮ��c(NH3��H2O)>c(![]() )>c(OH)>c(H+)
)>c(OH)>c(H+)
B. 0.2mol��L1NH4HCO3��Һ(pH>7)��c(![]() )>c(
)>c(![]() )>c(H2CO3)>c(NH3��H2O)
)>c(H2CO3)>c(NH3��H2O)
C. 0.2mol��L1��ˮ��0.2mol��L1NH4HCO3��Һ�������ϣ�c(![]() )+c(NH3��H2O)=c(H2CO3)+c(
)+c(NH3��H2O)=c(H2CO3)+c(![]() )+c(
)+c(![]() )
)
D. 0.6mol��L1��ˮ��0.2mol��L1NH4HCO3��Һ�������ϣ�c(NH3��H2O)+c(![]() )+c(OH)=0.3mol��L1+c(H2CO3)+c(H+)
)+c(OH)=0.3mol��L1+c(H2CO3)+c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʽ������þ[Mg2ClO(OH)3��H2O]����ˮ������ʪ������ȶ�����һ���п�����ֵ������������ij�з�С��ͨ�����������Ʊ���ʽ������þ��
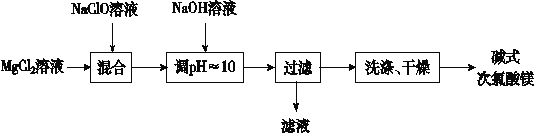
��1�����������й��˲������õIJ���������__________
��2�������������п����жϣ���Һ�пɻ��յ���Ҫ������__________��
��3��NaClO��Һ��Cl2��NaOH��Һ��Ӧ��ã�д���÷�Ӧ�Ļ�ѧ����ʽ��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ���ʼ��仯�����ںܶ���������Ҫ����;�������ͭ����������ߵ��£���ˮ����ͭ������ɱ������
��1��Cuλ��Ԫ�����ڱ���IB�塣Cu2+�ĺ�������Ų�ʽΪ____________��
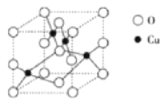
��2����ͼ��ͭ��ij��������ľ����ṹʾ��ͼ����ȷ���þ����������ӵĸ���Ϊ___________��
��3��������ͭ��Һ�м��������ˮ��������[Cu(NH3)4]2+�����ӡ���֪NF3��NH3�Ŀռ�ṹ���������Σ���NF3������Cu2-�γ������ӣ���ԭ����__________��
��4��Cu2O���۵��Cu2S��________����ߡ��͡���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�к��д�����K+��Cl-��Br-������������Ca2+��Mg2+��SO42-��ij�о���ѧϰС���������ַ�Һ����ȡ�ϴ������Ȼ��ؾ��弰Һ�壨Br2�������������ɫҺ�壩���������������ͼ��
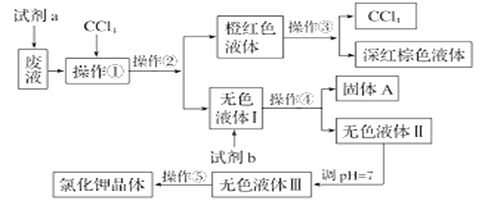
���������ͼ���ش�������⣺
(1)���Լ�aΪH2O2��Һ(H��)����֪�����ԣ�H2O2>Br2
��д����Һ�е�ij�����Ӻ�a������Ӧ�����ӷ���ʽΪ��__________________________��
��ÿ����0.2mol H2O2����Ӧת�Ƶĵ���Ϊ______mol��
(2)Ϊ�˳�ȥ��ɫҺ��I�е�Ca2+��Mg2+��SO42-���Լ�b��ѡ��KOH��BaCl2��K2CO3��Һ��������˳����ȷ������_______��
A��KOH��BaCl2��K2CO3 B��BaCl2��KOH��K2CO3
C��BaCl2��K2CO3 ��KOH D��KOH��K2CO3 ��BaCl2
(3)�������pH=7(����)��Ϊ�˳�ȥ��������___��___��������Ȼ��ؾ���Ĵ��ȣ�
(4)�����٢ڢۢܢ���Ӧ�����Ʒֱ��ǣ�____����Һ��_____�����ˡ�______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A. �л��![]() ��������Ϊ2-��-1-����
��������Ϊ2-��-1-����
B. ���Ӵ��� ���ܷ���������ȡ����ˮ�⡢�Ӿ۷�Ӧ
���ܷ���������ȡ����ˮ�⡢�Ӿ۷�Ӧ
C. 1mol��ԭ�ᣨ ����������ˮ��Ӧ���������4molBr2
����������ˮ��Ӧ���������4molBr2
D. �л���׳ơ�һ���㡱���� ����һ�ֺ�������ͬ���칹���ܷ���������Ӧ
����һ�ֺ�������ͬ���칹���ܷ���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����CO��H2Ϊԭ�Ϻϳɼ״��ķ�Ӧ��CO(g)+2H2(g)![]() CH3OH(g) ��H��0�����ݻ�Ϊ1 L�ĺ��������У��ֱ���T1��T2��T3�����¶��ºϳɼ״�����ͼ�����������¶��²�ͬH2��CO����ʼ��ɱȣ���ʼʱCO�����ʵ�����Ϊ1mol����COƽ��ת���ʵĹ�ϵ������˵����ȷ����
CH3OH(g) ��H��0�����ݻ�Ϊ1 L�ĺ��������У��ֱ���T1��T2��T3�����¶��ºϳɼ״�����ͼ�����������¶��²�ͬH2��CO����ʼ��ɱȣ���ʼʱCO�����ʵ�����Ϊ1mol����COƽ��ת���ʵĹ�ϵ������˵����ȷ����
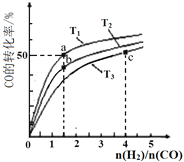
A. H2ת���ʣ�a��b��c
B. ���������¶�֮���ϵΪT1��T2��T3
C. a��״̬����ͨ��0.5 mol CO��0.5 mol CH3OH��ƽ�����������ƶ�
D. c��״̬����ͨ��1 molCO��4 mol H2����ƽ����CH3OH�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������Ҫ�Ĺ���Ԫ�ء���ش��������⣺
��1������Ԫ�����ڱ��е�λ����___________�����̬ԭ�ӵļ۵����Ų�ͼΪ___________��
��2��FeCO3�����������Ҫ�ɷ֣�����Cԭ�ӵ��ӻ���ʽΪ________�������еĴ��������÷�����![]() ��ʾ������m���������γɴ�������ԭ������n���������γɴ������ĵ�����(�籽�����еĴ������ɱ�ʾΪ��
��ʾ������m���������γɴ�������ԭ������n���������γɴ������ĵ�����(�籽�����еĴ������ɱ�ʾΪ��![]() )����CO32���еĴ�����Ӧ��ʾΪ________��
)����CO32���еĴ�����Ӧ��ʾΪ________��
��3����֪Fe2+�뾶Ϊ61pm��Co2+�뾶Ϊ65pm���ڸ������������·ֱ����FeCO3��CoCO3��ʵ����FeCO3���ȷֽ��¶ȵ���CoCO3����ԭ�������______��
��4��Co(NH3)5Cl3���ܵ�һ��������0.01mol����������Һ�м�������AgNO3��Һ�����ɰ�ɫ����2.87g�������������λ��Ϊ_____��
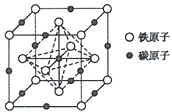
��5����������̼�ܽ���r��Fe���γɵ�һ�ּ�϶�����壬���ԣ��侧��Ϊ���������ṹ(��ͼ��ʾ)����þ���������ԭ�Ӿ����������ԭ����ĿΪ___________�����þ�������Ϊa pm����þ�����ܶ�Ϊ___________g��cm��3(�����ӵ�������ֵ��NA��ʾ)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com